Focus
Publié le 31 mai 2015Lecture 9 min
Le MitraClip® en France en 2015- Pour quels patients ? Comment les sélectionner ?
É. BROCHET, D. HIMBERT, D. MESSIKA-ZEITOUN, B. IUNG, A. VAHANIAN, Département de cardiologie, hôpital Bichat, Paris
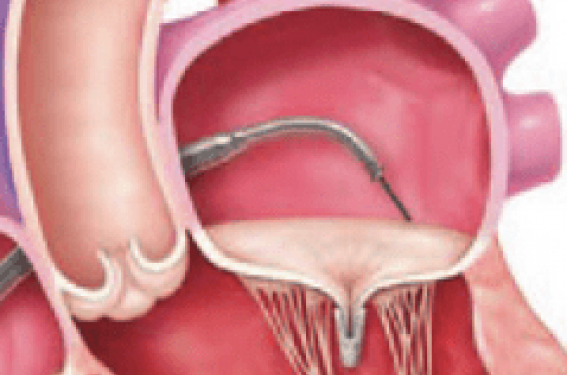
Introduit en 2003, le MitraClip® (Abbott Vascular) s’inspire de la technique chirurgicale de suture « bord à bord » des feuillets mitraux (technique d’Alfieri), visant à réduire l’insuffisance mitrale (IM) par création d’un double orifice. Dans l’approche percutanée, la capture du bord libre des feuillets mitraux est réalisée à l’aide d’un clip repositionnable introduit dans l’oreillette gauche par cathétérisme transseptal (figure 1). Cette technique permet de traiter aussi bien des IM primaires (ou organiques), par prolapsus, que les IM secondaires (ou fonctionnelles) des cardiopathies dilatées ou ischémiques.
Figure 1. Représentation schématique de la procédure MitraClip®. A : Positionnement du clip dans l’oreillette gauche après cathétérisme transseptal. B : Capture des feuillets mitraux au niveau du bord libre de A2 et P2. C : Aspect de double orifice mitral. D : Largage du clip après vérification de son bon positionnement.
Le MitraClip® reste actuellement la seule technique percutanée de réparation mitrale disponible commercialement. Depuis sa mise sur le marché en 2008, vingt mille patients ont été traités dans le monde et 400 patients sont implantés en Europe chaque mois (source Abbott). En France, 300 patients ont été implantés à ce jour. Ces disparités d’implantation importantes sont principalement liées aux conditions de remboursement du dispositif selon les pays.
Le MitraClip®, quelle validation ?
La validation principale du système MitraClip® vient de l’étude EVEREST-II, étude randomisée contre la chirurgie, et plus récemment par les registres rapportant l’expérience européenne qui a suivi sa commercialisation (ACCESS-EU, expérience de Hambourg).
Dans l’étude EVEREST-II, les patients avec IM sévère étaient randomisés entre MitraClip® et chirurgie.
Les résultats immédiats ont confirmé la faisabilité de la procédure avec un taux de succès très élevé et sa sécurité avec un taux de complications très faible, inférieur à celui de la chirurgie. Les résultats à 5 ans montrent un bénéfice comparable dans les deux groupes en termes d’amélioration fonctionnelle et de remodelage ventriculaire gauche.
En revanche, il existe un taux plus élevé d’insuffisances mitrales résiduelles dans le groupe MitraClip®, avec un taux de réintervention également plus élevé après MitraClip® (25 % vs 5 % des cas dans le groupe chirurgical). Il est à noter que dans cette étude, compte tenu de la comparaison nécessaire avec la chirurgie, les patients étaient à risque modéré, et principalement (deux tiers des cas) des IM organiques par prolapsus (IM dites « primaires »).
Après sa commercialisation en 2008, le système MitraClip® a connu un développement rapide en Europe du Nord, notamment en Allemagne. Les patients traités par MitraClip® diffèrent radicalement de ceux testés dans l’étude EVEREST, incluant en majorité (80 %) des patients à haut risque, avec beaucoup de comorbidités, souvent inopérables et principalement des IM secondaires ou fonctionnelles avec dysfonction ventriculaire gauche. Malgré ces différences, les registres européens confirment la faisabilité et la sécurité de la procédure, et une amélioration symptomatique et de la qualité de vie significative en cas de succès. Il est important de noter qu’il s’agit d’une réduction et non d’une suppression de l’IM, avec persistance d’une IM légère à modérée dans la majorité des cas.
Technique du MitraClip® : une procédure échoguidée
La technique MitraClip® est une procédure complexe, mais son taux de succès dépasse 95 % dans les équipes entraînées, grâce à des protocoles très standardisés et un guidage très précis, radioscopique et surtout échocardiographique. Le rôle de l’ETO est en effet essentiel pendant toute la procédure, avec un apport très important de l’ETO 3D. La qualité du résultat dépend en grande partie de la bonne communication entre échographistes et cardiologues interventionnels.
La première étape consiste en un cathétérisme transseptal très précis dont la position est guidée par l’ETO. Le clip est ensuite introduit dans l’oreillette gauche, toujours sous contrôle ETO et guidé vers l’orifice mitral pour s’aligner avec le jet d’IM. Le clip est ensuite ouvert et placé perpendiculairement aux feuillets valvulaires.
Il est ensuite introduit dans le ventricule gauche et progressivement remonté sous le bord libre des feuillets mitraux. Lorsque la position est satisfaisante, les bras du clip sont fermés pour capturer les feuillets. Si la capture valvulaire paraît de bonne qualité et que l’IM a diminué, le clip est largué. En cas de réduction insuffisante de l’IM, un deuxième clip peut être mis en place (figure 2).
Figure 2. Guidage échographique par ETO 3D de la procédure MitraClip®. Images du haut, cathétérisme transseptal échoguidé et positionnement du clip en face de la valve mitrale sous contrôle ETO 3D. Images du bas : capture des feuillets et évaluation de l’insertion du clip (ETO 3D), puis largage du clip avec aspect de double orifice mitral (vue en face à partir de l’OG).
Le MitraClip® : pour quels patients ?
Importance de la Heart team
Le traitement percutané de l’insuffisance mitrale (IM), dominé actuellement par le MitraClip®, s’adresse aux patients présentant une IM sévère symptomatique non éligibles pour la chirurgie en raison d’un risque opératoire trop élevé ou de contre-indications. Déjà en 2005, l’étude Euro Heart Survey avait montré que 50 % des patients ayant une indication opératoire formelle selon les recommandations n’étaient pas adressés à la chirurgie du fait de l’âge, d’une dysfonction ventriculaire gauche ou de comorbidités.
La sélection des patients est à la fois clinique et échographique.
La sélection clinique des patients est essentielle. Comme l’ont précisé les recommandations européennes pour la prise en charge des valvulopathies et pour le traitement de l’insuffisance cardiaque (2012), le traitement par MitraClip® peut être envisagé pour améliorer les symptômes chez les patients porteurs d’IM primaire ou secondaire, restant symptomatiques malgré un traitement médical optimal (incluant, si indiqué, la resynchronisation et/ou une revascularisation coronaire).
Les recommandations insistent sur la nécessité d’une évaluation multidisciplinaire de ces patients (« Heart team »), incluant des chirurgiens et anesthésistes, jugeant le patient inopérable ou à haut risque pour la chirurgie et estimant son espérance de vie à plus d’un an.
Les recommandations ajoutent qu’il est nécessaire de valider ces indications par des études randomisées.
Aux États-Unis, les recommandations pour le traitement de l’insuffisance cardiaque vont dans le même sens. Par contre, la FDA limite l’indication potentielle de cette technique aux patients ayant une IM primaire, d’origine dégénérative, en attendant des données complémentaires dans l’IM secondaire.
L’échocardiographie : élément essentiel de la sélection
Comme le soulignent également les recommandations européennes, les patients qui répondent aux critères de sélection clinique doivent également répondre aux critères échographiques d’éligibilité.
L’analyse échographique est en effet essentielle pour une sélection optimale de ces patients et le succès de la procédure (figure 3).
L’échographie transthoracique (ETT) est l’étape initiale, systématique et complète, essentielle pour une première évaluation de l’indication et de la faisabilité.
Figure 3. Sélection échographique pour MitraClip® (IM secondaire). Paramètres à recueillir en échographie transthoracique (ETT) et transoesophagiennne (ETO).
Les questions auxquelles doit répondre l’ETT
Elles sont principalement six :
- l’IM est-elle primaire (organique) ou secondaire (fonctionnelle) ?
- l’IM est-elle sévère ?
- la morphologie valvulaire estelle compatible avec le MitraClip® ?
- quel est le degré de dysfonction ventriculaire gauche et droit ?
- existe-t-il d’autres valvulopathies (aortique, tricuspide) significatives ?
- existe-t-il des contre-indications anatomiques ou techniques à la procédure MitraClip® ?
Les éléments à recueillir en échographie
Ils comprennent notamment :
L’analyse de l’anatomie valvulaire et des mécanismes de dysfonction :
- en cas d’IM secondaire l’anatomie est normale et le mécanisme de dysfonction est une restriction valvulaire systolique (type IIIb de Carpentier), avec déplacement apical du point de coaptation et déformation valvulaire (tenting) ;
- en cas d’IM primaire, l’anatomie est anormale et il faut confirmer le mécanisme de dysfonction (type II de Carpentier en cas de prolapsus, seule atteinte organique accessible au MitraClip®) ;
La sévérité de l’IM doit être appréciée par une approche multiparamétrique, en utilisant des critères quantitatifs (SOR et VR), et en se rappelant que les seuils de sévérité sont différents en cas d’IM primaire et secondaire.
Des critères échographiques de faisabilité ont été développés et validés dans l’étude EVEREST (tableau). Les éléments importants à retenir sont :
- la localisation du jet régurgitant qui doit être idéalement centrale, en provenance de A2 ou P2 (coupe petit axe et 2 cavités en ETT) ;
- en cas d’IM primaire, un prolapsus modéré (profondeur ou gap de moins de 10 mm, peu large (< 15 mm) et situé dans la zone centrale (A2 ou P2) ;
- en cas d’IM secondaire, une déformation valvulaire modérée avec persistance d’une coaptation > 2 mm et hauteur de tenting < 11 mm ;
- la technique est contre-indiquée ou non faisable s’il existe des calcifications annulaires ou valvulaires, notamment dans la zone de capture des feuillets, une surface mitrale insuffisante (< 4 cm2), un large défaut de coaptation ou des feuillets valvulaires trop courts ou trop restrictifs (longueur de la partie mobile du feuillet postérieur < 10 mm) ou enfin des prolapsus complexes, bivalvulaires ou commissuraux ;
- de même, les IM primaires d’autre origine (rhumatismale, post-endocarditique) et les IM restrictives d’autre origine (postradique, médicamenteuses) ne sont pas accessibles à cette technique.
L’échographie transoesophagienne (ETO) est systématique, permettant une analyse plus détaillée de l’anatomie mitrale des mesures plus précises concernant la faisabilité de la procédure (coaptation résiduelle, symétrie ou non de l’orifice régurgitant, épaisseur du bord libre des feuillets). L’ETO exclut une thrombose intra-auriculaire gauche ou une anomalie du septum interauriculaire empêchant la faisabilité de l’abord transseptal. L’ETO 3D permet un bilan lésionnel très précis ainsi que la recherche de contre-indications non visibles en ETO 2D comme une fente mitrale. L’ETO permet également d’apprécier la qualité de l’imagerie, condition essentielle de la réussite de la procédure.
Si les meilleurs résultats sont obtenus dans les IM centrales, respectant les critères décrits ci-dessus (critères « EVEREST »), des résultats satisfaisants peuvent également être obtenus dans des formes anatomiques plus complexes, non centrales notamment, comme l’ont montré certaines études récentes. Ces indications doivent néanmoins être analysées au cas par cas et nécessitent une bonne expérience des équipes.
Le MitraClip® en France : protocole MITRA-FR
En attendant un remboursement du MitraClip® en France, l’accès au MitraClip® n’est actuellement possible en France que dans le cadre de l’étude randomisée MITRA-FR (coordonnée par l’hôpital Louis Pradel à Lyon, Pr J.-F. Obadia). Cette étude multicentrique, incluant 21 centres en France. vise à mettre en évidence l’efficacité du MitraClip® par rapport au traitement médical optimal chez des patients présentant une IM secondaire avec dysfonction ventriculaire gauche (FEVG < 40 %) restant symptomatiques malgré le traitement. L’objectif est d’étudier la réduction du pourcentage de décès toutes causes ou d’hospitalisations non programmées insuffisance cardiaque à 12 mois après la randomisation.
Les patients potentiellement éligibles doivent être adressés aux centres participants pour une évaluation clinique et échographique. Après validation des critères d’inclusion, et notamment de l’échographie par un laboratoire central de revue (Core Lab), les patients sont randomisés entre le bras « MitraClip® » ou le bras « traitement médical optimal ».
Les critères de sélection du protocole multicentrique français sont résumés dans l’encadré.
Questions résiduelles et perspectives
En l’absence d’études randomisées dans les groupes de patients réellement candidats à la technique (groupes à haut risque), des données complémentaires sont nécessaires pour mieux préciser les indications de ce traitement.
Dans l’IM secondaire avec dysfonction VG, on attend beaucoup des résultats des essais randomisés en cours dans les pays où le MitraClip® n’est pas disponible commercialement dans cette indication (COAPT aux États-Unis et MITRA-FR en France). L’étude européenne RESHAPE est actuellement interrompue en raison d’un recrutement insuffisant.
Dans les IM primaires dégénératives à haut risque (âge, dysfonction ventriculaire gauche) ou contre-indiqués pour la chirurgie, aucun essai n’est pour l’instant débuté.
Par ailleurs, d’autres techniques percutanées de traitement de l’IM en cours de développement. Citons notamment les techniques d’annuloplastie directe par voie transseptale (Cardioband, Valtech®) ou indirecte (Mitralign, Inc.®), ou les techniques d’implantation de néocordages par voie apicale (NeoChord, Inc.®). La place du MitraClip®, seul ou en combinaison avec ces techniques reste à évaluer.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :






