Publié le 02 juin 2013Lecture 8 min
L’imagerie par résonance magnétique dans les urgences cardiologiques
F. SANGUINETI, M. MANA, J. GAROT, IRM cardiovasculaire, Institut Cardiovasculaire Paris-Sud, Hôpital Privé Jacques Cartier, Massy
En pratique, l’IRM a une place relativement modeste dans le diagnostic et la prise en charge des urgences cardiologiques. Cependant, il s’agit d’un examen ayant une grande valeur diagnostique dans diverses situations d’urgence et qui peut, lorsqu’elle est disponible rapidement, faciliter et accélérer la prise en charge des patients. Dans ce chapitre, nous essaierons de synthétiser les situations cliniques « urgentes » pour lesquelles l’IRM est susceptible de porter un diagnostic, de raccourcir et d’améliorer la prise en charge.
Douleur thoracique aiguë compatible avec une pathologie ischémique mais avec un ECG non contributif
Il s’agit d’une situation diagnostique souvent délicate, chez des patients présentant plus ou moins de facteurs de risque cardiovasculaire, et avec parfois une élévation modérée de la troponine. Cependant, l’ECG ne montre pas de signes spécifiques (pas de sus-décalage du ST notamment) et l’IRM, si elle peut être réalisée très rapidement, apporte une aide substantielle pour le diagnostic et le traitement.
Myocardite
Le plus souvent, il s’agit d’un(e) patient(e) jeune, ayant un risque cardiovasculaire global faible ou modéré, et qui présente une douleur thoracique aiguë, souvent dans un contexte d’infection virale aiguë ou récente. En l’absence de sus-décalage soutenu du ST, il est possible de réaliser une IRM cardiaque dans ce contexte d’urgence. En cas de sus-décalage du ST, il faut réaliser une coronarographie en urgence afin de ne pas perdre de temps en cas d’infarctus aigu. L’IRM pourra alors être réalisée dans un second temps si la coronarographie est normale. Dans ces situations cliniques fréquentes, l’IRM permet de porter le diagnostic de myocardite aiguë. Les séquences réalisées permettent l’analyse de la fonction VG globale et segmentaire (ciné-IRM), la mise en évidence d’un œdème intramyocardique avec des foyers en mottes intramyocardiques ou sous-épicardiques (sang noir T2), d’une perfusion myocardique normale au repos (diagnostic différentiel avec un SCA) et montrent plusieurs foyers distincts de rehaussement en mottes après injection de gadolinium, intramyocardiques ou sous-épicardiques, souvent déjà présents précocement (2-3 min après l’injection) ainsi qu’à 10-15 min (figure 1). Cette sémiologie est très spécifique du diagnostic de myocardite aiguë et s’oppose en tout point au diagnostic de SCA(1). L’IRM permet aussi de visualiser l’épanchement péricardique lorsqu’il est présent.
Figure 1. Patient de 22 ans ayant présenté une douleur thoracique prolongée avec des signes ECG non spécifiques et une élévation modérée de troponine. Pas d’anomalie de cinétique segmentaire en écho ou en ciné-IRM. L’IRM montre une zone d’œdème intramyocardique au niveau de la paroi antéro-latérale (hypersignal T2 spontané, A, flèche), avec des plages de rehaussement tardif nodulaires et linéaires intramyocardiques et sous-épicardiques en faveur d’une myocardite aiguë inflammatoire antéro-latérale (B-C, flèches). La perfusion myocardique était homogène dans les conditions de base.
SCA
La présentation clinique est souvent assez proche de la précédente. Il s’agit d’un patient ayant un risque cardiovasculaire global modéré ou intermédiaire, qui a présenté une douleur thoracique prolongée compatible avec un angor, sans signe ECG évocateur au décours. L’IRM peut être réalisée dans les conditions de base au repos, mais aussi au cours d’un stress pharmacologique afin de sensibiliser le diagnostic. L’étude de la fonction VG segmentaire montre souvent une anomalie focale de cinétique. L’imagerie T2 sang noir peut montrer une zone limitée d’œdème myocardique. La perfusion myocardique au repos met souvent en évidence un déficit localisé de perfusion, souvent visible au repos (et a fortiori au cours du stress). S’il y a eu une élévation même modeste de la troponine, l’étude du rehaussement tardif met en évidence un petit foyer unique de rehaussement sous-endocardique, au sein d’un territoire coronaire (figure 2)(2). Le tableau synthétise les principaux éléments du diagnostic différentiel entre la myocardite et le SCA. Les implications thérapeutiques sont majeures. En cas de SCA, avec une zone de myocarde à risque, même très peu étendue, le traitement de prévention secondaire est absolument nécessaire et permet une réduction marquée du risque de récidive.
Tableau. Diagnostic différentiel entre SCA et myocardite.
Figure 2. Patient hypercholestérolémique de 45 ans ayant présenté une douleur thoracique de 40 min. Les signes ECG ne sont pas spécifiques à son arrivée. La troponine est modérément élevée. L’IRM montre une hypokinésie inféro-latérale basale limitée, avec un petit déficit de perfusion inféro-latéral basal au repos (A, flèche). Il existe en rehaussement tardif, une petite zone d’infarctus sous-endocardique limité en inféro-latéral, signant le SCA (B, flèche).
Tako-Tsubo
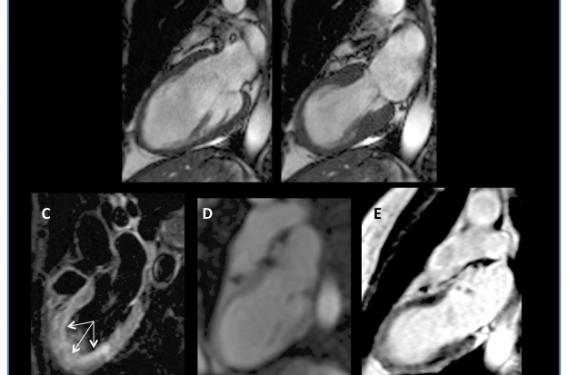
Il s’agit le plus souvent d’une femme âgée, ayant présenté une douleur thoracique aiguë au décours d’un stress émotionnel ou physique. L’ECG montre souvent des signes non spécifiques, et la troponine est modestement élevée. La coronarographie ne montre pas de lésion critique thrombotique. Le plus souvent, le ciné-IRM montre une anomalie de cinétique segmentaire apicale étendue, dépassant le territoire de l’IVA (« ballooning » apical). Les formes médio-ventriculaires symétriques ou les formes basales sont moins fréquentes. Si l’examen est réalisé très tôt, on note un léger œdème myocardique en T2 au sein de la zone asynergique. La perfusion myocardique reste homogène au repos. Dans l’immense majorité des cas, il n’y a pas de rehaussement tardif 10 min après injection de contraste (figure 3)(3). La récupération fonctionnelle se fait spontanément en 6 semaines et le traitement de prévention secondaire n’est pas indiqué.
Figure 3. Patiente dyslipidémique de 68 ans ayant présenté une douleur thoracique prolongée de 45 min avec des ondes T négatives sur les précordiales à son arrivée. La troponine est modérément élevée. Le ciné-IRM montre une zone d’akinésie apicale (« ballooning »), dépassant le territoire de l’IVA (A-B). Il existe une zone en hypersignal T2 spontané intramyocardique à l’apex traduisant un œdème myocardique (C, flèches), la perfusion myocardique est homogène à l’apex dans les conditions de base (D). Il n’y a pas de zone de rehaussement tardif apical (E), ces éléments étant en faveur d’un Tako-Tsubo (pas de séquelle de myocardite, pas d’infarctus du myocarde).
CMH
Il s’agit d’une 4e situation clinique assez similaire, la pathologie étant parfois révélée par une douleur thoracique prolongée, avec un ECG montrant souvent des ondes T négatives symétriques sur les précordiales. Dans ce contexte, l’IRM permet parfois le diagnostic de CMH, notamment apicale. Le ciné-IRM permet une bonne analyse morphologique de l’ensemble des parois VG et la mise en évidence d’une CMH focale difficile à visualiser en échographie (formes apicales, antérieures strictes, antéro-latérales) (figures 4A et 4B). Il n’y a pas d’œdème myocardique franc en imagerie T2 sang noir. L’imagerie dynamique de perfusion montre parfois plusieurs petits foyers intramyocardiques de déficit de perfusion au sein des segments hypertrophiés. L’imagerie de rehaussement tardif met en évidence un rehaussement intramyocardique en patch, signant la désorganisation architecturale des fibres myocardiques et la présence de fibrose intramyocardique (figure 4C)(4). La douleur thoracique aiguë est expliquée par des phénomènes ischémiques et par l’hypertrophie ventriculaire. La troponine est souvent modérément élevée. Les implications de ce diagnostic pour la prise en charge et le traitement sont spécifiques et majeures (bêtabloquant, évaluation du risque rythmique, enquête familiale).
Figure 4. Patient de 28 ans ayant présenté une douleur thoracique prolongée avec un ECG non spécifique au décours (ondes T négatives sur les précordiales). La troponine est modérément élevée. Le ciné-IRM met en évidence une forme antéro-septale focale de cardiomyopathie hypertrophique (épaisseur 31 mm), sans obstruction (A-B). Il existe des plages de rehaussement tardif intramyocardiques diffuses, en patch, au sein du segment hypertrophié, traduisant la présence de fibrose intramyocardique (facteur pronostique) (C, flèche).
Syndromes aortiques aigus
L’IRM n’est en général pas une technique de première ligne pour le diagnostic des syndromes aortiques aigus en urgence. Elle est en effet moins disponible que le scanner, plus longue à réaliser et les images sont plus délicates à acquérir dans le contexte. Cependant, l’IRM a une grande valeur diagnostique pour mettre en évidence les différentes formes anatomiques de dissection aortique aiguë : flap, vrai et faux chenal (figure 5A), extension de la dissection, extension aux vaisseaux collatéraux, hématome pariétal aortique (figure 5B), ulcère pénétrant aortique (figure 5C).
Figure 5. A. Dissection aortique avec porte d’entrée isthmique, avec un vrai chenal (*), un flap, et un faux chenal peu circulant (**). B. Hématome pariétal aortique récent se traduisant par un hypersignal T1 spontané en croissant de la paroi aortique (flèche). C. Ulcère athéromateux pénétrant diagnostiqué par l’angio-IRM tridimensionnelle (flèche).
Urgences rythmologiques
Au décours d’une TV ou d’une syncope inexpliquée survenant à l’effort chez un sujet jeune, parfois dans un contexte familial de pathologie rythmique ou de mort subite, l’IRM est un examen clé pour le diagnostic de dysplasie du VD. Les critères majeurs du diagnostic sont les suivants(5) :
– existence d’une zone d’asynergie segmentaire du VD sur le ciné-IRM (figure 6A), et au moins l’un des 2 critères suivants :
– FE VD ≤ 40 % et/ou volume VD ≥ 110 ml/m2 chez l‘homme ;
– FE VD ≤ 40 % et/ou volume VD ≥ 100 ml/m2 chez la femme.
L’imagerie permet aussi parfois de mettre en évidence la présence de graisse intramyocardique en T1 (figure 6B) ou de fibrose intramyocardique sur les séquences en rehaussement tardif (figure 6C), ces éléments venant alors conforter le diagnostic. L’atteinte biventriculaire est fréquente.
Figure 6. A. Ciné-IRM (systole et diastole) mettant en évidence une dysplasie biventriculaire avec une dyskinésie infundibulaire pulmonaire (flèches) et une atteinte du VG (falciforme). B. Présence de graisse intramyocardique médio-pariétale et sous-épicardique (hyper T1 spontané, flèches). C. Fibrose intramyocardique au niveau du VD et du VG en rehaussement tardif (flèches).
Embolie pulmonaire
L’examen de référence pour le diagnostic d’embolie pulmonaire aiguë est le scanner avec injection. Cependant, il est possible de redresser ce diagnostic avec l’IRM. L’imagerie ciné-IRM passant par le tronc et les branches de l’AP permet de mettre en évidence un thrombus proximal. La sensibilité pour la détection des embolies pulmonaires est beaucoup moins bonne que celle du scanner. L’angiographie pulmonaire tridimensionnelle par résonance magnétique peut mettre en évidence des thrombus intraluminaux, s’ils sont suffisamment gros et proximaux.
Lorsqu’elle est disponible, l’IRM cardiaque est une modalité qui permet de manière unique de faire le diagnostic différentiel dans le contexte de douleur thoracique aiguë avec un ECG non diagnostique. Dans cette situation d’urgence, l’IRM permet de distinguer la myocardite aiguë, le syndrome coronaire aigu, la cardiomyopathie de stress, ou une douleur aiguë au cours d’une CMH. Les implications pour la prise en charge et le traitement sont souvent majeures. L’organisation d’un plateau technique autorisant la réalisation rapide de l’examen permet de raccourcir les délais de prise en charge et les séjours hospitaliers de nombreux patients, et d’instaurer rapidement les thérapeutiques adaptées.
"Cardiologie Pratique : publication avancée en ligne".
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :