Cardiologie générale
Publié le 24 juin 2008Lecture 16 min
Apnée du sommeil : quel impact pour le cardiologue ?
M.-P. d’ORTHO, hôpital Henri Mondor, Créteil
Les syndromes d’apnées du sommeil se caractérisent par la survenue répétitive d’apnées et d’hypopnées au cours du sommeil. Leur prévalence chez les patients déjà porteurs de pathologies cardiovasculaires est élevée : de 30 à 80 % selon les sous-groupes de patients. Leur dépistage systématique est donc justifié. Le SAS des patients insuffisants cardiaques peut prendre plusieurs formes : obstructif, central, ou mixte, à l’inverse de ce qui se voit dans la population générale où le SAS est pour 90 % de type obstructif. Le syndrome d’apnées obstructives du sommeil constitue un facteur de risque cardiovasculaire indépendant.
Ces événements respiratoires nocturnes induisent une importante désorganisation de l’architecture du sommeil qui explique le retentissement sur la vigilance diurne et les fonctions cognitives.
Tant les conséquences socioprofessionnelles des troubles de la vigilance et la détérioration de la qualité de vie que les fréquentes complications cardio- et cérébrovasculaires du syndrome d’apnées du sommeil en font un véritable problème de santé publique.
L’individualisation du syndrome d’apnées du sommeil est relativement récente. Pourtant, Charles Dickens nous avait laissé une description remarquable du SAS obstructif à travers le personnage de Joe dans « les aventures de Mr Pickwick » en 1837. L’équipe du Dr Burwell dénommera ce tableau en 1956, le « syndrome de Pickwick ». En 1965, le Dr Gastaut découvrira et enregistrera des pauses respiratoires (apnées) répétées chez ces malades « pickwickiens ». Enfin, ce syndrome sera identifié chez des sujets non obèses en 1976. Les études épidémiologiques récentes indiquent clairement qu’il s’agit d’une pathologie fréquente touchant 5 à 10 % de la population générale entre 35 et 60 ans.
Encore insuffisamment reconnu, le syndrome d’apnées du sommeil se caractérise par la survenue répétitive d’apnées et d’hypopnées au cours du sommeil. Les phénomènes d’hypoxie répétée secondaires aux apnées expliquent en partie la morbi-mortalité cardiovasculaire. La détérioration de la qualité de vie que les fréquentes complications cardio- et cérébrovasculaires du syndrome d’apnées du sommeil en font un véritable problème de santé publique. En parallèle, plusieurs études ont démontré l’effet bénéfique du traitement.
Définitions
Le syndrome d’apnées du sommeil est défini par la survenue au cours du sommeil d’apnées et/ou d’hypopnées. Ces événements respiratoires sont définis par l’interruption (apnée) ou la diminution de plus de 50 % (hypopnée) du flux inspiratoire, durant plus de 10 secondes, survenant en nombre supérieur à 10/h de sommeil.
Les apnées d’origine obstructive sont distinguées des apnées centrales selon que les événements respiratoires sont liés à une obstruction des voies aériennes supérieures, ou à un trouble de la commande respiratoire.
Syndrome d’apnées obstructives du sommeil (SAOS)
L’obstruction des voies aériennes supérieures (VAS) apparaît ou est majorée au cours du sommeil. Elle concerne les différents niveaux de la filière aérienne supérieure, des fosses nasales à l’hypopharynx. Les voies aériennes supérieures sont constituées de tissus mous, sous-tendus de muscles, en tension en période de veille et hypotoniques lors du sommeil.
Le diamètre des voies aériennes peut déjà être rétréci à l’état de veille en raison de l’hypertrophie de certains de ses éléments, par exemple un voile du palais allongé et épaissi, ou de l’inadéquation entre contenant et contenu, par exemple une macroglossie relative par rapport à une microrétrognathie. Au cours du sommeil, l’obstruction des voies aériennes est majorée en raison de l’hypotonie musculaire qui fait s’affaisser les parois pharyngées. Il semble de plus exister une neuropathie spécifique au cours des rhonchopathies, favorisant ce phénomène.
Ces obstacles sont, bien sûr, aggravés par la surcharge pondérale, l’inflammation des VAS (tabac), la consommation de produits majorant le relâchement musculaire au cours du sommeil (alcool, hypnotiques…).
L’obstruction des voies aériennes supérieures est une obstruction dynamique, per se variable dans le temps, au cours d’un même cycle respiratoire, d’un cycle à l’autre (en particulier en fonction du stade de sommeil), et d’une nuit à l’autre pour un même sujet.
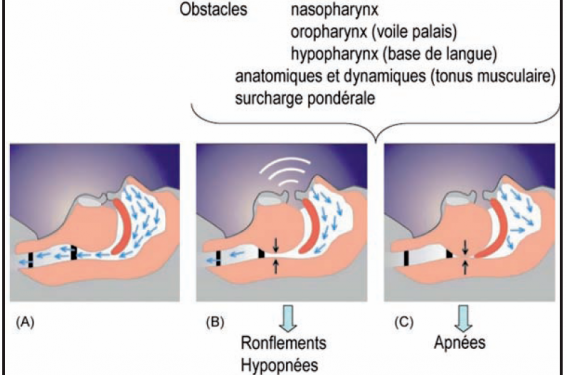
Elle s’accompagne de modifications des débits inspiratoires, se traduisant au minimum par une limitation de débit (forme particulière, en plateau, du débit inspiratoire) dont la conséquence audible est le ronflement, et selon l’importance de l’obstruction des VAS, par des hypopnées et/ou des apnées (figure 1). Les hypopnées et les apnées (figure 2A) sont plus ou moins désaturantes (figure 2B), en fonction de leur durée, des modifications des rapports ventilation/perfusion induites par le décubitus, et de la saturation d’éveil du sujet.
Figure 1. Représentation schématique des voies aériennes supérieures au cours du sommeil, chez un sujet en décubitus dorsal. Les flèches noires indiquent la circulation de l’air dans les VAS, (A) en situation normale (pas d’obstruction), (B) lorsqu’existe une obstruction partielle, se traduisant au minimum par des ronflements, des débits limitants, voire une hypopnée, (C) ou en cas d’obstruction complète provoquant une apnée.
L’obstruction des voies aériennes supérieures nécessite pour être levée, une augmentation de l’effort inspiratoire, dont témoigne l’augmentation de l’activité électromyographique du diaphragme et des muscles inspiratoires, avec pour conséquence l’augmentation (en valeur absolue) des pressions intrathoraciques, mesurées par la pression œsophagienne (figure 2C). La levée de l’obstacle et la reprise de la ventilation (figure 2D) s’accompagne en règle d’un éveil, qui peut revêtir différentes graduations, de l’éveil autonomique (augmentation de l’activité sympathique) se traduisant par une accélération du pouls (figure 2E) et une montée de la pression artérielle, à l’éveil électroencéphalographique (allègement en ondes lentes ou décharges brutales et transitoires d’activité alpha, (figure 2F) jusqu’à l’éveil comportemental au maximum (figure 2).
Figure 2. Enregistrement polysomnographique au cours d’apnées du sommeil. Sont présentés de haut en bas l’électroencéphalogramme, la saturation en oxygène de l’hémoglobine mesurée par voie transcutanée (SpO2), le flux nasal, le pouls, la pression œsophagienne représentative de la pression intrathoracique. Se reporter au texte pour les explications. La barre noire représente 10 s.
Syndrome d’apnées centrales du sommeil (SACS) et respiration de Cheyne-Stokes (CS)
Les syndromes d’apnées centrales constituent un groupe hétérogène de troubles respiratoires du sommeil secondaires à un arrêt ou une diminution transitoire de la commande des muscles respiratoires.
Ces syndromes sont donc distincts des troubles obstructifs au cours desquels les efforts respiratoires se poursuivent ou même augmentent pendant l’apnée.
Classiquement moins fréquents que le syndrome d’apnées obstructives du sommeil, leurs causes sont très diverses. Une étiologie prédomine par sa fréquence : la respiration périodique de Cheyne-Stokes (figure 3), présente chez environ 30% des patients insuffisants cardiaques. Cette ventilation est dite périodique car elle se caractérise par la diminution progressive decrescendo de la respiration puis sa reprise progressive, crescendo, jusqu’à quelques cycles d’hyperventilation, suivie d’une nouvelle diminution progressive, donnant à la respiration un aspect en fuseaux typique. La présence d’un CS est un facteur pronostique déterminant de l’insuffisance cardiaque. Chez un même patient, les deux types de trouble respiratoire peuvent être observés en proportions variables et c’est le mécanisme prédominant qui permet de classer le type de syndrome d’apnées du sommeil, central ou obstructif.
Figure 3. Exemple de syndrome d’apnées centrales du sommeil avec ventilation périodique de Cheyne-Stokes. De haut en bas sont notés les stades de sommeil (stade 3), la saturation en oxygène de l’hémoglobine mesurée par voie transcutanée (SpO2), le flux nasal, le flux buccal, les mouvements thoraciques et abdominaux. L’aspect typique crescendo - decrescendo de la ventilation est clairement visible sur les flux nasal et buccal ; le caractère central est établi sur la simultanéité des modifications du flux et de la commande ventilatoire que représentent les mouvements thoraco-abdominaux.
Comment diagnostiquer un syndrome d’apnées du sommeil ?
Les signes cliniques évocateurs de SAS obstructifs ne sont pas spécifiques, même si les notions d’obésité, de pauses respiratoires nocturnes constatées par les proches, de ronflements nocturnes, de somnolence diurne, de sensation de sommeil non réparateur avec fatigue sont évocatrices. La symptomatologie est encore plus pauvre en ce qui concerne les SAS centraux, car les patients sont peu, voire non somnolents. Ils décrivent parfois leur ventilation périodique, qui gêne l’endormissement, et est quelquefois remarquée aussi à l’éveil. Cette ventilation périodique est alors ressentie comme une dyspnée, et il faut savoir évoquer le diagnostic devant une telle plainte.
Dans la mesure où la clinique est non spécifique, le diagnostic repose clairement sur les examens complémentaires. L’examen de dépistage le plus simple est la mesure transcutanée de la saturation nocturne de l’hémoglobine en oxygène ou oxymétrie nocturne qui permet de détecter les épisodes de désaturation durant le sommeil (figure 4A). En raison de sa facilité de mise en œuvre et de sa sensibilité, cet examen est un outil précieux pour le dépistage mais reste insuffisant pour identifier précisément le mécanisme du SAS et en apprécier la sévérité.
Si l’examen s’avère positif (plus de 5 épisodes d’apnées-hypopnées par heure), il sera complété par une polysomnographie (figure 4B) réalisée en laboratoire du sommeil. Il s’agit de la méthode de référence au cours de laquelle sont enregistrés simultanément les variables permettant de définir :
– le sommeil électroencéphalogramme, électrooculogramme, électromyogramme mentonnier ;
– la respiration (flux naso-bucal) ;
– les mouvements thoraciques et abdominaux ;
– l’oxymétrie ;
– l’électrocardiogramme ;
– la position corporelle et les mouvements des jambes (électromyogramme jambiers).
Un examen plus simple est la polygraphie nocturne qui n’enregistre que les paramètres ventilatoires et est possible au domicile du patient.
Figure 4. Méthode de dépistage des SAS par oxymétrie (A) et de diagnostic par polysomnographie (B). L’oxymétrie nocturne permet de suivre la saturation en oxygène de l’hémoglobine mesurée par voie transcutanée (SpO2) tout au long du sommeil (A). En cas de SAS, on remarque, comme sur cet exemple, des désaturations nocturnes. La polysomnographie (B) permet l’enregistrement simultané du sommeil, d’une part, au moyen de l’EEG, des mouvements oculaires (électro-occulogramme) et de l’EMG mentonnier et, d’autre part, de paramètres respiratoires incluant le flux naso-buccal, les mouvements thoraciques et abdominaux.
Polysomnographie et polygraphie permettent de déterminer le type (apnées du sommeil obstructives ou centrales) et la sévérité du SAS, en calculant l’index d’apnées – hypopnées, IAH.
Pour un IAH < 10/h de sommeil, l’on considérera qu’il n’y a pas de SAS, un IAH entre 10 et 20/h définira un SAS modeste, un IAH entre 20 et 30/h, un SAS modéré et > 30/h, un SAS sévère.
Les syndromes d’apnées obstructives du sommeil (SAOS)
Épidémiologie
La prévalence du SAOS augmente nettement avec l’âge et ce, surtout après 50 ans. Dès les premières études, il est apparu une nette prédominance masculine. Le rôle des hormones sexuelles est confirmé par l’augmentation de la prévalence des troubles respiratoires nocturnes chez la femme après la ménopause. Le rôle de l’obésité (cf plus haut), essentiellement l’obésité tronculaire (ou androïde), est confirmé par la diminution de l’IAH après une perte de poids. La prévalence du syndrome d’apnées obstructives du sommeil initialement rapportée était de 2 % chez les femmes entre 35 et 60 ans et 4 % chez les hommes du même âge, les études les plus récentes suggèrent une prévalence plus élevée, de l’ordre de 5 à 10 %.
La prévalence augmente franchement dans le cas de pathologie associée : entre 30 et 60 % des sujets porteurs d’une pathologie cardio- et cérébrovasculaire, quelle qu’elle soit, ont un syndrome d’apnées du sommeil, et jusqu’à 80 % dans certains sous-groupes comme celui de l’HTA instable (figure 5).
La recherche d’un SAS devant une HTA sévère ou instable apparaît d’ailleurs dans les recommandations de la HAS.
Figure 5. Prévalence des SAS dans différentes pathologies cardiovasculaires, et dans la population générale. En abscisse est représentée la prévalence du SAS, exprimée en %.
Morbidité et mortalité du syndrome d’apnées du sommeil
Somnolence diurne excessive
La présence d’une somnolence diurne excessive est un maître symptôme du syndrome d’apnées obstructives du sommeil. Sa prévalence chez les patients présentant un IAH > 5/h est estimée entre 20 et 30 %. Elle augmente avec la valeur de l’index, avec toutefois une corrélation lâche, soulignant que la somnolence n’est pas uniquement secondaire à la fragmentation du sommeil induite par les apnées. Elle est importante à reconnaître car ses conséquences sont majeures : toutes causes confondues de somnolence, elle est à l’origine de 30 % des accidents mortels de la voie publique, et augmente le risque d’accidents du travail. Le risque d’accidents de la voie publique est important en cas de SAS : 24 % des SAOS dans une étude rapportaient s’être endormis au moins une fois au volant, et le risque d’accidents chez des patients dont l’IAH était > 15/h était multiplié par 7 à 8 dans d’autres études. Actuellement, la législation sur la sécurité routière stipule que la somnolence représente un cas d’inaptitude à la conduite automobile (arrêté du Journal Officiel du 28 décembre 2005).
En plus du risque accidentel qu’elle fait courir, la somnolence diurne excessive retentit fortement sur la qualité de vie des patients, en altérant leur vie sociale et professionnelle.
Conséquences cardiovasculaires
Depuis trente ans, l’hypothèse d’un lien entre syndrome d’apnées obstructives du sommeil et pathologies cardiovasculaires est soulevée, mais la preuve de la causalité n’a été apportée que plus récemment, grâce à des études épidémiologiques de grande envergure comme la Wisconsin Sleep Cohort Study portant sur le risque d’apparition d’une HTA. Celle-ci a démontré un risque significatif d’apparition d’HTA dès un IAH > 5/h. Le syndrome d’apnées obstructives du sommeil constitue également un facteur de risque de survenue d’accidents vasculaires cérébraux, dont la particularité est de survenir volontiers en fin de nuit ou au petit matin. Le SAS constitue aussi une cause indépendante d’athérome ; des travaux menés chez l’homme et dans des modèles expérimentaux l’ont clairement démontré. Concernant les autres pathologies cardiovasculaires, le syndrome d’apnées obstructives du sommeil semble prédisposer aux troubles du rythme et de la conduction nocturnes, au point que certains holters cardiaques proposent maintenant ces éléments pour le dépistage du syndrome d’apnées du sommeil.
Enfin, le syndrome d’apnées obstructives du sommeil a une influence pronostique délétère claire sur l’insuffisance cardiaque, et à l’inverse, traiter le syndrome d’apnées du sommeil permet une amélioration significative de la fonction cardiaque.
Retentissement métabolique
Le retentissement métabolique du syndrome d’apnées obstructives du sommeil est maintenant, lui aussi, clairement reconnu. Plusieurs études ont montré que le syndrome d’apnées obstructives du sommeil est un facteur de risque d’apparition de l’intolérance au glucose et de la résistance à l’insuline, premiers signes du diabète non insulinodépendant. Chez les patients déjà atteints, une corrélation positive significative existe entre des signes biologiques de déséquilibre du diabète et l’importance du syndrome d’apnées du sommeil. Inversement, le traitement du syndrome d’apnées du sommeil pourrait participer à un meilleur équilibre de la glycémie.
Autres conséquences
Le syndrome d’apnées du sommeil a de multiples autres conséquences qu’il serait fastidieux de lister ici. Citons toutefois l’altération des fonctions supérieures, mémoire, apprentissage, etc. et ce, indépendament de la somnolence diurne. Un point important, pas toujours soulevé spontanément par les patients, est le retentissement sur la libido. On note de nombreuses autres conséquences, comme l’induction d’une réponse inflammatoire ou les perturbations de la réponse immune.
Traitement
Le traitement des SAS obstructifs repose sur la ventilation nocturne en pression positive continue. En « pressurisant » les voies aériennes supérieures, elle offre une « attelle pneumatique » aux parois des voies aériennes supérieures et empêche leur collapsus inspiratoire. Ce traitement doit s’associer à des mesures hygiénodiététiques qui visent à réduire les facteurs favorisants (contrôle de la surcharge pondérale, arrêt du tabac, suppression des hypnotiques, suppression de la prise d’alcool dans les heures qui précèdent le coucher… ).
Des alternatives thérapeutiques existent sous forme de chirurgie ORL (uvulopharyngopalatoplastie conventionnelle, palatopastie par laser ou par radiofréquence), de chirurgie maxillo-faciale ou d’orthèse d’avancée mandibulaire à port nocturne. Ces dernières modalités peuvent être associées en cas d’obstacles multiples. Ces alternatives sont moins contraignantes que la ventilation ; toutefois, elles posent le problème d’un taux de succès de 50 à 60 % (à l’inverse de la ventilation), et du recours nécessaire, pour la chirurgie conventionnelle, à une anesthésie générale. La ventilation nocturne reste par conséquent largement le traitement de référence.
La ventilation nocturne est appliquée par voie nasale au moyen d’un masque ajusté sur la tête par un harnais. L’inspiration et l’expiration se font dans le même circuit (absence de valve), la ré-inhalation de CO2 expiré est évitée grâce à une fuite obligatoire présente sur les masques. L’adjonction d’un humidificateur sur le circuit d’air permet d’améliorer le confort. Plus d’une vingtaine d’appareils sont actuellement disponibles. Ces modèles diffèrent par leur taille, leur poids, leur confort sonore, l’existence ou non de logiciel d’observance, de circuit d’humidification incorporé, etc. La question essentielle posée par cette modalité thérapeutique est son observance. Les patients la trouvent volontiers contraignante et inconfortable, ce qui conduit, selon les séries, à environ 15 à 20 % d’arrêt de traitement. L’équipe soignante, en conjonction avec le prestataire de ventilation à domicile a donc, là, un rôle essentiel d’éducation et de suivi thérapeutique. L’étroite collaboration entre les différents spécialistes, par exemple cardiologues, pneumologues et spécialistes du sommeil s’avère indispensable pour accompagner le patient.
Ce qu’il faut en retenir
- Les études récentes montrent que la prévalence des syndromes d’apnées du sommeil chez les patients porteurs de pathologies cardiovasculaires est élevée, de 30 à plus de 80 %, comme c’est le cas par exemple en cas d’HTA instable.
- Les syndromes d’apnées du sommeil peuvent être de deux types : obstructifs ou centraux, ces deux mécanismes n’étant pas exclusifs. Leurs conséquences, notamment sur la morbi-mortalité cardiovasculaire et accidentelle ainsi que sur la qualité de vie des patients, justifient un diagnostic et un traitement adaptés.
- Ce dernier est représenté en première intention par la ventilation nocturne en pression positive continue, dont l’observance passe par une éducation thérapeutique renforcée et une étroite collaboration entre cardiologues et spécialistes du sommeil.
Les syndromes d’apnées centrales du sommeil (SACS)
Il est important d’aborder les syndromes d’apnées centrales du sommeil dans le contexte de l’insuffisance cardiaque chronique. Ils y sont fréquents et constituent un facteur aggravant. La prévalence des SAS serait de 51 à 61 % chez les patients porteurs d’une insuffisance cardiaque stable, dont environ un tiers de SASC avec respiration de Cheyne-Stokes. La présence d’un syndrome d’apnées du sommeil (SAS) a été décrite comme étant l’un des nombreux facteurs contribuant à l’altération de l’insuffisance cardiaque, au même titre par exemple que la dilatation auriculaire évaluée par la surface auriculaire en échocardiographie. Ainsi, dans la cohorte de 6 424 individus de la « Sleep Heart Health Study », la présence d’un SAS était associée à une majoration du risque d’insuffisance cardiaque (odds ratio = 2,38), indépendamment des autres facteurs de risque connus.
Physiopathologie des apnées centrales du sommeil avec respiration périodique de Cheyne-Stokes
Au sein des mécanismes responsables de l’apnée, l’hyperventilation semble paradoxalement jouer un rôle fondamental. Elle serait la conséquence de la stimulation des récepteurs intrapulmonaires sensibles à l’étirement, activés par la congestion pulmonaire, et des chémorécepteurs périphériques sensibles à l’hypoxie. L’hyperventilation entraîne une baisse de PaCO2 sous le seuil apnéique, et provoque une apnée qui entraîne une élévation secondaire de la PaCO2 au-dessus du seuil ventilatoire, ce qui permet la reprise de la respiration. L’oscillation du système est favorisée, d’une part, par l’allongement du temps de circulation qui transmet avec retard les modifications de la PaCO2 aux chémorécepteurs carotidiens, d’autre part, par une augmentation du gain de ces récepteurs. L’hypocapnie induite par l’hyperventilation est constatée aussi sur les gaz du sang diurnes ; sa constatation chez l’insuffisant cardiaque doit faire rechercher le SASC.
Traitement des syndromes d’apnées centrales du sommeil
La prise en charge du SAS avec respiration de Cheyne-Stokes suppose en premier lieu la prise en charge optimale de l’insuffisance cardiaque par les traitements ayant récemment démontré leur intérêt (diurétiques, inhibiteurs de l’enzyme de conversion, bêtabloquants). Dans le même ordre d’idée, la stimulation atriale forcée a été proposée chez des patients à fonction ventriculaire modérément altérée ayant une bradycardie sinusale symptomatique associée au SAS. L’efficacité sur le SAS n’est toutefois pas retrouvée chez les patients présentant un SASO et une FEVG peu altérée.
La ventilation nocturne est la même que pour les SAS obstructifs, et reposait jusqu’à présent sur la ventilation en pression positive continue, tout en requérant des précautions particulières compte tenu des effets délétères potentiels de la PPC sur la précharge. Certains autres modes de ventilation sont actuellement développés qui semblent plus indiqués dans ces indications, comme la ventilation à deux niveaux de pression, ou encore la ventilation servo-adaptée.
En pratique
La morbi-mortalité du syndrome d’apnées du sommeil (SAS) est pour l’essentiel liée aux conséquences de la somnolence diurne et aux conséquences cardiovasculaires. Si la reconnaissance des premières a rapidement fait l’objet d’un consensus, les conséquences cardiovasculaires du SAS ont été plus difficiles à établir, mais ne font aujourd’hui plus l’objet de controverse.
Dans la mesure où les pathologies cardio- et cérébrovasculaires représentent des pathologies chroniques avec handicap et risque vital parmi les plus fréquentes dans les pays industrialisés, et que leur traitement repose pour beaucoup sur le contrôle des facteurs de risque, les données acquises ces dernières années, tant concernant les conséquences physiopathologiques cardiovasculaires du SAS que la démonstration du lien causal entre SAS et pathologies cardiovasculaires, montrent que la prise en compte du SAS entre dans cet objectif et justifie un large dépistage.
* Données tirées des corrélations établies par les fournisseurs.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :









