Publié le 24 nov 2015Lecture 7 min
Les traitements actuels du SAOS : indications, modalités pratiques, acceptation
F. GAGNADOUX, Département de pneumologie, CHU d'Angers
Le syndrome d’apnées obstructives du sommeil (SAOS) est caractérisé par une fermeture répétée des voies aériennes supérieures au cours du sommeil, complète (apnée) ou incomplète (hypopnée), dont la survenue est sous-tendue par des anomalies anatomiques (réduction de calibre) et fonctionnelles (collapsibilité augmentée) du pharynx.
La définition du SAOS associe des symptômes nocturnes (ronflement, apnées décrites par l’entourage), diurnes, dominés par la somnolence diurne excessive, et la survenue d’au moins 5 apnées et/ou hypopnées obstructives par heure de sommeil lors d’une polysomnographie(1). La prise en charge thérapeutique du SAOS associe des traitements spécifiques instrumentaux visant à éviter le collapsus inspiratoire du pharynx durant le sommeil et des mesures générales tendant à réduire les facteurs favorisants du SAOS et les facteurs de risque cardiovasculaire (CV) auxquels il est fréquemment associé. Les objectifs thérapeutiques sont la suppression des troubles respiratoires au cours du sommeil et de leurs conséquences immédiates (hypoxie, fragmentation de sommeil), l’amélioration des symptômes diurnes et la prévention des complications associées au SAOS.
La pression positive continue nasale (PPC), traitement de référence du SAOS
Principe du traitement
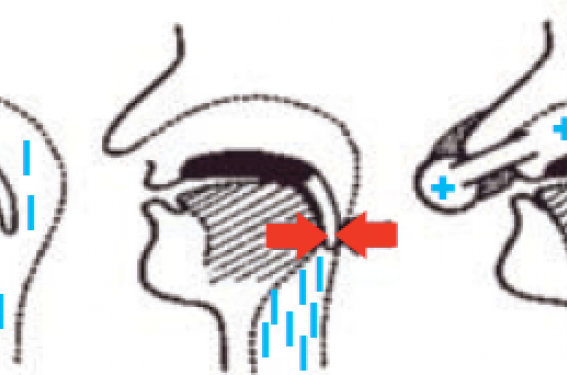
Grâce à un effet d’attelle pneumatique, l’application d’une PPC dans les voies aériennes supérieures au cours du sommeil via un masque nasal ou naso-buccal permet d’éviter le collapsus inspiratoire du pharynx, responsable des apnées et hypopnées obstructives(2) (figure 1).
Les méta-analyses d’études randomisées contrôlées ont démontré une amélioration de la vigilance diurne, de la qualité de vie et une diminution de la pression artérielle (PA) après quelques semaines de traitement quotidien par PPC(3). Le suivi de cohortes cliniques est en faveur d’une réduction de la morbi-mortalité cardiovasculaire et du risque d’accident automobile sous traitement régulier par PPC.
Le bénéfice thérapeutique de la PPC sur les symptômes et complications du SAOS est étroitement lié au nombre d’heures quotidiennes d’utilisation au cours du sommeil, qui peut être contrôlé régulièrement grâce aux données enregistrées par l’appareil.
Figure 1. Effet d’attelle pneumatique de la PPC s’opposant au collapsus pharyngé (d’après(2)).
Indications, mise en œuvre et prise en charge
Le traitement par PPC est indiqué en première intention chez les patients porteurs d’un SAOS sévère diagnostiqué par un enregistrement polygraphique au cours du sommeil avec un index d’apnées/hypopnées (IAH) au moins égal à 30 événements par heure(1). Chez les patients ayant un IAH entre 5 et 30, la PPC peut être proposée en cas de somnolence diurne importante sans autre étiologie ou lorsque le patient présente un risque cardiovasculaire élevé.
La mise en œuvre et le suivi du traitement par PPC font intervenir des prestataires de santé à domicile organisés autour d’un réseau associatif (issu de l’ANTADIR) ou commercial (depuis les années 1990).
Les prestations assurées au domicile des patients, telles que définies par le forfait 9 de la liste des produits et prestations remboursables, comportent la mise à disposition et la maintenance du matériel, la gestion du dossier administratif et une contribution au suivi et à l’éducation thérapeutique. Cette prestation fait l’objet d’une demande d’entente préalable et bénéficie d’une prise en charge à hauteur de 60% par les caisses d’assurance maladie. Son renouvellement annuel est conditionné à l’efficacité clinique et à une observance journalière moyenne d’au moins 3 heures lors des visites de suivi, qui sont rapprochées au cours des 6 premiers mois, puis au minimum annuelles.
Principaux effets secondaires et acceptation de la PPC
La PPC n’expose à aucun effet secondaire grave, mais à des effets secondaires locaux (tableau 1) qui concernent au moins 50% des patients et sont susceptibles de diminuer l’observance journalière, voire de décourager le patient de poursuivre le traitement(4). Ils surviennent habituellement dès les premières semaines et doivent être rapidement corrigés. Les blessures cutanées, en particulier au niveau de l’arête du nez, sont dues le plus souvent à un masque mal adapté et/ou trop serré. Il existe actuellement une très large gamme de masques permettant d’éviter ce type d’effet secondaire.
Les phénomènes d’intolérance nasale à la PPC (sécheresse naso-buccale, obstruction nasale, rhinorrhée) sont fréquents, en particulier chez les patients âgés, aux antécédents ORL, ou recevant un traitement susceptible d’assécher les voies aériennes (antihypertenseurs, psychotropes…).
L’adjonction d’une humidification chauffante sur l’appareil de PPC améliore les symptômes locaux et augmente l’observance thérapeutique. Chez les patients ayant des difficultés à tolérer la pression à l’expiration ou des phénomènes d’aérophagie, en particulier lorsque la pression efficace est élevée, l’utilisation d’une pression variable peut être bénéfique.
Une insomnie peut être associée au SAOS et peut être aggravée en début de traitement par PPC. Le recours ponctuel à certains hypnotiques peu dépresseurs respiratoires (type zolpidem ou zopiclone) peut favoriser l’endormissement sous PPC en début de traitement. Une prise en charge spécialisée est souhaitable en cas d’insomnie persistante sous PPC.
Si les refus initiaux sont rares (< 4%), une étude récente portant sur une large cohorte multicentrique a estimé à environ 37% le risque d’abandon ultérieur ou d’observance insuffisante (< 4h/nuit) de la PPC(5). Le risque d’abandon prédomine dans les 6 premiers mois de traitement. Il est plus élevé chez les patients porteurs de SAOS léger à modéré (IAH < 30), chez les sujets en activité et/ou vivant seuls.
Le suivi régulier et l’éducation thérapeutique du patient permettent de réduire le risque d’abandon et d’augmenter le nombre d’heures quotidiennes d’utilisation de la PPC.
L’orthèse d’avancée mandibulaire (OAM), une alternative thérapeutique à la PPC
Principe du traitement
Un dispositif endobuccal moulé sur les arcades dentaires supérieures et inférieures permet d’avancer le maxillaire inférieur durant le sommeil. En propulsant le massif lingual, l’OAM s’oppose au collapsus inspiratoire du pharynx(6) (figure 2). Des biellettes de taille variable permettent de régler le niveau d’avancée (figure 3).
L’impact de l’OAM sur les troubles respiratoires au cours du sommeil est en moyenne inférieur à celui observé sous PPC. L’absence d’obésité et le caractère léger ou modéré des troubles respiratoires nocturnes augmentent les chances d’efficacité complète.
A cours terme, l’OAM bénéficie d’une meilleure observance que la PPC et d’une efficacité comparable sur les symptômes diurnes de la maladie(7). A l’heure actuelle, nous manquons de données sur l’efficacité et l’observance à long terme, et l’impact de l’OAM sur la morbidité associée au SAOS reste à démontrer.
Figure 2. Principe d’action de l’orthèse d’avancée mandibulaire (d’après(6)).
Figure 3. Exemple d'orthèse d'avancée mandibulaire avec biellettes de taille variable permettant de régler l'avancée mandibulaire.
Indications, mise en œuvre et prise en charge
Les sociétés savantes recommandent l’utilisation de l’OAM dans les formes légères à modérées de SAOS ou en seconde intention dans le SAOS sévère, en cas d’échec ou d’intolérance à la PPC(1). Seule cette dernière indication bénéficie actuellement d’un remboursement par l’Assurance Maladie à hauteur de 60%.
La mise en œuvre et le suivi du traitement par OAM impliquent une étroite collaboration entre le médecin spécialiste du sommeil et un praticien dentaire formé. Un bilan préalable doit éliminer les contre-indications dentaires et maxillo-faciales. Une phase d’adaptation de quelques semaines permet de déterminer l’avancée mandibulaire réalisant le meilleur compromis entre la tolérance et l’efficacité thérapeutique qui doit être vérifiée par un enregistrement nocturne.
Principaux effets secondaires et acceptation de l’OAM
Les effets secondaires rapportés en début de traitement par OAM sont habituellement d’intensité modeste et disparaissent au bout de quelques semaines de port régulier de l’appareil. Ils sont dominés par la sécheresse buccale ou l’hypersalivation. Les douleurs dentaires, temporo-mandibulaires et gênes à la mastication, prédominent le matin au retrait de l’appareil et s’estompent lors des premiers efforts de mastication. A long terme, le traitement par OAM est associé à des modifications mesurables de l’articulée dentaire dont l’amplitude dépend de l’occlusion initiale, du degré d’avancée mandibulaire et de la régularité d’utilisation de l’appareil. Bien qu’ayant peu de retentissement clinique, les conséquences potentielles de l’OAM sur l’occlusion justifient une surveillance dentaire semestrielle(1) par un praticien formé.
L’observance thérapeutique déclarée par le patient est plus élevée sous OAM que sous PPC, ce qui pourrait expliquer une amélioration comparable des symptômes malgré une moindre correction des troubles respiratoires nocturnes. Des microcapteurs intégrés permettront prochainement de mesurer objectivement l’observance thérapeutique de l’OAM, comme cela est fait pour la PPC.
Des mesures générales indispensables
Dans plus de 50% des cas, le SAOS est associé à un syndrome métabolique (SM) dont les différents paramètres doivent être pris en charge de façon optimale pour réduire le risque cardiovasculaire. En cas d’obésité associée au SAOS, une perte de poids significative (10-12 kg) et durable s’accompagne d’une réduction des troubles respiratoires au cours du sommeil et d’une amélioration des différents paramètres du SM(8). La prise en charge d’une HTA associée au SAOS ne peut se limiter à la PPC et doit comporter un traitement pharmacologique.
Lorsque le SAOS est associé à une insuffisance veineuse, le port de bas de contention pourrait améliorer les troubles respiratoires en réduisant les mouvements de fluides vers la partie supérieure du corps au cours de la nuit.
La consommation d’alcool avant le coucher et la prise de médicaments dépresseurs respiratoires (anxiolytique, myorelaxant, morphinique) peuvent majorer les troubles respiratoires nocturnes et doivent donc être évités. En cas de SAOS « positionnel », certains dispositifs peuvent éduquer le patient à éviter le sommeil en décubitus dorsal.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :