Publié le 15 déc 2016Lecture 8 min
Quelques nouveautés dans la thrombose
É. FERRARI, CHU de Nice
CNCF
L’embolie pulmonaire
« Même quand on y pense toujours, on n’y pense pas encore assez », dit l’adage.
Le beau travail de l’équipe de Prandoni dans le NEJM vient confirmer cette règle(1).
En bref : chaque fois qu’un patient est hospitalisé pour syncope inexpliquée, si vous recherchez une embolie pulmonaire, vous la retrouverez dans 1 cas sur 6 et si vous ne prenez en compte que les patients qui ont une probabilité acceptable d’EP vous trouverez une EP dans 42 % des cas !
L’étude a été faite dans 11 centres italiens. Chez 560 patients (76 ans de moyenne d’âge) hospitalisés pour syncope sans cause évidente, on élimine ceux avec une faible probabilité d’EP et des D-dimères négatifs. Restent 230 patients chez lesquels, lorsqu’on pratique un scanner spiralé, une EP va être retrouvée dans 42,2 % des cas !
Sans exclure les patients à faible probabilité prétest, l’incidence d’EP est tout de même de 17,3 %. Si on distingue ceux qui avaient un diagnostic alternatif de ceux qui n’en avaient pas la probabilité d’une EP passe de 12,7 % à 25,4 %.
De quelle EP s’agit-il ? Dans 42 % des cas, la localisation la plus proximale du thrombus est dans une des 2 AP proximales. Dans 25 % des cas, dans une lobaire. Dans 26 % des cas, il s’agissait d’une EP segmentaire et dans les 7 % des cas restants, une EP sous-segmentaire.
Il ne s’agit pas de faire un scanner spiralé systématique à toutes les syncopes mais lorsque l’approche clinique ne permet pas d’éliminer une syncope vaso-vagale, une hypotension iatrogène ou une déshydratation… alors il faut évoquer l’EP, calculer la probabilité prétest, et doser les D-dimères pour éviter de faire des scanners inutiles mais pour les patients restants la probabilité d’une EP devient, d’après ce travail, très importante.
Remarques
Cela repose tout le problème d’une maladie pour laquelle les signes typiques que nous enseignons à la faculté (dyspnée, point de côté basi-thoracique, hémoptysie…) sont finalement très rares.
Habituellement, les D-dimères augmentent après une syncope du fait des hématomes, même infracliniques. Dans ce contexte, ils risquent d’être moins contributifs pour éliminer une EP.
L’histoire ne dit pas si un Doppler veineux aurait pu nous affranchir de quelques scanners inutiles, mais le résultat essentiel est là :
1 patient sur 6 hospitalisés pour une syncope a une EP et c’est près de 1 patient sur 2 (42 %) si on ne prend en compte que les patients qui n’ont pas une probabilité pré-test faible !
Anti-inflammatoires et patient cardiaque ou à risque
Des règles de bonne utilisation ont été édictées sur la prescription des anti-inflammatoires chez le coronarien comme chez le patient à haut risque cardiovasculaire : en bref, il faut les éviter autant que faire se peut, leur préférer les antalgiques, voire les corticoïdes en première intention. Lorsqu’un anti-inflammatoire est donné, il ne faut prescrire que la plus petite dose efficace pendant la plus courte durée possible. On rajoute même dans ces recommandations que lorsqu’on doit prescrire des AINS chez des sujets à risque (mais non coronariens avérés) il faut introduire de l’aspirine en sus de pratiquer une surveillance de la tension artérielle.
Par ailleurs, tout le monde se rappelle du retrait de certains anti-Cox2 du fait de leur toxicité cardiovasculaire. Enfin de nombreuses études cas-témoins semblaient faire ressortir le fait que le naproxène était probablement l’AINS le moins délétère.
Ces données étant rappelées, restaient deux questions :
- les anti-Cox2 à faible dose sont-ils plus toxiques que les AINS ?
- le naproxène se démarque-t-il vraiment de l’ibuprofène ?
L’étude PRECISION(2) a apporté une réponse à ces deux questions. Elle a comparé trois traitements anti-inflammatoires chez des arthrosiques ou des rhumatisants : le naproxène, L’ibuprofène et un anti-Cox2 à faible dose (le celecoxib 200 mg/j). L’étude était randomisée et a inclus plus de 24 000 patients. La durée moyenne du traitement était de 20 mois et le suivi moyen de plus de 34 mois. Tous les patients étaient sous IPP.
Les résultats sont très intéressants :
L’anti-Cox2 à faible dose n’est pas plus à risque que les deux autres AINS, en revanche il donne moins de toxicité gastrique et moins de toxicité rénale.
Le naproxène n’est pas vraiment moins à risque que l’ibuprofène même si une tendance semble se dessiner pour une moindre toxicité.
Notons que sur le suivi de 34 mois un événement cardiovasculaire survient chez moins de 2 % des patients sous AINS.
Au total, si on doit utiliser un AINS, autant prescrire un anti-Cox2 à faible dose qui, s’il ne sera pas moins délétère que les autres AINS, sera mieux supporté.
Le ticagrelor est-il plus efficace que le clopidogrel chez l’artéritique des membres inférieurs ?
C’est la question a laquelle a essayé de répondre la grande étude EUCLID.
Plus de 13 000 patients artéritiques symptomatiques ou avec un IPS < 0,8 ont été randomisés clopidogrel 75 mg/j ou ticagrelor 90 mg x 2 par jour.
À noter qu’une enquête génétique à la recherche des résistances au clopidogrel était systématiquement faite. Le suivi moyen était de 30 mois.
Les résultats montrent que, dans cette population à haut risque s’il en est, le ticagrelor n’est pas plus efficace que le clopidogrel. Il faut noter qu’un événement cardiovasculaire est survenu chez environ 10 % des patients avec une incidence annuelle de 4,4 %. Qu’il n’y a pas eu de différence en termes de tolérance hémorragique entre les 2 régimes d’antiplaquettaire. La note positive que l’on peut trouver à cette étude est qu’en termes d’AVC, chez les patients artéritiques, le ticagrelor semble faire mieux que le clopidogrel avec une incidence d’AVC de 1,9 % vs 2,4 %. Si la faible incidence des AVC ne peut pas permettre de conclure que le ticagrelor protège mieux des AVC, ce type de résultat était déjà présent dans PEGASUS et peut donner à réfléchir. Notons qu’en termes de tolérance, 4,8 % des patients se sont plaints d’une dyspnée sous ticagrelor vs 0,8 % sous clopidogrel (cette incidence de dyspnée était beaucoup plus importante dans PEGASUS).
Après l’apport des nouveaux antiplaquettaires, dont le ticagrelor, après un SCA, il est décevant de constater qu’on ne peut être plus efficace dans la prévention des événements cardiovasculaires graves dans cette population à risque.
On en vient à penser que l’évolution de l’athérosclérose n’est peut-être pas la même que celle de nos patients qui rentrent dans la maladie athéroscléreuse par un événement coronarien.
PIONEER
Enfin, une grande étude pour progresser sur notre conduite à tenir chez nos patients coronariens en arythmie complète qui doivent être stentés.
Jusque-là, des recommandations existaient mais ne reposaient pas sur grand-chose. Il y a peu, la pensée était de maintenir une trithérapie avec 2 AAP et 1 AVK et d’éviter les stents actifs… puis l’étude WOEST, qui était une étude de sécurité, nous a montré que nous n’avions peut-être pas besoin de maintenir 2 AAP en sus de l’AVK, enfin des recommandations (avis d’experts sans aucune donnée solide) proposaient d’utiliser un AOD à la plus petite dose possible pour la FA avec un régime AAP raccourci. Mais d’études majeures… point du tout.
L’étude PIONEER, la première parmi d’autres études en cours et à venir sur cette thématique, fait avancer les choses. Elle a comparé 3 stratégies antithrombotiques chez 2 124 patients devant être stentés et ayant par ailleurs besoin d’un anticoagulant oral pour une FA non valvulaire :
- rivaroxaban 15 mg + clopidogrel 75 pendant 12 mois ;
- rivaroxaban 2,5 mg x 2 + une bithérapie (essentiellement clopidogrel) pour 1, 6 ou 12 mois ;
- AVK + bithérapie pour 1, 6 ou 12 mois.
Comme pour l’étude WOEST, il s’agissait d’une étude de sécurité où l’objectif était de démontré un bénéfice en termes de risque hémorragique.
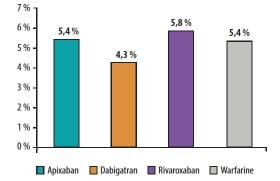
Les résultats sur cet end point primaire montrent une très nette diminution du risque hémorragique avec les 2 stratégies « rivaroxaban » sans que l’une apparaisse supérieure à l’autre : 16,8 % et 18 % versus 26,7 % dans le bras AVK : soit une réduction du risque hémorragique de plus de 40 %.
L’étude ne visait pas à établir si une des 3 stratégies était meilleure en termes d’événements thrombotiques, mais les données sur ce plan (end point secondaire) sont rassurantes puisqu’il n’y a pas de différences d’événements CV.
Quelques remarques
D’abord sur les doses choisies de rivaroxaban : on peut dire que le 15 mg de rivaroxaban correspond à la plus petite dose validée dans la FA non valvulaire alors que le 2,5 mg x 2 correspond à l’étude TIMI-Atlas 51 dans laquelle, à cette dose particulière le rivaroxaban a montré un bénéfice substantiel en post-SCA (sans FA) en sus de la bithérapie aspirine clopidogrel, ce qui lui a valu en Europe une obtention d’AMM en post-SCA. Sauf qu’à ce jour la dose de 2,5 mg n’est pas disponible en France.
Sur les patients inclus : il s’agissait plus souvent d’angioplasties électives que de SCA. Les FA étaient non valvulaires avec un CHADS moyen a plus de 3. Dans le bras AVK, l’INR a été dans la cible dans plus de 60 % du temps. Il n’est pas dit si les patients sous AVK l’étaient déjà auparavant ou s’il s’agissait de patients mis sous AVK pour l’étude, ce qui peut avoir contribué à un sur-risque hémorragique. La fonction rénale devait autoriser la mise sous AOD. Enfin 65 % des stents étaient pharmacologiquement actifs. Il sera difficile d’extrapoler ce protocole à tous nos patients stentés en FA : mais les 2 stratégies nous laissent un choix. Peut-être privilégier la dose modérée de rivaroxaban avec un seul antiplaquettaire lorsque la gravité porte sur la FA ou garder deux antiplaquettaires avec une petite dose de rivaroxaban lorsque le contexte doit faire privilégier la coronaire. Tout le monde devrait y trouver son compte.
Ces résultats sont très utiles. Ils nous permettent d’envisager une stratégie antithrombotique moins risquée mais également plus simple d’utilisation, en particulier si on utilise le 15 mg de rivaroxaban en 1 prise par jour et 1 seul antiplaquettaire.
D’autres études sont en cours avec les autres AOD qui devraient venir confirmer cette tendance. On pourrait penser qu’il est dommage de ne pas disposer du même type d’étude dont l’objectif primaire aurait été l’efficacité sur les événements thrombotiques. Sauf que dans cette population particulière qui représentent entre 5 et 10 % de nos patients coronariens, le problème majeur est bien celui du risque hémorragique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :