Vasculaire
Publié le 18 avr 2006Lecture 9 min
CAT devant une claudication intermittente des membres inférieurs
S. KOWNATOR, cabinet de cardiologie, Thionville
La claudication intermittente (CI) permet souvent de découvrir une artériopathie oblitérante des membres inférieurs (AOMI) ou est, en tout cas, le premier motif de consultation d’un sujet porteur de cette pathologie.
Pour autant, il faut se souvenir que pour un patient présentant une AOMI symptomatique, un à trois sujets présenteraient une forme dite asymptomatique.
Avant d’envisager le traitement du patient porteur d’une CI, il faut bien évidemment affirmer le diagnostic dont l’interrogatoire et l’examen clinique sont les étapes indispensables.
Physiopathologie
La CI artérielle traduit l'inadéquation entre les besoins des muscles impliqués dans l'exercice et le débit artériel disponible pour ces muscles. Cette définition exprime bien l’ambiguïté qui prévaut à l’identification des formes dites asymptomatiques et le caractère flou de la frontière entre ces deux formes.
Pour se manifester, une CI doit impliquer un effort susceptible de déclencher l’ischémie d’effort responsable des symptômes. Ainsi, un sujet sédentaire pourra être totalement asymptomatique malgré des lésions qui pourraient être invalidantes chez un sujet actif.
La CI se traduit classiquement par une douleur du ou des mollets survenant pour une distance de marche constante à une allure donnée. La localisation de la douleur peut varier logiquement avec le siège des lésions artérielles dominantes. Les sténoses ou occlusions symptomatiques de l’iliaque commune se manifestent au niveau de la fesse, de la cuisse ou du mollet.
Celles de l’iliaque externe ou de la fémorale commune parlent au niveau de la cuisse ou du mollet. Les lésions de la fémorale superficielle ou de la poplitée s’expriment au niveau du mollet. Enfin, l’atteinte des artères jambières est responsable de douleurs du pied.
Certaines claudications sont trompeuses : claudication lombaire à type de lombalgie, claudication fessière pouvant évoquer une coxarthrose, claudication de cuisse se présentant comme une douleur du genou, claudication plantaire évoquant une atteinte du pied. Le déclenchement systématique et univoque à la marche et la sédation de la douleur au repos doivent attirer l’attention.
La clé de voûte est certainement la mesure du rapport de pression cheville/bras ou index de pression systolique (IPS). Un IPS < 0,9 permet d’affirmer l’AOMI.
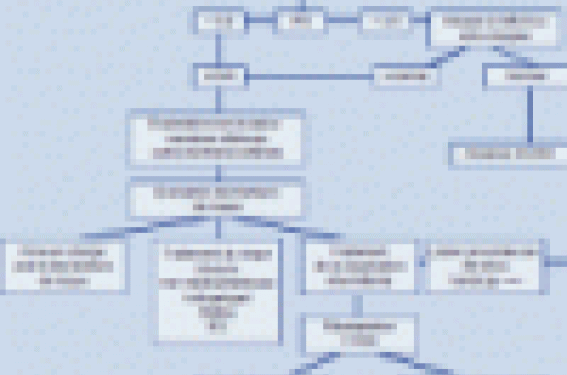
Chez un patient présentant une symptomatologie typique de CI dont l’IPS est > 0,9, la mesure doit être effectuée après un effort ; idéalement, on effectue une épreuve de marche standardisée sur tapis roulant, à défaut, il peut s’agir d’une marche dans le couloir ou d’une dizaine de flexions. En cas d’AOMI, les pressions à la cheville baisseront après l’effort, confirmant ainsi le diagnostic (figure 1).
Figure 1. Arbre décisionnel : conduite à tenir devant une claudication typique.
Explorations
Explorations des lésions responsables
Au stade de l’AOMI symptomatique, des explorations complémentaires peuvent être proposées afin d’identifier les lésions responsables et d’établir une cartographie lésionnelle.
- À ce stade, l’artériographie conventionnelle n’est pas justifiée en 2006, sauf exception. Cette technique, considérée comme méthode de référence par beaucoup, doit être réservée aux patients chez lesquels une décision d’intervention a été prise sur la base d’autres investigations. Les méthodes d’imagerie non invasives sont aujourd’hui les méthodes de choix.
- L’écho-Doppler, en raison de sa très large disponibilité, de son coût peu élevé, est certainement la méthode à préférer. Il faut cependant que l’examen soit complet, incluant l’exploration de l’axe artériel depuis l’aorte sous-diaphragmatique jusqu’aux extrémités. On pourra ainsi détecter et quantifier les lésions susceptibles de faire l’objet d’un geste de revascularisation. Une attention toute particulière doit être apportée à l’exploration des axes iliaques et à celle des bifurcations.
- L’angioscanner multibarrettes et l’angiographie par résonance magnétique (ARM) peuvent être proposés en cas de lésions complexes ou si l’écho-Doppler est incomplet ; chacun présente des avantages et des inconvénients. Ils peuvent être choisis en fonction des habitudes locales et de l’expérience des équipes.
Exploration des autres territoires artériels
- En plus de l’exploration artérielle des membres inférieurs, il faut considérer chez le patient claudicant, la recherche d’une atteinte dans les autres territoires artériels car :
• > 50 % des patients claudicants ont une maladie coronaire avérée,
• et 25 à 30 % d’entre eux présentent une atteinte significative des axes artériels à destinée cérébrale.
Atteinte coronaire. On recommande au moins un ECG de repos. Un ECG d’effort quand il est réalisable, ou une scintigraphie ou encore une échocardiographie de stress sont, dans les faits, souvent réalisés. La coronarographie systématique n’a pas d’indication ; des études sont encore nécessaires pour préciser à ce stade l’utilité d’un scanner coronaire.
Atteinte carotidienne. Un écho-Doppler des troncs supra-aortiques peut être réalisé à la recherche de sténoses carotidiennes > 60 %. Enfin, il faut bien sûr éliminer un anévrisme de l’aorte abdominale, ce qui est fait systématiquement par les explorations non invasives.
L’AOMI étant évaluée, sa prise en charge répond à deux impératifs : le traitement du risque cardiovasculaire (CV) et l’amélioration fonctionnelle.
Traitement du risque CV : l’enjeu essentiel
Il s’agit de l’enjeu essentiel. Le pronostic du patient claudiquant est essentiellement conditionné par la survenue d’événements cardiovasculaires. Le pronostic local à ce stade de la maladie apparaît au deuxième plan (figure 2).
Figure 2. Pronostic à 5 ans pour 100 patients suivis pour une claudication intermittente.
Le patient claudicant doit être considéré comme un sujet à haut risque cardiovasculaire ; il s’agit d’un équivalent de prévention secondaire. De cette équivalence dépendent les mesures devant être mises en place. Pour autant, la sévérité de l’AOMI conditionne le pronostic cardiovasculaire. On sait, en effet, que le risque d’événement est étroitement lié au niveau d’IPS (figure 3). Ainsi un patient ayant un IPS à 0,85 n’aura pas le même niveau de risque qu’un sujet avec un IPS < 0,5.
Figure 3. Mortalité à 5 ans en fonction de la valeur d’IPS de base.
Cela étant, en attendant les recommandations de l’HAS, les recommandations américaines publiées récemment considèrent tous les patients ayant une CI comme des sujets à risque élevé. En termes de traitement, cela implique des mesures visant à modifier le style de vie ainsi qu’un traitement pharmacologique.
Mesures non médicamenteuses
Ces mesures viennent au premier plan avec, si possible, un programme d’éducation thérapeutique ciblé sur l’activité physique, les mesures diététiques et, si nécessaire, le sevrage tabagique.
Mesures médicamenteuses
Antiagrégants plaquettaires. Paradoxalement, très peu d’études ont été menées chez le patient présentant une AOMI. L’Antithrombotic Trialists’ Collaboration meta-analysis, clé de voûte de ces études, montre un bénéfice de l’aspirine dans la prévention des événements cardiovasculaires chez 135 000 pa-tients à haut risque ou en prévention secondaire. Parmi eux, 9 716 présentent une AOMI. Le traitement antiagrégant plaquettaire, surtout par aspirine, permet une réduction de 23 % du risque d’événement. La dose la plus efficace se situe entre 75 et 150 mg.
Dans l’ensemble de la population de l’étude CAPRIE (Clopidogrel vs Aspirin in Patients at Risk of Ischemic Events), le clopidogrel apporte un bénéfice supplémentaire de 8,7 % comparativement à l’aspirine. Il faut cependant préciser que, pour les patients présentant une AOMI à l’inclusion (6 452), ce bénéfice sur l’aspirine atteint 23,8 %.
Ainsi, même si les données de la littérature sont assez limitées, l’indication d’un antiagrégant plaquettaire apparaît indispensable avec, dans l’AOMI, un avantage du clopidogrel sur l’aspirine.
Statines. L’utilité des statines chez les patients à haut risque n’est plus à démontrer et leur utilisation s’impose chez ces patients, indépendamment du niveau de base du cholestérol avec comme cible un LDL-C < 1 g/l.
Parmi les essais à notre disposition, l’étude HPS (Heart Protection Study) surtout, menée avec la simvastatine 40 mg, montre un bénéfice chez les sujets porteurs d’une AOMI. Dans cette étude, 6 748 patients ayant une artérite des membres inférieurs, dont 4 042 coronariens, ont été inclus. Dans la population des artéritiques, comme dans l’ensemble de la population, le bénéfice obtenu est de l’ordre de 24 % tant sur la survenue du critère primaire (mortalité globale et cardiovasculaire) que sur la survenue d’événements.
- IEC. Une analyse de sous-groupe de l’études HOPE (Heart Outcomes Prevention Evaluation) a montré que le traitement par ramipril (10 mg/j) prévient significativement la survenue de complications cardiovasculaires graves chez des patients atteints d’AOMI sans distinction de stade évolutif (1 725 patients symptomatiques vs 7 349 asymptomatiques), qu’ils soient ou non hypertendus.
Ainsi, chez l’artéritique, sujet à haut risque cardiovasculaire, il paraît licite, au vu de la littérature, de préconiser de manière systématique un traitement comportant l’association antiagrégant, statine + IEC, même si à l’heure actuelle aucune étude n’a permis de tester l’efficacité de cette association.
Au-delà de cette attitude systématique, la prise en charge active des facteurs de risque s’impose. Un sevrage tabagique doit être obtenu. La valeur cible du LDL-C est de 1g/l. Le niveau tensionnel doit être <140/90 ou 130/80 mmHg chez le diabétique et l’insuffisant rénal. À cet égard, l’étude ASCOT (Anglo-Scandinavian Cardiac OuTcomes), publiée récemment, montre que l’association amlodipine + perindopril permet chez des sujets hypertendus de réduire de 33 % l’apparition ou l’aggravation d’une AOMI.
Enfin, le contrôle du diabète est bien évidemment fondamental. Dans UKPDS (United Kingdom Prospective Diabetes Study group), une diminution de 1 % du taux d’HbA1c était associée à une réduction de 43 % des amputations ou des décès dus à une pathologie vasculaire périphérique.
Traitement de la claudication intermittente
Ce traitement comporte lui aussi plusieurs versants : l’intervention non médicamenteuse, le traitement pharmacologique et le traitement interventionnel.
Intervention non médicamenteuse
On retrouve ici les mesures entreprises pour la prévention cardiovasculaire. L’exercice physique et la marche jouent un rôle tout particulier. Idéalement, un programme spécifique de réadaptation à la marche devrait être entrepris. Ce type de programme, comportant au moins 3 séances supervisées de 30 à 60 minutes par semaine pendant 3 mois, permet d’améliorer la distance de marche sans douleur de 150 % en moyenne. Bien sûr, pour une évaluation pertinente, la mesure de la distance de marche initiale devrait être quantifiée au préalable sur tapis roulant. Force est de constater que, dans la grande majorité des cas, ces programmes n’existent pas. L’efficacité des mesures non encadrées n’a pas, ou peu, été démontrée dans la littérature.
La crénothérapie est souvent évoquée. Son efficacité avec ou sans carbothérapie est très discutée mais peu s’avérer comme un complément utile.
Traitement pharmacologique
Les vasodilatateurs. Leur prescription est courante et ancienne. Plusieurs d’entre eux ont montré une efficacité sur la claudication dans des essais contrôlés randomisés de petite taille. Les recommandations américaines récentes mettent l’accent sur l’efficacité du cilostazol (non disponible en France) et, dans une moindre mesure, sur celui de la pentofyxilline (Torental®). Le naftidrofuryl (Praxilène®) et le buflomédyl (Fonzylane®) ont également montré des résultats mais force est de constater que l’amélioration obtenue avec ces molécules est de faible importance, ce qui a conduit à leur conférer un service médical rendu insuffisant (Afssaps 2004). À l’heure actuelle, au vu des résultats de la littérature, il n’y a pas d’indication pour les vasodilatateurs chez le patient claudicant.
Les statines. Plusieurs essais, en particulier avec la simvastatine et l’atorvastatine dans l’étude Treadmill, ont montré des résultats intéressants sur la claudication intermittente. Bien que limités, ces résultats associés à ceux obtenus pour la prévention du risque d’événements sont autant d’arguments pour renforcer l’indication d’une statine chez le patient claudicant.
Traitement interventionnel
Au stade de la CI, le traitement interventionnel en première intention ne se justifie pas, sauf circonstances particulières. De manière générale, il doit être discuté uniquement après échec à 3 mois d’un traitement médical bien conduit. Il peut être proposé plus précocement chez les patients particulièrement handicapés dans leur vie quotidienne et/ou chez ceux présentant des lésions serrées, menaçantes, sans possibilité de développement d’une collatéralité efficace.
Le choix entre traitement endovasculaire et chirurgie sera largement dépendant du type de lésion. Ainsi, pour les lésions proximales courtes, l’angioplastie sera largement préférée. Il faut retenir cependant que la revascularisation des lésions fémoro-poplitées n’a que très peu d’indications à ce stade.
En conclusion
L’apparition d’une CI conduit souvent à identifier le patient comme sujet à haut risque cardiovasculaire.
C’est la prise en charge de ce risque qui prévaut à ce stade, le risque local passant au second plan.
Cette attitude mérite des efforts d’explications et d’éducation du patient qui est principalement préoccupé par la gêne fonctionnelle.
Ainsi, le diagnostic d’AOMI doit être considéré comme une opportunité majeure de prévention. Cela justifie les efforts indispensables pour un dépistage plus précoce de cette affection souvent négligée.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :