Rythmologie et rythmo interventionnelle
Publié le 03 mai 2005Lecture 12 min
Quand proposer une ablation à un patient qui souffre de tachycardies de Bouveret ?
J.-F. LECLERCQ, CMC de Parly II, Le Chesnay, CMC de Vinci, Paris XIe
Le médecin lyonnais Bouveret a décrit en 1889 – avant l’électrocardiogramme – les tachycardies paroxystiques régulières à début et fin brusques sur cœur sain. En pratique clinique de rythmologie, les tachycardies responsables de la maladie de Bouveret s’appellent des rythmes réciproques paroxystiques. Elles peuvent correspondre à des rythmes réciproques intranodaux ou faire appel à une voie accessoire.
Les tachycardies réciproques nodales
Mécanisme
Responsables de la maladie de Bouveret dans 90 % des cas, elles sont liées à une anomalie de développement du nœud auriculo-ventriculaire. Du fait d’un développement trop important, en particulier de sa « corne » postéro-inférieure, celui-ci se comporte comme étant capable de conduire l’influx atrial au ventricule par deux voies différentes, l’une dite « rapide » antéro-supérieure et l’autre dite « lente » postéro-inférieure.
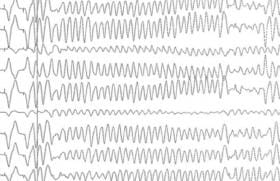
La forme la plus habituelle de la maladie de Bouveret par rythme réciproque nodal est un circuit de réentrée qui emprunte la voie lente pour la descente de l’oreillette au ventricule, et la voie rapide pour la remontée (circuit slow-fast des Anglo-Saxons). Dans ce schéma, pour qu’il puisse y avoir tachycardie réciproque entre ces deux voies, il faut que la période réfractaire de la voie rapide soit plus longue que celle de la voie lente. Un influx atrial prématuré bloquera alors dans la voie rapide et sera conduit par la voie lente avec un décrément de conduction important (PR long) : c’est ce que l’on voit sur le déclenchement artificiel de la figure 1. Si, lorsque l’influx arrive à la partie basse du nœud AV — où les deux voies, rapide et lente, se rejoignent pour donner le faisceau de His — la voie rapide est sortie de sa période réfractaire, il pourra remonter à l’oreillette par cette voie et enclencher le rythme réciproque. Cela fait un certain nombre de conditions plus ou moins faciles à réaliser, ce qui explique que bien des patients n’ont des crises que très sporadiques et qu’il est parfois bien difficile de les reproduire au laboratoire d’électrophysiologie où l’on n’obtient parfois péniblement qu’un « écho » atrial, c’est-à-dire le premier demi-tour du circuit de réentrée.
Figure 1. Tracé de rythme réciproque nodal lancé par une extrasystole atriale, avec allongement de P’R et onde P’ invisible dans les QRS de la tachycardie.
La conduite à tenir dépend donc de la clinique, car il n’y a pas de risque vital dans cette maladie. À signaler néanmoins quelques exceptionnelles observations de mort subite à l’effort. L’activité sportive doit donc être évitée chez ces patients ; en tout état de cause, la première chose à expliquer aux patients est que tout effort physique doit être stoppé dès l’apparition de la crise.
À l’ECG
La tachycardie paroxystique « nodale » liée à ce rythme réciproque « slow-fast » se présente à l’ECG comme des ventriculogrammes réguliers, à QRS fins, pas trop rapides (< 200 bpm), entre lesquels on ne voit pas d’activité atriale (ou parfois immédiatement après le QRS). En effet, après le point de jonction inférieur des deux voies, le temps que met l’influx à descendre vers le ventricule est sensiblement égal à celui mis à remonter dans la voie rapide ; les dépolarisations de l’oreillette et du ventricule sont simultanés, contrairement aux rythmes réciproques sur voie accessoire où il y a forcément un délai entre les deux. L’onde P’ est donc invisible dans le QRS, car les deux dépolarisations sont simultanées (figure 1).
Formes atypiques
Il existe par ailleurs des tachycardies nodales « atypiques », soit empruntant le même circuit décrit précédemment mais en sens inverse, descendant par une voie rapide et remontant par une voie lente (rare), soit empruntant deux voies « lentes », chose plus fréquente en particulier après une première séance d’ablation incomplètement efficace. Elles peuvent prêter à confusion avec une tachycardie orthodromique sur WPW car P’ est alors bien détachée du ventriculogramme.
Cliniquement
Il n’y a pas de crise avant l’adolescence (contrairement au syndrome de WPW) car le nœud AV n’a pas encore atteint une taille suffisante pour donner lieu à une réentrée. Il y a possibilité de tachycardie réciproque lorsque la corne postéro-inférieure du nœud est suffisamment développée après l’adolescence. Cela concerne probablement quelques pour cent de la population. Mais, dans bien des cas, les crises sont très rares et très brèves, ne posant aucun problème clinique.
On se contentera d’expliquer les manœuvres vagales : les deux plus efficaces lorsqu’elles sont effectuées par le patient sont la manœuvre de Valsalva et le réflexe nauséeux.
Il faut bien enseigner au patient qu’une manœuvre vagale a d’autant plus de chances d’être efficace qu’elle est effectuée tôt après le démarrage de la crise : après quelques minutes, il y a une stimulation sympathique réflexe qui accélère la fréquence de la crise et la rend beaucoup plus difficile à stopper.
Traitement
Le traitement médical est de mise pour arrêter la crise (ATP flash IV, plutôt que vérapamil). Pour le traitement de fond, on a le choix entre des médicaments à long terme (bêtabloqueurs, vérapamil, voire flécaïnide) ou une procédure d’ablation. Celle-ci comportant un risque de bloc AV, la décision doit être bien pesée et la balance bénéfice/risque bien exposée au patient. Par définition, on ne proposera l’ablation qu’aux patients fonctionnellement gênés et demandeurs d’un traitement radical.
Un traitement radical par ablation commence à se discuter en cas de crises longues ou fréquentes. Il devient impératif quand les patients se retrouvent fréquemment aux urgences hospitalières en tachycardie soutenue, ou lorsque soit spontanément, soit après les manœuvres vagales on constate un passage en FA. Le Bouveret nodal peut se révéler tardivement et donner lieu d’emblée à des crises fréquentes et gênantes, susceptibles de dégénérer souvent en FA après la cinquantaine. Même chez des patients plus jeunes, l’hypertonie vagale transitoire réalisée par le Valsalva peut transformer la tachycardie de Bouveret en FA.
Une autre gêne fréquente des patients est liée au caractère imprévisible du déclenchement de la crise. Si, dans certains cas, on retrouve un déclenchement à l’activité physique ou à l’antéflexion du tronc, dans la plupart des cas, il n’y a pas de circonstances favorisant le déclenchement. Aussi, certains patients vivent très mal l’insécurité réalisée par des crises fréquentes et hésitent à avoir une activité physique soutenue, à voyager, etc. Lorsque le patient est souvent pour raison professionnelle à l’étranger dans des pays médiocrement médicalisés, le traitement radical par ablation se discute fortement.
Ablation d’un Bouveret nodal
Radiofréquence
Elle consiste à modifier les propriétés de conduction du nœud AV en altérant ou en supprimant la conduction dans la « voie lente ». Le positionnement de la sonde d’ablation se fait sur des repères électroradiologiques. On se positionne donc en regard du sinus coronaire, entre celui-ci et l’anneau tricuspide, le plus bas possible par rapport au cathéter hissien. On enregistre à ce niveau des potentiels caractéristiques, de réflexion atriale (pointus) ou de potentiel nodal (mousses) (figures 2 à 4). La radiofréquence à ce niveau entraîne une activité automatique prouvant que l’on est bien au contact du tissu spécifique nodal (figure 5). On commence à délivrer des tirs le plus bas possible (à condition de bien avoir une activité automatique).
Figure 2. Schéma anatomique de la région du nœud AV.
Figure 3. Repérage radiologique et électrophysiologique de la voie lente.
Figure 4. Radiologie d’une ablation de la voie lente de face. En routine, 3 cathéters sont utilisés. Deux servent de repères anatomiques : le His et le sinus coronaire (SC). Le troisième qui est le cathéter d’ablation, recherche le potentiel de Jackmann ou celui de voie lente, devant l’ostium du sinus coronaire. Un tir de radiofréquence est délivré entre la grosse électrode distale (4 mm) et la plaque posée dans le dos.
Figure 5. Rythme jonctionnel actif au cours d’une ablation par radiofréquence de la voie lente. On voit une dépolarisation hisienne (indiquée par une flèche) devant tous les battements liés à l’irritation du tissu nodal par le courant de radiofréquence. Chacun de ces battements ventriculaires prématurés est accompagné d’une dépolarisation atriale simultanée (A) prouvant l’existence de la conduction rétrograde par la voie rapide.
Pendant le tir, il est indispensable de vérifier sur chaque battement la conduction AV rétrograde et de stopper le tir dès qu’elle manque. Le risque de lésion de la « voie rapide » est, bien entendu, de plus en plus important au fur et à mesure que l’on est amené à remonter le cathéter au-dessus du sinus coronaire, de plus en plus près du faisceau de His. Mais il est impossible de le prévoir chez un patient donné, probablement en raison des variations de conformation individuelle du nœud AV d’un patient à l’autre. Il faut donc être très prudent : arrêter le tir au moindre doute, et ne pas utiliser des températures trop élevées (60°, voire 55°).
L’autre difficulté est de savoir quand on peut arrêter la procédure : il semble qu’il ne soit pas nécessaire de supprimer totalement toute possibilité de conduction par la « voie lente ». Si, malgré tous types de stimulation et sous stimulation sympathique par l’isoprénaline, on ne déclenche qu’un écho unique, on s’arrête là, quitte à recommencer en cas de récidives. Cela suffit habituellement à obtenir un succès clinique, c’est-à-dire à transformer la vie du patient qui n’aura plus de crises fréquentes ni prolongées et ni besoin de traitement à long terme.
Moyennant ces précautions, le risque de bloc AV définitif (nécessitant habituellement un pacemaker double chambre) est faible, < 1 % dans les équipes entraînées. Il doit néanmoins être connu et accepté par le patient avant la procédure.
Cryoablation
Une alternative à la radiofréquence est réalisée par la cryo-ablation maintenant disponible par cathéter. La réversibilité de la lésion est effective tant que l’on n’a pas refroidi à une température trop basse et trop longtemps. Le risque de BAV définitif est donc réduit. En revanche, il n’y a pas de rythme automatique et le repérage est plus délicat, voire quasi-impossible si le patient n’est pas facilement déclenchable. Enfin, le diamètre de la lésion est très réduit (quelques mm) et celle-ci est très peu profonde. De fait, il y a davantage de récidives qu’avec la radiofréquence. La technique est donc nettement plus difficile d’emploi et elle n’a pas détrôné la radiofréquence, d’autant qu’elle est beaucoup plus onéreuse.
En cas de rythme nodal atypique
Chez les patients ayant un rythme réciproque nodal atypique, soit fast-slow, soit slow-slow, l’ablation doit également porter sur la « voie lente » du nœud AV. Mais la technique est plus difficile, le risque de bloc AV un peu plus important, et les résultats plus difficiles à apprécier. En particulier, il y a fréquemment un blocage rétrograde au cours de l’activité hissienne automatique générée par l’ablation de la zone postéro-inférieure du nœud AV. Cela correspond au fait que la voie « rapide » est, chez ces patients, peu perméable en rétrograde : c’est bien pour cela qu’ils n’ont pas un rythme réciproque slow-fast comme il est habituel. En soi, l’absence de conduction rétrograde au cours de l’échappement hissien actif n’est donc pas anormale chez ces patients, mais elle prive l’opérateur de tout repère pour apprécier le risque de lésion de cette voie au cours de l’ablation. Dans ces cas, le risque de bloc est plus important.
Préexcitations auriculo-ventriculaires
Les préexcitations auriculo-ventriculaires peuvent également être responsables de tachycardies de Bouveret. Cela peut être le cas dans un syndrome de WPW classique avec PR court et onde delta, donc une préexcitation patente, mais aussi, voire surtout, dans le cas des préexcitations latentes, qui sont presque toujours situées à gauche sur l’anneau mitral.
En règle des tachycardies orthodromiques
Dans ces cas, les tachycardies réciproques sont presque toujours orthodromiques, c’est-à-dire descendant de l’oreillette au ventricule par la voie normale nodo-hissienne et remontant par la voie accessoire. Le passage de l’influx dans la voie accessoire se fait plus facilement du ventricule à l’oreillette qu’en sens inverse en raison de la différence du nombre de cellules à dépolariser (impedance mismatch). La période réfractaire de la voie accessoire est habituellement plus longue en antérograde qu’en rétrograde, d’où blocage des extrasystoles atriales et déclenchement du rythme réciproque si la conduction nodo-hissienne permet de boucler le circuit de réentrée. Elles surviennent souvent à l’effort, en particulier chez l’enfant, cette circonstance étant nécessaire chez lui pour avoir à la fois des extrasystoles initiatrices et une période réfractaire nodale raccourcie permettant de boucler le circuit.
Préexcitation latente : comment la suspecter ?
À l’interrogatoire, l’existence de crises avant l’adolescence est très en faveur d’un WPW latent. Pendant la tachycardie, l’activité atriale est habituellement visible entre les ventricules, dans la première moitié de la diastole (RP’ < P’R), et sa polarité indique le siège de la préexcitation (P’ négative en VL = voie latérale gauche). Cela est surtout utile pour le diagnostic des préexcitations latentes qui se manifestent uniquement par des crises de Bouveret avec un ECG intercritique normal. Si les manœuvres vagales ne suffisent pas à stopper la crise, celle-ci est toujours arrêtée par l’injection IV flash d’ATP qui donne un blocage nodal.
Des tachycardies plus rapides.
Les préexcitations donnent des tachycardies réciproques plus fréquentes, plus rapides (> 200 bpm) et plus difficiles à stopper par les manœuvres vagales que le Bouveret nodal habituel.
L’ablation est proposée.
Les indications d’ablation sont donc nettement plus fréquentes. Une fois le diagnostic de préexcitation AV établi, soit sur le simple ECG de surface, soit après l’exploration électrophysiologique, on proposera en général l’ablation de cette voie accessoire gauche. En effet, on constate habituellement qu’une fois installées, les crises de rythme réciproque sont de plus en plus fréquentes : les deux mécanismes essentiels de démarrage que sont les extrasystoles atriales et l’altération de la conduction antérograde dans la voie accessoire (patente ou cachée) ne peuvent qu’augmenter au cours du vieillissement. De plus, elles peuvent à chaque fois entraîner un passage en FA conduite rapidement au ventricule si la voie accessoire est encore perméable.
Médicaments ou ablation ?
L’alternative est donc traitement médical ou ablation. Celle-ci sera systématiquement proposée comme traitement radical chez un patient encore jeune, la difficulté et donc les risques étant essentiellement liés à l’abord artériel rétrograde fémoral. Le risque embolique cruorique est négligeable depuis que l’on dispose de sondes à thermistance, celui de bloc AV est nul en cas de localisation latérale ou postérolatérale, de loin les plus fréquentes. Seules les localisations vraiment septales gauches ou intermédiaires posent encore problème avec taux de succès plus faible et risque de bloc AV non négligeable.
Résultats de l’ablation
À titre d’exemple, on trouvera sur le tableau nos résultats personnels de l’ablation du Bouveret au cours des 12 dernières années, en fonction des différentes localisations. On voit que l’expérience de l’équipe est l’élément majeur permettant de limiter les complications : le taux de bloc AV involontaire est de 2,3 % pour les quatre premières années, 0,5 % pour les quatre suivantes et 0,2 % pour les cinq dernières. La durée de la courbe d’apprentissage semble être de l’ordre de 4 à 5 ans à condition que l’activité de l’équipe soit importante (plus de 50 ablations de voies lentes ou de voies accessoires par an).
En pratique
La fréquence et la gêne fonctionnelle générée par les tachycardies de Bouveret sont souvent sous-estimées, par le patient, mais surtout par les médecins. De plus, le diagnostic est souvent fait avec retard chez les patients qui ne décrivent pas avec netteté les caractéristiques cliniques de leurs palpitations, puisque tous les examens intercritiques sont normaux.
Si les accès sont rares et brefs, aucun traitement n’est utile. Dès que la gêne fonctionnelle est significative et qu’un traitement se discute, les progrès techniques de l’ablation sont tels depuis plus de 10 ans que cette technique doit être proposée au patient, après lui en avoir expliqué les avantages et les inconvénients.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :