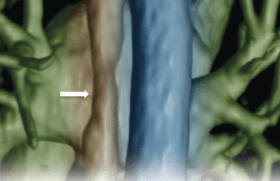
Complication
Publié le 30 sep 2013Lecture 8 min
Comment gérer la découverte tardive d’une sonde involontairement placée dans les cavités gauches ?
G. DUTHOIT, C. D’ALESSANDRO, F. HIDDEN-LUCET, Groupe Hospitalier Pitié-Salpêtrière, Paris
Les recommandations de l’HRS/AHA de 2009 sur l’extraction de sondes endocavitaires sont claires : l’extraction n’est pas indiquée (classe III) pour des sondes (fonctionnelles ou non) anormalement insérées à travers des structures inhabituelles (artère sous-clavière, aorte, plèvre, paroi atriale ou ventriculaire, médiastin) ou implantées involontairement dans une oreillette sous-aortique ou dans le ventricule systémique. Voilà le problème en théorie réglé. Il reste cependant entier pour le patient, en particulier s’il est jeune et à long terme du fait d’un risque élevé de complications cardioemboliques systémiques et infectieuses potentielles (endocardite du cœur gauche).
Chronique d’un engrenage
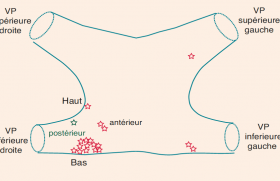
De nombreuses situations ou enchaînements malencontreux peuvent amener à positionner involontairement une sonde de stimulation/défibrillation dans l’oreillette ou le ventricule gauche (OG/VG). Il est difficile d’apprécier la prévalence de cette anomalie, heureusement rare, car elle est habituellement méconnue en l’absence de complication.
En l’absence de série publiée, une recherche sur PubMed nous a permis de dénombrer une cinquantaine de cas cliniques. La situation la plus fréquente est liée à la présence d’une communication interatriale (CIA) en particulier haute (sinus venosus) ou d’un simple foramen ovale perméable (FOP). Mais 10 Complication une stimulation VG peut également être obtenue au travers d’une communication interventriculaire :
- suite à une ponction de l’artère sousclavière ou directe de l’aorte avec franchissement rétrograde des cusps aortiques ;
- suite à une canulation du sinus coronaire et d’une veine latérale VG ;
- voire après perforation du septum interventriculaire ou de l’apex du ventricule droit (VD) avec migration épi/péricardique. Nous n’aborderons pas la gestion des sondes VG posées intentionnellement par voie transseptale à dessein de resynchronisation.
Diagnostic
Le diagnostic d’une malposition de sonde se doit d’être le plus précoce possible car :
Ce n’est qu’en période postopératoire qu’il sera suspecté et non lors d’un contrôle de pacemaker (PM) de routine, où l’ECG 12 dérivations et/ou le test magnétique ne sont pas toujours réalisés et où les paramètres de stimulation n’ont aucune raison d’être anormales sur une sonde stable.
L’extraction et le repositionnement de la sonde paraissent raisonnables dans les premiers mois et déconseillés tardivement (> 1 an) chez un patient asymptomatique.
L’ECG postopératoire et de sortie d’hospitalisation doit donc comporter 12 dérivations et un test magnétique afin de démasquer la stimulation ventriculaire pour un PM réglé en mode sentinelle ou spécifique AAI↔DDD. La présence d’un aspect de retard droit en V1 en l’absence de système resynchronisateur doit faire suspecter le diagnostic (figure A), même si cet aspect peut être présent lors d’une stimulation VD en cas de VD dilaté et/ou de stimulation septale (axe gauche du QRS entre -30° et -90°, transition précordiale en V3, absence d’onde q en D1 et aspect qR ou RS en V1).
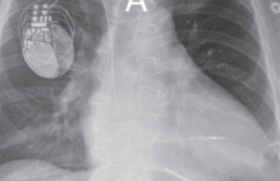
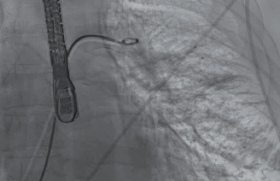
La réalisation d’une radiographie de thorax de face et de profil est impérative avant la sortie car c’est le trajet postérieur de la sonde au travers d’une CIA qui indique, de profil, le mauvais positionnement. Des sondes correctement positionnées se dirigent vers la partie antérieure du massif cardiaque (figure B). De même, la réalisation systématique ou au moindre doute à l’implantation du PM d’un cliché en OAG 30° permet de corriger le tir immédiatement (figures C et E).
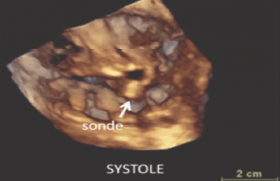
En cas de suspicion de positionnement d’une sonde dans les cavités gauches, l’échocardiographie transthoracique (ETT), plus rarement transœsophagienne (ETO), confirmera le diagnostic. Chez les patients peu échogènes, le scanner sera l’examen de choix. C’est souvent une ETT systématique qui révèle l’anomalie, plusieurs années après l’implantation.
Figure. Patient greffé cardiaque appareillé d’un pacemaker DDD pour BAV paroxystique. A : ECG électroentraîné en DDD montrant un aspect de retard droit, axe hyperdroit des QRS. B et C : Sous radioscopie de face et en OAG 30°, respectivement, la sonde ventriculaire se dirige vers le VG au travers d’un PFO. D et E : La sonde ventriculaire gauche, implantée 11 mois auparavant, est extraite au mandrin seul. Une nouvelle sonde est implantée dans le VD au niveau septal bas sous contrôle radioscopique de face et en OAG 30°, respectivement. La sonde atriale est, elle, correctement positionnée au niveau de l’auricule droit.
Gestion des sondes et des complications
Complications
La présence d’une sonde dans les cavités gauches expose à un risque spontané de complication cardioembolique et surtout cérébrale, estimé à 37 %. Il peut s’agir d’embols cruoriques ou fibrineux qui ont été décrits dès les premières 24 h postimplantation, mais également plusieurs années après. L’expérience limitée d’implantation intentionnelle de sonde VG par voie transseptale a été associée à un cas d’embolie systémique sur 20 patients anticoagulés. Selon le trajet emprunté par la sonde, on peut également observer d’autres complications : thromboses artérielles, épanchement péricardique, perforation de la valve mitrale, insuffisance mitrale, endocardite mitrale/aortique, stimulation diaphragmatique, perte de capture (sonde transfixiante), ou une toux sèche chronique par irritation du nerf laryngé récurrent gauche (trajet intra-aortique).
Techniques d’implantation
Afin d’éviter d’être confronté à des situations parfois saugrenues, la meilleure stratégie réside dans la prévention et l’usage de quelques règles simples. On ne pourra que conseiller l’abord céphalique, qui, s’il ne permet pas toujours d’implanter 2 sondes, constitue un repère anatomique fiable en vue d’une ponction veineuse sous-clavière et permet d’éviter une ponction de l’artère sous-clavière, axillaire ou de l’aorte.
Le trajet du guide vers l’oreillette droite (OD) doit être vérifié avant l’avancée du dilatateur et du désilet, ce qui permet d’éviter un risque de plaie artérielle ou aortique. En cas de doute, une phlébographie par injection directe de contraste à l’aiguille peut être utile. Pour le positionnement de la sonde atriale, l’exercice d’un mouvement de rotation horaire sur le mandrin préformé permet d’orienter la sonde vers l’OD.
Le franchissement de la valve tricuspide en boucle (« dos à la tricuspide »), formée au contact de la paroi latérale basse de l’OD permet d’une part d’éviter d’embrocher un cordage de la valve tricuspide et de créer une régurgitation et d’autre part de s’engager dans le VD sans risquer de cathétériser par abord direct le sinus coronaire ou un FOP. Dans ce dernier cas, l’incidence OAG 30° permettra le diagnostic de malposition (figure C).
Enfin il est recommandé pour la sonde destinée au VD, de franchir la valve pulmonaire jusqu’à l’artère pulmonaire (AP) droite ou gauche dont la projection est aisément identifiable. Ce dernier point permet également, en reculant la sonde vers le VD de garantir une position septale (l’AP étant plus postérieure que le septum interventriculaire) et d’éviter une perforation apicale du VD et une migration péricardique.
Anticoagulation
Au vu de l’incidence des complications thromboemboliques, il apparaît impératif, en l’absence de contre-indication d’ordre hémorragique, d’instaurer une anticoagulation orale (ACO) par antivitamine K. En effet, une revue de la littérature n’a permis d’identifier qu’un cas de récidive d’embolie systémique dans un contexte d’INR infrathérapeutique(1,6). L’INR cible est de 2,5 à 3,5. L’usage de l’aspirine n’est pas recommandé car inefficace dans cette indication.
Extraction des sondes
Dans les recommandations de l’HRS/AHA de 2009, l’extraction d’une sonde OG/VG n’est pas indiquée (classe III). Cependant, il y est précisé que des techniques additionnelles incluant une stratégie chirurgicale d’extraction peuvent être appliquées en cas de nécessité impérieuse (sic). Il apparaît donc logique de proposer en cas de découverte précoce, notamment chez un jeune patient, un retrait des sondes par voie percutanée afin de lui éviter d’être soumis à un traitement ACO au long cours.
En cas de découverte tardive (> 1 an) et en l’absence de symptômes, le risque de complications emboliques d’une extraction percutanée incite à adopter un traitement conservateur et une ACO. Entre les deux, l’expérience du centre et le bon sens doivent prévaloir. L’utilisation d’une gaine laser dans les cavités gauches est contre-indiquée. L’ETO préopératoire ne permet pas d’identifier à coup sûr du matériel fibrineux ou cruorique sur le trajet des sondes, identifié a posteriori après explantation chirurgicale de matériel. Si nécessaire, l’extraction de sondes gauches anciennes doit donc être chirurgicale, sous circulation extra-corporelle, même si des cas d’extraction percutanée ont été publiés et associés à l’utilisation de filtres de protection des troncs supraaortiques, pas toujours sans complication cérébrale…
Dans notre expérience, l’extraction tardive de sonde intraVG devrait être réservée aux récidives d’accident thromboembolique sous ACO, aux patients qui présentent une contre-indication aux ACO (ou les refusent), un épanchement péricardique récidivant ou, bien entendu, une endocardite du coeur gauche.
En cas de trajet intra-artériel, la difficulté réside dans la fermeture de la brèche d’entrée. L’HAS n’a pas reconnu en 2012 de progrès clinique pour les systèmes de fermeture percutanée par suture (système ProStar®) comparativement à une fermeture directe chirurgicale. Des cas cliniques d’extraction/fermeture percutanées réussies de sonde et de brèche artérielle sous-clavière par stent couvert ont cependant été récemment décrits.
En pratique
Le positionnement involontaire d’une sonde dans les cavités gauches, bien que rare, s’accompagne d’un risque de complications parfois dévastatrices.
Une analyse soignée du QRS électroentraîné et de la radiographie de thorax post-opératoires peut réduire la morbidité et la mortalité en permettant un diagnostic et une extraction percutanée précoces.
Pour les patients chez qui le diagnostic est retardé, un traitement anticoagulant est indiqué et une extraction chirurgicale de sonde doit être discutée en fonction de l’âge du patient et des complications rencontrées ou potentielles.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :