Indispensable ?
Publié le 30 oct 2022Lecture 9 min
L’athérectomie orbitale : un nouvel outil disponible !
Jacques MONSEGU, Institut CardioVasculaire, Grenoble
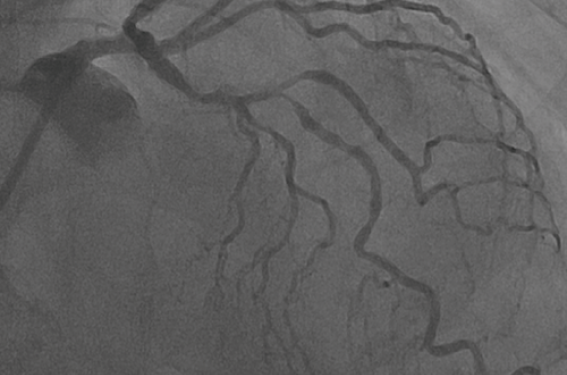
La fréquence des lésions calcifiées croît régulièrement impliquant environ 20 % des procédures d’angioplastie. Si ces lésions sont largement sous-estimées par l’angiographie conventionnelle, elles complexifient singulièrement les procédures avec un risque d’échec d’implantation de stent, de dissection, de malapposition et/ou sous-déploiement des endoprothèses coronaires générant un risque de MACE élevé dont la thrombose de stent et/ou la resténose. Elles nécessitent une préparation spécifique dominée par l’athérectomie et la lithotripsie endovasculaire.
Si cette dernière apparaît très séduisante, facile à mettre en œuvre, elle n’affecte que la compliance du vaisseau, et d’autre part la taille et le nombre d’impulsions potentiellement délivrables des ballons limitent son utilisation. L’athérectomie rotationnelle, sur les étagères depuis plus de 30 ans, n’a jamais démontré une supériorité d’efficacité sur le long terme et sa pénétration reste inéluctablement stable aux environ de 2 %. L’arrivée d’un nouveau système d’athérectomie orbitale vient bousculer la préparation de ces lésions calcifiées.
DE QUOI S’AGIT-IL ET COMMENT ÇA MARCHE ?
Le système d’athérectomie orbitale (OAS) a été développé par la société Cardiovascular Systems (CSI) sous le nom de Diamondback 360™. Il est distribué en France par OrbusNeich. Approuvé par la FDA depuis 2014, le système vient d’obtenir il y a un peu plus d’un an le marquage CE permettant sa diffusion.
Il s’agit d’un système d’athérectomie composé d’une pompe, d’un guide spécifique, d’un lubrifiant et d’une couronne sertie de diamants possédant un double mécanisme d’action (figure 1) :
– un ponçage progressif de la plaque calcifiée par un mouvement centrifuge et de rotation de la couronne ;
– une modification profonde de la plaque par les forces pulsatiles générées augmentant la compliance du vaisseau.
Le dispositif, coaxial, est constitué d’un cathéter gainé souple possédant dans sa partie distale (nosecone) une couronne de 1,25 mm de diamètre (taille unique) sertie de diamants d’épaisseur de 10 microns disposée de façon circonférentielle (figure 2). Le bloc moteur de commande (figure 3) se situe à l’extrémité proximale avec un bouton central permettant d’activer et de mobiliser la couronne, une commande tactile des vitesses et de de la purge du système. Enfin, sur la partie toute distale on trouve le bouton du frein qui permet de bloquer le guide lors de l’athérectomie.
Le système est connecté à la pompe électrique qui va transmettre par force centrifuge un mouvement elliptique et rotationnel à la couronne qui va ainsi venir au contact de la plaque calcifiée et progressivement réduire son épaisseur en réalisant une athérectomie de façon circonférentielle. La pompe peut délivrer 2 vitesses, l’une lente à 80 000 tours/min avec laquelle on débutera toujours le traitement, et la 2e rapide à 120 000 tours/min adaptée à des vaisseaux de gros diamètre (> 3 mm). Ainsi, la technique permet le traitement de vaisseaux de 2,5 à 4,0 mm de diamètre.
L’équation de la force centrifuge F= (m.v2)/r (m étant la masse de la couronne, v la vitesse de rotation et r le rayon du vaisseau) permet aisément de comprendre qu’en augmentant la vitesse, la force augmente et permet un traitement des plus larges vaisseaux. La progression de la couronne se fait sur un guide spécifique de 0,012’’ (Viper-Wire Advance™, OrbusNeich) possédant une âme en nitinol dont les caractéristiques allient souplesse, manœuvrabilité assez exceptionnelle et support, son extrémité distale étant en 0,014’’ avec un grammage de 1 g. La progression de la couronne sur son axe longitudinal se fait sur une distance maximale de 7,5 cm de long avec le bouton central. Le lubrifiant (ViperSlide™) est infusé dans le système et la coronaire via la pompe, dont la finalité est de permettre la dispersion des microparticules issues du ponçage (de taille inférieure à celle d’un globule rouge). Il permet de réduire le risque d’embolisation distale et de no-reflow, mais aussi de minimiser le risque thermique induit par la cinétique de la couronne.
L’originalité de ce système d’athérectomie est de fonctionner à la fois en antérograde et aussi en rétrograde, sans risque de blocage de la couronne. Sur des vaisseaux un peu tortueux, il s’ensuit une action d’abrasion optimisée sur la partie supérieure du vaisseau en antérograde, et sur la partie inférieure en rétrograde. Ces deux derniers points singularisent la technique par rapport à l’athérectomie rotationnelle.
Le 2e mécanisme d’action est en lien avec les forces pulsatiles générées par le phénomène elliptique de la couronne couplé à sa masse, à l’origine de fractures de la média calcifiée, bien individualisées en imagerie endocoronaire contribuant ainsi à modifier la plaque calcifiée et donc améliorant la compliance du vaisseau permettant une expansion et une apposition optimale du stent.
LES RÈGLES D’UTILISATION
Le système est compatible avec un cathéter guide 6 F et le choix d’un porteur avec un bon support est requis, pouvant dans certains cas nécessiter le recours à une extension de cathéter guide. Le choix de la voie d’abord importe peu en privilégiant la voie radiale.
Le bon positionnement du guide ViperWire Advance™ en distalité est essentiel car il est impératif de respecter une distance suffisante de 5 mm entre la partie distale du nosecone et la partie floppy du guide afin d’éviter un risque de fracture du guide lors du ponçage. Les propriétés mécaniques du guide dont sa flexibilité et la réponse de son torque permettent dans la très grande majorité des cas de le manœuvrer aisément sans avoir recours à un microcathéter.
Après avoir purgé le dispositif OAS, vérifié la mobilisation et la rotation de la couronne, la gaine est introduite dans le cathéter en faisant point fixe sur le guide et la couronne est placée en amont de la lésion à traiter. On veillera ensuite à relâcher les tensions dans le système afin d’éviter que la couronne ne saute dans la lésion lors de l’activation de la couronne.
Après verrouillage du frein, la première séquence d’athérectomie peut être débutée. Celle-ci s’effectue toujours à basse vitesse (quelle que soit la taille du vaisseau) et l’avancement de la couronne doit être très progressif sans forcer, à environ 1 mm/s avec une durée de 30 s maximum pour chaque run. Il s’agit de respecter le concept de ponçage ou d’abrasion progressive de la plaque, de façon circonférentielle, en insistant particulièrement sur les zones très calcifiées. Néanmoins, l’outil ne doit pas rester sur la même zone mais doit avancer ou reculer lentement, et ce grâce au bouton spécifique du dispositif, avec un ratio 1:1 entre la mobilité du bouton et la réponse obtenue de la couronne.
L’arrêt de la couronne doit se faire si possible dans une zone non sténosée. À la différence de l’athérectomie rotationnelle, on ne doit pas réaliser de picorage de la lésion avec l’OAS. Il est aisé de comprendre que plusieurs runs vont être nécessaires pour préparer de façon optimale la lésion, alternant une abrasion anté et rétrograde. Un temps de repos entre chaque run doit être respecté, le plus souvent égal au temps de ponçage. Sur les lésions de gros vaisseaux > 3,0 mm et massivement calcifiées, on complètera le ponçage en vitesse rapide avec des runs un peu plus courts de 20 secondes environ.
L’évaluation du résultat et du moment où on va arrêter l’athérectomie est une étape importante et repose sur plusieurs critères : certains sont purement subjectifs comme la sensation tactile de la disparition de la résistance et le bruit de sifflement de la couronne qui disparaît, mais doivent être complétés soit par une évaluation avec un ballon au ratio 1:1 afin de vérifier l’absence d’empreinte résiduelle, soit par une évaluation endocoronaire (IVUS ou OCT).
Le retrait de la couronne se fait en mode GlideAssist (vitesse ultralente à 5 000 tr/min) après avoir levé le frein du système. La qualité de support du guide permet dans la majorité des cas de terminer la procédure et l’implantation du stent sans changer de guide.
Contre-indications à respecter et complications
Ce sont les lésions de pontages, la resténose intrastent, la présence de thrombus et/ou d’une dissection au site. Des précautions devront être prises devant une dysfonction ventriculaire gauche sévère ou chez un patient présentant une hypersensibilité aux produits du lubrifiant. Comme tout système d’athérectomie et en s’attaquant à des lésions complexes, certaines complications doivent être connues et prévenues dont l’incidence diminue avec l’expérience de l’opérateur.
• Au premier rang, il faut citer le risque de perforation (0,7 %) le plus souvent lié à la couronne qui saute dans la lésion, ou les lésions sur de trop petits vaisseaux.
• Le risque de dissection est présent comme sur chaque angioplastie d’une lésion calcifiée et sera couverte par un stenting parfois long.
• Le risque de slow ou no-flow est évalué à 0,7 % des procédures et d’autant marqué que la charge calcique est importante et que le ponçage a été prolongé, singulièrement lors de l’utilisation d’une vitesse rapide. Il rétrocède le plus souvent après injection de nitré ± inhibiteur calcique, et s’accompagne d’une élévation plus ou moins importante de troponine avec un petit risque d’infarctus postprocédural.
• Enfin, citons le risque de troubles conductifs transitoires lors de l’athérectomie de grosses coronaires droites ou de circonflexe dominante, pouvant nécessiter une stimulation transitoire que nous conseillons sur guide comme dans les procédures de TAVI.
Exigée par la société CSI, une formation initiale est requise sur les 6 premiers cas avec une supervision permettant l’obtention d’une certification du praticien.
QUELLES LÉSIONS PROPOSER À L’ATHÉRECTOMIE ORBITALE ?
Technique récemment disponible, son positionnement reste encore confidentiel mais les premiers résultats obtenus sont très encourageants dans des lésions particulièrement hostiles avec une procédure relativement simplifiée dès lors qu’on accepte de prendre le temps d’effectuer une athérectomie progressive.
Avec une expérience d’une cinquantaine de procédures, il ressort que les calcifications circonférentielles avec une large extension dans la média, a fortiori sur des portions longues d’artère, se prêtent particulièrement à cette technique permettant une préparation optimale du vaisseau.
La tortuosité d’une artère, si elle doit être abordée avec précaution en évitant la vitesse rapide, est une bonne alternative dans le choix thérapeutique (figure 4).
L’OAS est particulièrement adaptée à un vaisseau dont le calibre varie entre les zones proximale et distale, la couronne unique permettant de traiter l’ensemble de la lésion avec efficacité. De même, l’efficacité de la technique dans l’approche d’un gros vaisseau calcifié est très optimale (figure 5).
D’excellents résultats angiographiques sont obtenus dans le traitement des bifurcations avec préservation de la branche collatérale dans la majorité des cas, en insistant sur un ponçage plutôt rétrograde lorsqu’il existe une discongruence de calibre entre l’amont et l’aval de part et d’autre de la bifurcation.
De même, une sténose très serrée focale est aussi aisément accessible en raison du profil très fin du nosecone.
D’excellents résultats sont obtenus sur les lésions excentriques en privilégiant le mode de traitement antéro ou rétrograde en fonction de la localisation de la lésion calcifiée (concavité ou convexité de l’artère), mais aussi sur les lésions bourgeonnantes (figure 6).
Enfin, les ostia coronaires sont accessibles par cette technique en privilégiant le traitement rétrograde, le franchissement de la couronne s’effectuant en GlideAssist en antérograde.
Pour finir, et bien que off-label, des resténoses intrastents calcifiées ont été traitées avec succès par orbital.
QUE NOUS DIT LA LITTÉRATURE ?
À l’heure actuelle, nous ne disposons que de registres mais dont le suivi à long terme est encourageant. ORBIT I, l’étude first-in-man a montré un taux de MACE de 20 % à 5 ans(1). Dans ORBIT II, étude prospective pivot ayant permis l’obtention de l’approbation FDA, le taux de sécurité était de 90 % et celui d’efficacité de 89 %(2). Le suivi de ces patients montre un taux de revascularisation de la lésion cible proche de ceux que les grands essais avec les DES retrouvent pour des lésions non calcifiées. Un large registre vient confirmer ces excellents résultats avec un taux de complications en baisse avec l’expérience acquise des opérateurs(3). De petites séries non randomisées et une méta-analyse comparant les deux systèmes d’athérectomie ont montré une efficacité similaire mais avec moins d’infarctus postprocédure avec l’athérectomie orbitale(4).
Bien entendu, la confirmation de ces résultats sera à évaluer en France et en Europe et le positionnement de cet outil nécessitera des essais randomisés comparatifs.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


