Polémique
Publié le 25 juin 2020Lecture 16 min
L’incontournable physiologie coronaire
Patrick DUPOUY, PCVI Hôpital Privé d’Antony ; Clinique les Fontaines, Melun
La FFR (fractional Flow Reserve ou fraction de réserve coronaire) a mis plus de 20 ans pour gagner ses lettres de noblesse et être admise dans les salles de cathétérisme. Le succès en est tel que de nombreux concurrents sont apparus et tentent de détrôner la reine FFR. Nous allons essayer de comprendre comment ils pourraient y arriver et ce qu’il faut en penser.
Pour cela, il n’est pas inintéressant de se rappeler le cheminement de la réflexion qui a conduit à faire de la FFR la référence de l’évaluation du retentissement des lésions coronaires.
Les publications princeps sur la FFR se sont attachées à transformer un paramètre purement hémodynamique en un paramètre d’évaluation de l’ischémie myocardique induite par des lésions intermédiaires. Les comparateurs étaient les tests fonctionnels traditionnels, essentiellement scintigraphie, épreuve d’effort et échographie de stress. La valeur seuil de 0,75 au-dessus de laquelle il n’y avait pas d’ischémie mise en évidence est devenue une référence. Il s’agissait à l’époque de comparer une nouvelle méthode par rapport à des références dont on connaissait pourtant les imprécisions diagnostiques.
Sur cette base là il est peu de dire que la FFR n’a pas enthousiasmé les foules interventionnelles, en dehors de quelques jeunes passionnés (dont votre serviteur) qui ont eu les plus grandes difficultés à faire passer le message : la FFR était peut-être plus appropriée que le sacro-saint réflexe oculosténotique, référence absolue de l’époque.
Il a fallu les revers de l’étude COURAGE (et plus récemment ISCHEMIA) et les quelques thromboses des premiers stents actifs pour que la communauté cardiologique interventionnelle ressente la nécessité de valider l’indication de revascularisation retenue et commence à naturellement se tourner vers un concept intellectuellement et techniquement simple, la mesure de FFR en hyperhémie par guide pression.
Entre temps, le concept de FFR avait progressivement évolué d’un statut de marqueur d’ischémie vers un statut de marqueur pronostique des patients. D’abord dans l’étude DEFER avec une valeur seuil de 0,75, qui montrait que le stenting d’une lésion coronaire avec une FFR < 0,75 avait un meilleur pronostic que le traitement médical, ou même que le stenting d’une lésion coronaire > 0,75, puis avec l’étude FAME(1) qui montrait que le choix des lésions à revasculariser sur la foi d’une FFR < 0,80 chez un patient pluritronculaire était bénéfique. Enfin l’étude FAME-2 confirmait le statut d’indicateur pronostique en montrant que de ne pas traiter une lésion < 0,80 était délétère. L’intégration de la FFR dans la pratique quotidienne s’est faite avec les résultats des études DEFER, FAME-1 et FAME-2(2) qui ont transformé un paramètre hémodynamique en un paramètre pronostique, sans plus passer par la case ischémie.
Il a fallu 15 ans pour en arriver là, puis encore 5 pour que la FFR obtienne un niveau IA dans les recommandations de l’ESC 2014(3).
Les concurrents sont allés beaucoup plus vite
Force est de constater que malgré un niveau de recommandation élevé et une prise en charge économique du guide pression, l’utilisation de la FFR se situe aux alentours de 6-10 % des examens invasifs.
Plusieurs raisons peuvent être évoquées comme la mauvaise tolérance de l’adénosine que ce soit en perfusion continue (douleurs thoraciques, dyspnée, BAV) ou en bolus (essentiellement BAV, toujours transitoires mais parfois stressants et parfois douleurs throraciques), le coût de l’adénosine, les manipulations et le temps nécessaire aux mesures en particulier sur des lésions pluritronculaires avec éventuel changement de cathéter.
Sur un plan plus physiologique, nombreux sont les collègues qui se posent des questions sur les incertitudes concernant la dose d’adénosine à utiliser en bolus ou la valeur seuil.
Par ailleurs, il a été montré par PET que l’hyperhémie pharmacologique n’était pas homogène en fonction du caractère plus ou moins sténosant de la lésion étudiée, avec une nette diminution de l’hyperhémie induite pour les sténoses les plus serrées(4). Ce qui est embêtant puisque le rôle de l’adénosine est de stabiliser les résistances distales, seule condition à la linéarité de la relation pression/débit, base théorique de la mesure de la FFR.
L’index de repos
D’où l’idée d’un index de repos, par définition plus « physiologique » et respectant le débit coronaire au dépend de la pression de perfusion distale à la lésion par autorégulation et diminution des résistance s microvasculaires. Comme on le sait, la circulation coronaire est phasique avec en systole des ondes de flux antagonistes venant d’une part de l’aorte et d’autre part de la microvascularisation distale (contraction myocardique et baisse du débit coronaire). En diastole, ces ondes de flux antagonistes disparaissent et les résistances microvasculaires sont minimales et surtout stables, autorisant l’utilisation de la linéarité de la relation pression/débit. C’est à partir de ces constatations et de la mesure du ratio Pd/Pa pendant cette wave free period qu’ont été développés les index diastoliques de repos dont l’iFr est le précurseur.
Dans un premier temps le jeu a consisté à se comparer à la référence FFR. La première publication est l’étude ADVISE(5) en 2012 qui a montré une bonne corrélation entre l’iFR et la FFR (r = 0,9) et une excellente reproductibilité de la mesure. Bonne corrélation pas toujours retrouvée dans toutes les études, ce qui a longtemps entretenu une suspicion sur la valeur de la iFR. La valeur seuil retenue pour la iFR était de 0,83 dans ces premières études. Il a aussi été montré que les résistances microvasculaires étaient égales en hyperhémie pharmacologique et en période diastolique sans onde de flux.
En fait, toutes ces comparaisons sont « empêchées » parce qu’il n’y pas de référence absolue en termes de test d’ischémie myocardique. Une autre approche physiologique a donc été de comparer iFR et FFR aux résistances sténotiques en hyperhémie (marqueur historique de l’ischémie myocardique décrit par Gould en 1978). Les deux types de mesure se sont révélées strictement identiques avec 92 % de précision diagnostique. Une autre étude a comparé iFR et FFR à la positivité des résistances sténotiques et au résultat d’une scintigraphie myocardique. Là encore les deux types de mesure ont fait match nul. Mêmes résultats par rapport à une évaluation de l’ischémie par PET ou par rapport à la mesure de réserve coronaire.
Très rapidement, la comparaison entre les deux techniques s’est déplacée sur l’aspect pronostique avec les études DEFINEFLAIR et SWEDEHEART(6,7), regroupant 4 500 patients à elles 2, randomisés entre FFR et iFR. Études de non-infériorité avec comme valeur seuil retenues, 0,80 pour la FFR et 0,89 pour la iFR. Les deux études ont validé la non-infériorité de la iFR par rapport à la FFR pour les MACE (réintervention, décès, infarctus) à 1 an et à 2 ans pour les deux études. À noter qu’il y avait moins de revascularisation dans le groupe iFR (-5 % vs FFR) dans DEFINE-FLAIR. Parmi les critères secondaires, la longueur de la procédure était significativement plus courte avec la iFR et les patients avaient significativement moins d’effets secondaires. À partir des résultats de ces deux études, confirmés par le registre SWEDEHEART et d’autres publications dont une métaanalyse qui confirment que FFR et iFR permettent de guider la décision d’angioplastie avec la même sécurité sur le pronostic des patients, les index diastoliques ont obtenu une recommandation IA en 2018, au même titre et sur la même ligne que la FFR, soit 6 ans après la première publication du concept.
Alors FFR ou IFR ?
On l’a vu, tout est question de comparateur. Le comparateur absolu n’existant pas en ce qui concerne l’ischémie myocardique (si ce n’est l’occlusion de l’artère), il faut certainement étudier plus en détail les finesses physiologiques de deux concepts qui ont validé un même intérêt pronostique dans la décision de revascularisation d’une lésion coronaire.
Chacun a ses partisans et ses détracteurs. Les afficionados de la FFR argumentent que la wave free period n’existe pas et que les index diastoliques ne sont qu’un Pd/Pa de repos. À l’inverse, on peut aussi souligner que la FFR mesurée sur l’ensemble du cycle cardiaque intègre des résistances microvasculaires variables entre la systole et la diastole, malgré l’hyperhémie pharmacologique utilisée ce qui tendrait à mettre à mal le postulat de la linéarité de la relation pression/débit.
Pourtant quand on compare la dispersion des mesures de FFR, iFR ou Pd/Pa sur les mêmes lésions, la dispersion des valeurs est identique pour la FFR et la iFR et bien plus concentrée pour la Pd/Pa traduisant une potentialité de différenciation des lésions moindre pour la Pd/Pa (figure 1).
Figure 1. A : Le débit coronaire de repos est préservé jusqu’à des sténoses pré-occlusives. Pour maintenir un débit de perfusion stable, il faut une vasodilatation de la microcirculation qui se fait au dépend d’une chute de la pression distale. La pression distale de repos est un indicateur du degré de sténose sur un territoire myocardique donné. B : Pour une même série de sténoses, la dispersion des mesures de la Pd/Pa est insuffisante pour discriminer les degrés de sténose. La iFR et la FFR ont à peu près le même pouvoir discriminant.
(D’après Sukhjinder S et al., Circ J 2015 ; 79: 1172 et Park JJ et al. Int J Cardiol 2013 ; 168 : 4070)
Ce qui est sûr, c’est que l’une et l’autre technique sont supérieures à la coronarographie même quantitative et permettent de différencier l’impact physiologique de lésions anatomiques avec un pronostic global meilleur, ou plus adapté. Ceci a été démontré par les études R3F(8), POST-IT pour la FFR, et des sous-études de DEFINE-FLAIR, SWEDEHEART pour la iFR selon lesquelles les 40 à 50 % des lésions évaluées qui n’étaient pas revascularisées sur l’argument physiologique, avaient le pronostic clinique identique et excellent avec les deux méthodes.
Comment interpréter les discordances FFR, IFR et qu'en faire ?
La tentation est grande pour « l’accro » à la physiologie coronaire de faire les deux types de mesure et la désillusion est aussi grande quand les résultats ne concordent pas, ce qui survient dans environ 20 % des cas, plus souvent sur des lésions proximales, chez les femmes, ou en cas de diabète.
Faut-il donc obligatoirement choisir son camp ?
Deux cas de figures sont possibles : situation 1 : iFR+ et FFR- ou situation 2 : iFR- et FFR+.
Plusieurs études ont essayé d’analyser le profil physiologique de chacun et de vérifier si leur impact clinique était le même.
On a déjà vu que plus une sténose était serrée, moins l’hyperhémie était importante, pouvant sous-estimer la mesure de FFR et expliquer la situation 1. A contrario, l’hyperhémie peut être anormalement élevée et donc majorer de façon paradoxale le débit translésionnel et donc sur-estimer la mesure de FFR, ce qui pourrait expliquer la situation 2.
Une étude de 2017 a ainsi montré que la réserve coronaire de débit ou de résistance était basse dans le cas 1 et sub-normale ou normale dans le cas 2(9). L’évolution technologique nous donne accès à une mesure rapide, facile et reproductible des débits coronaires et donc à la réserve coronaire. Le système Coroventis™ permet de faire des mesures de débit au repos ou en hyperhémie en plaçant un microcathéter de perfusion à l’ostium de l’artère étudiée. Ce microcathéter (RayFlow™, Hexacath) doit être monté sur un guide de pression équipé de thermistance pour une mesure des débits par thermodilution et des résistances microvasculaires (figure 2).
Figure 2. La mesure de la réserve coronaire pourrait permettre de différencier les ambiguïtés FFR/index diastolique(9). L’infusion de sérum physiologique à température ambiante sur un guide pression équipé d’une thermistance permet de mesurer facilement la réserve coronaire et un index de résistances microvasculaires (IMR).
Reste à déterminer l’impact clinique de l’une ou l’autre situation, ce qui n’a pour le moment pas été clairement établi, entre pronostic identique des deux aspects « ambigus » ou indication de revascularisation du cas 1 où la réserve coronaire est basse et de traitement médical du cas 2 où la RC est normale ou élevée.
Pour les plus sceptiques, un protocole hybride ?
Pour les sceptiques de la iFR, il a pu être proposé une attitude hybride consistant à d’abord faire une mesure de iFR pour son gain de temps, de coût, de tolérance et de facilité d’utilisation et de ne compléter par une mesure de FFR que si la iFR se situait dans une zone entre 0,86 et 0,93. On obtenait ainsi une concordance de décision thérapeutique dans 95 % des lésions explorées, en se passant de l’hyperhémie dans 60 % des cas.
Si ce type de protocole reste encore largement utilisé, il se heurte aux ambiguïtés de résultats décrits plus haut et surtout il fait fi des résultats des études DEFINE-FLAIR et SWEDEHEART qui ont montré que la décision thérapeutique sur la iFR seule avait un impact pronostique équivalent à la mesure de FFR.
Les deux techniques ont un niveau de recommandation IA et donc une égale légitimité médicale à être utilisées. Il n’est donc pas logique, en 2020, de valider le résultat de l’une par l’autre. Chaque concept a ses forces et ses faiblesses dont découlent les apparentes contradictions, dont on sait qu’elles n’ont pas forcément de conséquences pronostiques discriminantes.
L’idée d’un protocole hybride sous-entend que l’une des techniques est la référence (en l’occurrence la FFR) et l’autre un dérivé moins performant qui peut rendre service.
Les choses pouvaient certainement être analysées de cette façon au début de l’expérience iFR, mais l’accumulation des études et de l’analyse fine de la physiologie coronaire ont changé la donne.
En 2020, il n’est plus rationnel d’utiliser ce protocole hybride, et il est plus juste de n’utiliser que l’une des deux techniques. Celle qui nous a le mieux convaincu et avec laquelle on se sent le plus confortable, en tant qu’opérateur et par rapport au patient.
Tous les index diastoliques sont-ils identiques ?
La iFR étant un concept propriétaire, de nombreux autres index diastoliques de repos nous ont été proposés. Le Pd/Pa sur toute la diastole (diastolic pressure ratio, dPR), de 25 à 75 % de la diastole (dPR25-75), à mi-diastole (dPRmid), des dérivés de l’iFR par raccourcissement de 50 ou 100 msecs de la durée analysée de la période libre de flux (iFR-50 ms, iFR-100 ms) ou la RFR (resting full cycle ratio, le nadir de Pd/Pa sur tout le cycle cardiaque) et la DFR (diastolic hyperhemia-free ratio, Pd/Pa moyenne pendant toute la diastole) sont commercialisés par les industriels de matériel coronaire que nous connaissons bien (figure 3).
Figure 3. Les index diastoliques. 1. iFR Pd/Pa moyenne pendant toute la wave free period. 2. DFR (diastolic hyperhemia free period) : Pd/Pa moyenne entre le point ou la Pa croise la courbe de Pa moyenne et le nadir de la Pa. 3. RFR (resting full cycle ratio) : Pd/Pa la plus basse pendant tout le cycle cardiaque. 4. DPR (diastolic pressure ratio) : Pd/Pa moyen ne sur toute la durée de la diastole.
Plusieurs études ont montré une concordance de 99 % entre tous ces paramètres et la iFR et une précision diagnostique de 77 % avec la FFR. C’est d’ailleurs dans ce sens que les recommandations ne font pas de différence entre tous ces paramètres de repos en les référençant sous le terme générique d’index diastolique de repos(10).
Le registre sud-coréen IRIS-FFR sur 1 102 lésions, confirme des performances diagnostiques et pronostiques équivalentes entre tous ces paramètres avec la FFR sur des lésions non revascularisées sur argument physiologique. La conclusion essentielle de toutes ces études est qu’il n’est pas dangereux et même sécurisant de différer une angioplastie coronaire quand les critères physiologiques le valident (figure 4).
Figure 4. La physiologie coronaire dans la vraie vie du cathlab. La décision de revascularisation et de type de traitement sont modifiés chez 30 à 40 % des patients par l’évaluation physiologique des lésions, que ce soit dans le syndrome coronaire chronique ou aigu et que ce soit par une mesure de FFR ou par une mesure d’index diastolique (A). Les patients pour qui l’indication de revascularisation a été récusée ont un excellent pronostic clinique (B).
(D’après Van Belle E et al. : Circulation 2014 ; Circ Cardiovasc Interv 2017 ; JACC Cardiovasc Interv 2018)
Vers un nouveau paradigme de la revascularisation coronaire ?
Toutes les maladies athéromateuses ne sont pas identiques d’un patient à l’autre. Une infiltration diffuse mais homogène le long d’une artère coronaire épicardique peut avoir les mêmes conséquences physiologiques sur la circulation coronaire qu’une ou plusieurs lésions successives et pourtant le traitement proposé ne sera pas le même.
L’évaluation des lésions angiographiquement suspectes en chapelet a toujours posé problème au cardiologue interventionnel. Quelle lésion traiter en sachant qu’une évaluation en hyperhémie ne peut analyser que l’impact FFR de l’ensemble du segment malade sur un territoire myocardique. L’analyse de l’impact physiologique de chaque sténose est difficile, voire impossible puisque chaque sténose influence le flux hyperhémique des lésions d’amont ou d’aval. Des équations compliquées, impossibles à appliquer en pratique quotidienne ont été proposées… pour en revenir à un choix très empirique de l’algorithme thérapeutique retenu.
Les index diastoliques sont mesurés en état stable de repos, à chaque battement cardiaque, sans hyperhémie et sans provoquer d’augmentation de débit translésionnel. Il est donc possible d’évaluer l’impact de chaque lésion, qui du fait de la stabilité des résistances d’aval influent beaucoup moins les unes sur les autres. À l’état de repos, le débit coronaire est préservé et stable, malgré la présence possible d’une sténose significative. Ce qui suggère que la chute de pression éventuellement observée est essentiellement dépendante de la lésion d’amont, sans interférence avec la maladie athéromateuse d’aval (tableau).
L’enregistrement en continu de l’index diastolique de repos lors du retrait du guide pression le long de l’artère étudiée (pull back) permet de visualiser et de calculer tous les gradients de pression de toutes les lésions observées et d’évaluer leur sévérité individuelle (figure 5).
Figure 5. L’intérêt du pull back. A. Infiltration athéromateuse diffuse avec une plaque 45-50 % de l’IVA moyenne. La RFR est positive à 0,86 mais le retrait ne met pas en évidence de gradient focal. Ce qui peut être interprété comme l’absence de gain attendu au stenting pour lequel il est du coup difficile de décider sur quel segment l’artère devrait être traitée. B : Même cas de figure mais avec à l’évidence un gradient de pression focal qui laisse espérer une normalisation des pressions distales par stenting de la zone (*).
Et puisque nous sommes en état stable, et que l’on connaît le gradient de pression que l’on va supprimer en dilatant, il est possible de calculer et de virtuellement prévoir l’index diastolique après correction de telle ou telle sténose. Quelques études ont montré une excellente prédictibilité du résultat physiologique après angioplastie et ont même amené à une modification de la procédure initialement prévue dans près de 30 % des cas(11).
Il a récemment été décrit le même principe de retrait progressif du guide pression en hyperhémie par mesure de FFR, appelé pull back pressure gradient index (PPG)(12).
Convenons-en, il pourrait s’agir d’une véritable révolution dans notre approche thérapeutique de l’angioplastie coronaire avec la possibilité d’analyser le profil physiologico- anatomique par co-enregistrement (co-registration) du retrait du guide pression et de l’image angiographique ou IVUS et ainsi de décider des zones à stenter ou pas, du nombre de stents à poser, leur longueur et même d’en prévoir un résultat physiologique virtuel.
Sur le plan pratique
Que ce soit pour une mesure de FFR ou d’index diastolique, la technique d’utilisation du guide pression doit répondre à la même rigueur technique. Égalisation à la sortie du guiding des signaux avant toute mesure et vérification de l’absence de déviation en fin d’évaluation, utilisation systématique de dérivés nitrés en début d’évaluation. Rincer le guiding avec du sérum physiologique plutôt que du produit de contraste qui est plus visqueux et amorti les pressions hydrostatiques (ceci est d’autant plus important que le diamètre de la sonde est petit) (figure 6). Sortir la sonde porteuse de l’ostium de l’artère évaluée pour ne pas créer un gradient parasite. Enfin pour les index diastoliques, respecter un délai entre la dernière injection (surtout s’il s’agit de produit de contraste qui est hyperémiant) et la mesure afin d’être sûr d’être en état de repos stable.
Figure 6. Trucs et astuces. La technique de mesure doit être rigoureuse (A). En particulier bien rincer au sérum physiologique le cathéter porteur (surtout s’il s’agit d’une sonde diagnostique) pour éviter l’amortissement des courbes de pression (Pa) aortique due à la viscosité du produit de contraste. Après rinçage (B), les courbes sont harmonieuses et la mesure est fiable.
Conclusion
Quel chemin parcouru depuis les débuts de l’angioplastie il y a 40 ans ! Rappelons que la première angioplastie coronaire par Andreas Gruentzig en 1978 s’est faite sous monitoring de la pression coronaire translésionnelle.
La physiologie de la circulation coronaire a beaucoup progressé tant sur le plan technique que conceptuel. On a vu que tous les paramètres physiologiques sont maintenant relativement facilement accessibles aux cardiologues interventionnels un peu motivés.
Reste bien sûr à valider l’impact clinique de tous ces nouveaux protocoles mais ne doutons pas que l’angioplastie coronaire des 10 prochaines années sera physiologique, aidées par les techniques de traitement d’image comme la QFr ou le FFR-CT qui pourraient rendre les mêmes services et qui sans chercher de validation head to head avec la reine FFR dont on a vu les ambigüités, s’engagent, comme les index diastoliques vers une validation clinique moins critiquable et pour finir plus rapide à obtenir.
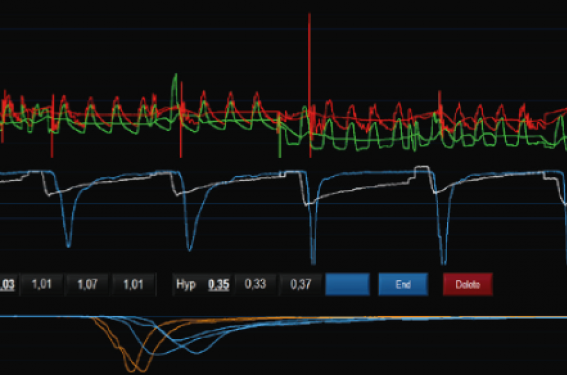
Cas clinique
➜ Il s’agit d’une patiente de 49 ans hospitalisée pour élévation isolée de la troponine. Notion de malaise 3 semaines avant. Pas de facteurs de risque particulier.
A : La coronarographie montre un athérome diffus avec une infiltration plus marquée de l’IVA apicale, sans réelle lésion a priori « ischémiante ». Cependant,
l’opérateur décide de faire une évaluation physiologique endocoronaire. La FFR et la RFR distale sont largement positives respectivement à 0,74 et à 0,77. La RFR
proximale est normale à 0,94 qui traduit un probable obstacle au niveau de l’IVA moyenne, non évident sur la coronarographie.
B : Le retrait RFR (pull back) de la partie moyenne de l’IVA vers son ostium met en évidence un gradient de RFR brutal de 0,15 au niveau de l’IVA moyenne qui traduit
l’existence d’une lésion focale, qu’une étude attentive de l’image coronarographique attribue à une image claire « sub-luminale » qui est confirmée par l’imagerie
IVUS et qui du coup sera traitée comme il se doit par un stenting focal, qui permettra de normaliser la RFR (0,95).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


