Publié le 28 fév 2009Lecture 10 min
Technique et indications du Rotablator® en 2009
N. DUMONTEIL, N. BOUDOU, D. CARRIÉ, Fédération de cardiologie, Pôle cardiovasculaire et métabolique, CHU Rangueil, Toulouse.
L’athérectomie rotationnelle (AR) est une technique d'angioplastie développée par le Dr David C. Auth et introduite durant la fin des années 1980. Son utilisation reste peu fréquente, correspondant actuellement à environ 1 à 2 % des procédures en France. Cette mise au point s’intéresse aux spécificités liées à cette technique, à ses indications et principaux résultats.
La technique
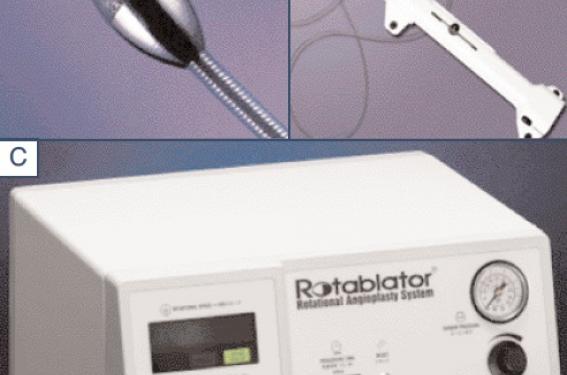
Elle repose sur la rotation à très grande vitesse (140 000 à 190 000 tours/min) d’une fraise dont la surface antérieure est recouverte de microparticules de diamants (figure 1) et qui est avancée au contact de la lésion à traiter. Ceci provoque une destruction des structures non élastiques rencontrées telles que les lésions d’athérome fibreuses et/ou calcifiées tandis que la paroi artérielle saine et élastique est respectée. C’est le principe du differential cutting (figure 2). La grande majorité des débris ainsi produits sont de taille inférieure à 12 μm. Ils n’ont le plus souvent pas d’impact objectivable sur le flux sanguin coronaire et sont éliminés dans la microcirculation.
Figure 1. Système d’athérectomie rotationnelle Rotablator®. A : extrémité d’une fraise montée sur son guide RotaWire® ; B : unité motrice et système d’avancement de la fraise ; C : console permettant le contrôle de la vitesse de rotation.
Figure 2. Illustration du differential cutting produit par l’athérectomie rotationnelle.
La fraise est montée sur un guide dédié (RotaWire®), fin en distalité (0,009’’) et long (325 cm), qui est moins performant et dont le maniement est plus délicat qu’un guide d’angioplastie conventionnel. C’est pourquoi, surtout en cas d’anatomie coronaire complexe et tortueuse, on commence fréquemment par franchir le segment cible au moyen d’un guide d’angioplastie adéquat. Un ballon coaxial ou un microcathéter est monté au-delà de la lésion à traiter, ce qui permet un échange de guide pour le RotaWire qui peut alors être facilement acheminé au fond de l’artère.
Six tailles de fraises sont disponibles, de 1,25 à 2,5 mm, avec nécessité d’adapter le calibre du cathéter-guide et donc de l’introducteur artériel à ces dimensions, influençant le choix de la voie d’abord, notamment pour les plus gros diamètres (lumière du cathéter-guide supérieure de 0,004’’ au diamètre de la fraise).
Après que la fraise, raccordée à l’unité motrice et à la console (figure 1) ait été testée en dehors du patient, l’athérectomie rotationnelle peut commencer. À chaque taille de fraise correspond une vitesse optimale de rotation, qui doit être réglée sur la console. On dit classiquement que la technique d’ablation consiste à « picorer » la lésion par avancées successives jusqu’au franchissement. Les temps de fraisage peuvent être de 30 secondes maximum avec, entre chaque passage, un temps d’attente équivalent au temps de fraisage précédent. Le diamètre maximal de la fraise à utiliser dépend de celui de l’artère cible avec un rapport diamètre fraise/artère ne devant pas excéder 0,70, comme l’ont démontré les essais STRATAS et CARAT(1). En fonction de la sévérité de la sténose à traiter, il est conseillé de commencer l’athérectomie rotationnelle par une fraise de plus petite taille puis d’augmenter les diamètres utilisés, sans incrémentation de plus de 0,5 mm.
Une des principales précautions d’emploi consiste à mettre en place, le temps de l’athérectomie rotationnelle, une sonde de stimulation endocavitaire temporaire lorsque la lésion cible se trouve sur une artère coronaire droite ou une circonflexe dominante, du fait de la grande fréquence de passages en bloc auriculoventriculaire complet transitoire, expliqués par des réflexes endocardiaques.
Les contre-indications, absolues ou relatives, à l’athérectomie rotationnelle par Rotablator® sont :
• une zone d’occlusion ne pouvant être franchie par un guide ;
• une dysfonction systolique VG sévère (FEVG < 30 %) avec un seul vaisseau restant ;
• une lésion située sur un pont veineux saphène ;
• un thrombus endoluminal au niveau de la zone à traiter ;
• une dissection préexistante au niveau de l’artère cible.
Cette technique peut être appliquée, mais avec beaucoup de précautions et un risque de complication accru en cas de :
• patient non éligible pour une éventuelle chirurgie de pontages de secours ;
• lésions à traiter multiples, tritronculaires (à effectuer en plusieurs temps) ;
• lésion du tronc commun coronaire gauche non protégé ;
• FEVG < 30 % ;
• lésion > 25 mm ;
• lésion angulée ≥ 45°.
De prime abord, l’AR au Rotablator® peut sembler agressive et faire craindre un taux de complications élevé. Les données issues de la plupart des registres s’étant intéressés à ce sujet sont en fait rassurantes avec un taux de décès intrahospitaliers voisin de 1 %, d’infarctus du myocarde avec onde Q de 1 à 2 % et de nécessité de pontage coronaire de 1 à 2 %. Les taux de complications angiographiques sont d’environ 1 % pour la perforation, 1 % pour les occlusions aiguës, 2 % de slowflow, 4 % de dissections et 5 % de spasmes(1). Le traitement est similaire à celui proposé en cas de complication de ce type survenant en cours d’angioplastie conventionnelle.
Les indications en 2009
L’AR, en abrasant les lésions athéromateuses par le principe du differential cutting, peut sembler être une méthode en théorie supérieure à l’angioplastie au ballon conventionnelle pour la préparation de la plaque. La réduction du volume de plaque résiduelle avant implantation d’une endoprothèse, dont on sait qu’il est proportionnel à la quantité de prolifération néo-intimale intrastent et la diminution du barotraumatisme subi par l’artère, sont autant d’avantages de l’AR dont on pourrait attendre un bénéfice clinique en termes de diminution des événements cardiovasculaires majeurs. Malheureusement, les différents essais cliniques ayant testé cette technique dans des indications variées n’ont pas permis de démontrer de réduction de mortalité ou de taux de revascularisation de la lésion cible (TLR) à longue échéance(1).
Prévenir la resténose et diminuer le taux de TLR
La plupart des indications potentielles ont fait l’objet d’essais dédiés. L’étude DART (Dilatation versus Ablation Revascularization trial Targeting restenosis), a cherché à déterminer si l’AR versus angioplastie au ballon pouvait prévenir la resténose après traitement de lésions simples, type A ou B1 ; TLR identique dans les deux bras(1). Même résultat dans l’étude SPORT (Stent implantation POst Rotational atherectomy Trial) qui s’est intéressée à une stratégie d’AR systématique avant stenting pour des lésions peu ou modérément calcifiées(1).
L’essai ERBAC (Excimer laser, Rotational atherectomy and Balloon Angioplasty Comparison study) a randomisé les patients en trois groupes de traitement : athérectomie au laser, AR et angioplastie conventionnelle au ballon, pour des lésions complexes de novo, type B2 ou C. Malgré un taux de succès de la procédure supérieur avec l’AR, les taux de TLR à 1 an en cas d’AR étaient significativement plus élevés(1).
L’AR a également été comparée au ballon dans le traitement de la resténose intrastent non actif, sans plus de succès puisque dans l’essai ARTIST (Angioplasty versus Rotational Atherectomy for the Treatment of Diffuse In-Stent Restenosis Trial), le taux de resténose à 6 mois était supérieur dans le bras Rotablator®. En cas d’occlusion coronaire chronique, une stratégie d’AR systématique n’apporte pas de bénéfice par rapport à l’angioplastie conventionnelle sur le taux de resténose à long terme ou de complication aiguë(1).
Améliorer l’efficacité des stents actifs ?
Enfin, plusieurs spécificités liées aux stents actifs (DES) peuvent faire espérer un bénéfice du Rotablator® avant implantation de ce type d’endoprothèses. On peut en effet se demander si d’importants frottements d’un DES sur une artère très calcifiée ne risquent pas d’altérer le polymère et de compromettre son effet de prévention de la resténose. La diffusion locale de la molécule antiproliférative ne peut-elle pas être atténuée au niveau d’une lésion très calcifiée ? Le sous-déploiement d’un DES dû à une lésion très calcifiée peut augmenter le risque de thrombose.
Malgré ces arguments théoriques en faveur de la préparation des lésions calcifiées par AR avant implantation d’un DES, on ne retrouve pas, à grande échelle, de bénéfice clinique procuré par cette technique. Dans une étude ancillaire de TAXUS IV, on observe une réduction de TLR avec un DES délivrant du paclitaxel identique, que les lésions soient calcifiées ou non(2).
Une étude rétrospective a comparé le TLR et la mortalité à 6 mois de patients avec des lésions très calcifiées après traitement par DES délivrant du sirolimus, avec et sans prétraitement par AR. Avec bien sûr toutes les réserves méthodologiques que l’on peut émettre concernant l’interprétation de ces résultats, aucun bénéfice clinique de l’AR n’a été observé dans ce travail(3).
En résumé, que ce soit dans le traitement des lésions simples ou complexes, dans la resténose intrastent, ou comme préparation à l’implantation d’une endoprothèse coronaire active ou non, aucune étude n’a montré de bénéfice clinique à long terme de l’athérectomie rotationnelle par Rotablator®.
On ne peut donc pas dégager d’indication systématique de cette technique, sous-tendue par l’espoir d’un bénéfice en termes de réduction de TLR ou d’événements cardiovasculaires majeurs.
En pratique quotidienne
Dans la pratique quotidienne, actuelle, d’un service de cardiologie interventionnelle, il existe néammoins des indications incontournables de l’AR correspondant tout simplement à des situations dans lesquelles, sans le recours au Rotablator®, la procédure d’angioplastie ne pourrait être menée à son terme.
Il s’agit, essentiellement du fait de leur caractère extrêmement calcifié et/ou fibreux, de lésions impossibles à dilater de manière satisfaisante au ballon ou impossibles à franchir avec le matériel d’angioplastie (ballon ou stent).
Cas cliniques
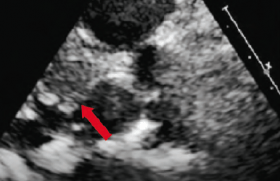
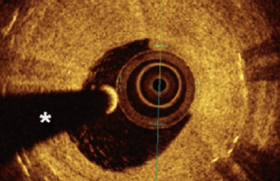
La première situation peut être illustrée par le cas d’un patient de 76 ans que nous avons eu à traiter pour un syndrome coronaire aigu sans susdécalage du segment ST avec signes électriques de souffrance en territoire antérieur. La coronarographie a révélé plusieurs lésions étagées longues, complexes, calcifiées de l’IVA proximale et moyenne (figure 3). Deux raisons ont conduit à l’utilisation du Rotablator® : l’extrême difficulté à acheminer un ballon au niveau de la lésion la plus distale malgré un bon support, l’impossibilité de prédilater de manière satisfaisante la lésion la plus serrée. L’emploi de l’AR avec fraises de 1,25 jusqu’à 1,75 mm a permis d’acheminer puis d’implanter deux DES jointifs.
Figure 3. A : lésions complexes étagées calcifiées de l’IVA ; B : lésion ne cédant pas lors de la prédilatation ; C : fraise de 1,75 mm ; D : résultat final après implantation de deux DES jointifs.
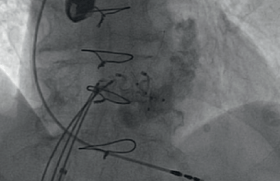
La deuxième situation dans laquelle l’AR vient apporter une solution salvatrice est illustrée par le cas de ce patient de 53 ans qui après de multiples pontages coronaires souffrait d’un angor de classe 3 avec ischémie documentée en rapport avec une occlusion coronaire chronique de la circonflexe (figure 4). Après franchissement de l’occlusion par un guide dédié aux occlusions chroniques, il nous a été impossible, là aussi malgré un bon support, de franchir la lésion avec le ballon. Le premier guide a donc été retiré, le franchissement d’un microcathéter dans le but d’un échange de guides ayant lui aussi été impossible. Puis la lésion a de nouveau été franchie, cette fois avec le Rota-Wire®, qui a permis une AR et le succès de la procédure.
Figure 4. A : occlusion chronique de la circonflexe moyenne ; B : passage d’un guide Miracle® à travers l’occlusion, échec de franchissement d’un ballon d’angioplastie ; C : Rotablator®, avec deux fraises de 1,25 puis 1,5 mm ; D : contrôle final après implantation d’un DES.
Conclusion
L’AR, effectuée grâce au système Rotablator®, est une technique d’angioplastie qui demande un apprentissage spécifique. Malgré l’absence de bénéfice clinique à long terme en cas d’utilisation systématique, elle n’en demeure pas moins un outil irremplaçable qui permet de traiter des lésions inaccessibles à l’angioplastie.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :