Publié le 14 oct 2015Lecture 15 min
Fonction rénale : quel tri faire entre les différentes formules du DFG ?
C. CARTERY, Service Néphrologie et Dialyses, Hôpital Tenon, Paris
En France, 60 000 individus sont atteints d’insuffisance rénale terminale (IRT), dont 35 000 ont recours à une méthode d’épuration extra-rénale (hémodialyse ou dialyse péritonéale). La maladie rénale chronique (MRC) augmente le risque de mortalité globale, de morbidité cardiovasculaire, d’hospitalisation, et a un impact négatif sur la qualité de vie personnelle, familiale et socioprofessionnelle. L’épuration extra-rénale (EER) représente 2 % des dépenses de santé et la MRC est donc considérée comme un problème de santé publique.
L’insuffisance rénale reste asymptomatique jusqu’à un stade avancé, et elle est encore trop souvent découverte au stade terminal (IRT). Or, il est possible de prévenir l’évolution vers l’IRT, à condition d’intervenir à un stade précoce.
La cible de cette prévention est large en raison du nombre croissant de patients, principalement âgés, atteints par la maladie rénale chronique dans les pays occidentaux. La prévalence de la MRC, définie par le débit de filtration glomérulaire (DFG), atteint 10 à 15 % dans de nombreux pays(1). En fonction de la formule d’estimation du DFG utilisée, la prévalence varie. Ainsi, avec l’arrivée de la formule CKDEPI, la prévalence de la MRC aux États-Unis a diminué de 3,2 millions de personnes(2). Ces données soulignent l’importance d’évaluer précisément le DFG.
Rappels de physiopathologie rénale
Les fonctions du rein sont multiples : filtration, équilibre hydro-électrolytique, et sécrétion hormonale. En cas de maladie rénale chronique, on observe une défaillance de ces trois fonctions.
Le dosage de la créatinine plasmatique est un très mauvais marqueur de défaillance rénale puisque la créatininémie ne s’élève que lorsque la baisse de DFG dépasse 50 %(3). La filtration, estimée par le calcul du débit de filtration glomérulaire (DFG), est considérée comme étant le meilleur indice de la fonction rénale. En situation normale, le débit de filtration glomérulaire est de 120 ml/min (180 l/24 h). Il existe néanmoins une diminution physiologique du DFG avec l’âge. En effet, après 40 ans, le DFG baisse de 0,5 à 1 ml/min par année(4). Ainsi, les patients de plus de 70 ans ayant un DFG stable compris entre 59 et 45 ml/min/1,73 m2, ne devraient pas être considérés comme ayant une MRC(5).
Tous les patients ayant un DFG inférieur à 60 ml/min/1,73 m2 pendant plus de 3 mois sont considérés comme ayant une maladie rénale chronique selon les recommandations américaines KDOQI/CKD (pour Kidney Disease/Improving Global Outcomes). La MRC est classée en 5 stades (tableau) selon la valeur du DFG(6). Il ne faut pas oublier que la mesure du débit de protéinurie est également indispensable pour guider le traitement et surveiller la progression de la MRC. Cette classification permet un dépistage de la MRC et a abouti à des recommandations de prise en charge propres à chaque stade. Une détermination aussi précise que possible du DFG occupe donc une place primordiale dans la prise en charge des patients.
Le DFG est défini par la clairance d’une substance x. Cette substance x doit être éliminée par le rein, filtrée librement par le glomérule (faible poids moléculaire, non liée aux protéines), et non sécrétée ni réabsorbée par le tubule. De plus, la sub stance ne doit pas être synthétisée, transportée, ou métabolisée par le rein. La clairance est le volume de plasma totalement épuré de cette substance par unité de temps. Le résultat doit être ramené à une surface corporelle de 1,73 m2 et s’exprime donc en ml/min/1,73 m2.
Mesure du DFG par traceurs exogènes ou endogènes
Traceurs exogènes
Le « gold standard » pour la détermination du DFG est sa mesure directe, grâce à l’utilisation d’un traceur exogène ayant les caractéristiques de x. Plusieurs traceurs peuvent être utilisés : Inuline, 51Chrome EDTA, Iohexol, Iothalamate. L’inuline reste la méthode de référence dans les recommandations américaines(7). La situation idéale, mais utopique, serait de mesurer le DFG par une méthode de référence chez tous les patients pour évaluer la fonction rénale et adapter au mieux la dose du médicament. Ces méthodes nécessitent néanmoins de nombreux prélèvements de sang et/ou d’urines dans un laboratoire spécialisé. En raison de sa lourdeur et de son coût, la mesure directe du DFG est donc réservée à des indications particulières, lorsque le patient a un morphotype atypique rendant l’estimation du DFG difficile : amyotrophie massive, para- ou tétraplégie, myopathie, dénutrition grave, obésité morbide, régime végétarien, gigantisme ou nanisme, etc.
Traceurs endogènes
Devant les obstacles à la mesure du DFG par des traceurs exogènes, des alternatives ont été développées utilisant des traceurs endogènes. Deux molécules ont été proposées : l’urée et la créatinine. La clairance de l’urée a été abandonnée en raison des variations de mesures dépendant des apports protidiques et de l’hydratation.
La mesure de la clairance de la créatinine a été utilisée en routine pendant plus de 40 ans, or elle est un marqueur imparfait du DFG pour de multiples raisons. En premier lieu, la mesure est tributaire de la qualité du recueil d’urine. Ensuite, la créatinine n’est pas une substance idéale pour déterminer la clairance : elle a une élimination extra-rénale en cas d’IRC sévère. De plus, elle surestime systématiquement le DFG quelle que soit la valeur de la fonction rénale en raison de sa sécrétion tubulaire(8). En cas de fonction rénale normale, la part tubulaire de son excrétion est faible (de l’ordre de 10 %), mais elle dépasse 50 % au stade terminal de l’insuffisance rénale terminale. Par ailleurs, certains médicaments inhibent sa sécrétion tubulaire (le triméthoprime et la cimétidine), alors que d’autres augmentent sa production (les fibrates et l’hormone de croissance). Enfin, la production de créatinine est aussi corrélée au volume des masses musculaires et aux apports alimentaires en viande. La clairance de la créatinine est donc un très mauvais reflet du DFG. Effectuée dans les meilleures conditions, elle conduit à méconnaître environ 30 % des insuffisances rénales(9).
D’autres traceurs endogènes de filtration glomérulaire ont été proposés. Au premier rang de ceux-ci, la cystatine C a donné naissance à plusieurs formules de DFG estimé. Certains proposent également d’intégrer deux traceurs dans la même équation afin de réduire la variance du modèle(10). Ces formules ne sont pas encore utilisées en routine.
Formules d’estimation du DFG
En pratique, le recours à des formules d’estimation du DFG est nécessaire. Il a donc été mis au point des formules permettant d’estimer le DFG à partir de la seule concentration plasmatique de la créatinine et de différentes données phénotypiques des individus. La performance d’une formule est jugée sur ses caractéristiques incluant : le biais, la précision, et l’exactitude par rapport à une mesure de référence. Mais le choix d’une formule d’estimation du DFG n’est pas exclusivement basé sur ses performances intrinsèques à estimer au mieux un DFG mesuré (DFGm) par une méthode de référence, mais aussi sur sa capacité à prédire la mortalité ou l’arrivée à un stade terminal de la MRC(11).
La formule de Cockcroft et Gault
La première formule proposée a été celle de Cockcroft et Gault (CG) qui prend en compte l’âge, le sexe et le poids(12). Elle est d’emploi facile et a donc rencontré un grand succès. La formule CG a été publiée en 1976 et établie à partir de l’étude d’une cohorte de 236 malades canadiens de sexe masculin. La formule de Cockcroft et Gault estime non pas le DFG (en ml/min/1,73 m2), mais la clairance de la créatinine sur les urines de 24 heures (en ml/min). La clairance des urines de 24 heures n’est cependant plus recommandée pour estimer le DFG.
Plusieurs limites ont été avancées. La formule CG surestime le DFG des individus âgés de moins de 65 ans ou dont l’indice de masse corporelle (IMC) est supérieur à 30 kg/m2 ou inférieur à 18,5 kg/m2. Elle le sous-estime largement si l’âge est supérieur à 65 ans(13). Les sujets âgés sont alors crédités d’une IRC qui n’existe pas. Ils risquent d’être soumis à des explorations, voire des traitements onéreux et inutiles. Malgré toutes les limites mentionnées, la formule CG reste une bonne option chez les patients âgés et ayant un BMI bas(14).
Il persiste un débat sur l’utilité de cette formule dans le champ spécifique de l’adaptation posologique. L’immense majorité des publications sur l’adaptation posologique des médicaments ont, de fait, utilisé la formule CG ou la clairance de créatinine. Par ailleurs, la variable « poids » est présente dans la formule CG, ce qui peut être un avantage au niveau pharmacocinétique, le poids étant une estimation du volume de distribution du médicament.
La formule du MDRD
Plus tard a été proposée la formule du Modification of Diet in Renal Diseases (MDRD) qui, dans sa version simplifiée, prend en compte l’âge, le sexe, un facteur ethnique et, dans sa version originale, l’urée sanguine et l’albumine sérique(15). La formule du MDRD a été publiée en 1999 et établie à partir d’une population de 1 628 malades caucasiens et afro-américains résidant aux États-Unis dont l’âge moyen était de 50,6 ± 12,7 ans. Les valeurs de référence étaient des mesures de DFG par clairance urinaire du 125I-iothalamate. L’estimation du DFG par la formule MDRD nécessite l’emploi d’un calculateur en accès libre sur Internet ou de calculettes individuelles.
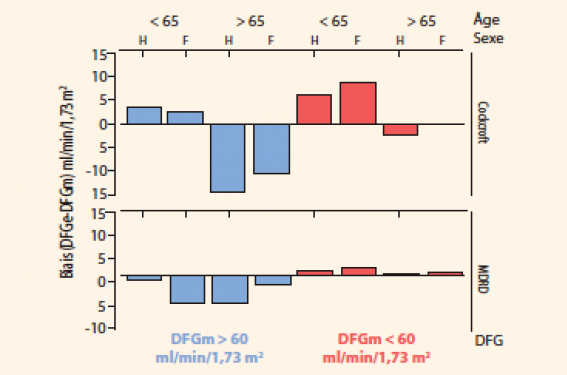
La formule MDRD surestime le DFG si l’IMC est inférieur à 18,5 kg/m2 et le sous-estime chez les femmes âgées de moins de 65 ans. Dans la plupart des situations, la formule MDRD a une meilleure précision que la formule CG. La formule MDRD permet une estimation nettement plus fiable du DFG dans la population âgée. À l’opposé, la formule MDRD sous-estime régulièrement le DFG des sujets à faible risque d’insuffisance rénale (donneurs de rein) ou diabétiques dont le DFG est dans les valeurs hautes de la normale (stade d’hyperfiltration)(13) (figure). Ces biais sont peut-être à l’origine d’une surestimation de la prévalence de la maladie rénale chronique dans les études épidémiologiques.
Biais d’estimation moyens observés pour les formules de Cockcroft et Gault et MDRD abrégé par rapport au DFG mesuré. Adapté de(13).
La formule CKD-EPI
Pour tenter d’atténuer les imperfections des formules CG et MDRD, une troisième a été publiée en 2009, le CKD-EPI (Chronic Kidney Disease EPIdemiology collaboration), qui utilise les mêmes variables que la formule MDRD(2).
Les performances de cette formule sont meilleures pour des valeurs normales ou élevées de DFG (au-delà de 90 l/min/ 1,73 m2) mais comparable à MDRD pour les stades 3 à 5 de la MRC(14).
L’équation CKD-EPI (comme les autres modes d’estimation du DFG) n’est pas encore complètement validée dans certaines populations de patients : patients de type non caucasien (le facteur de correction ethnique fourni pour l’équation n’est validé que pour la population afro-américaine) ; patients âgés de plus de 75 ans ; patients de poids extrême ou dont la masse musculaire est élevée ou faible ; patients dénutris ou ayant une alimentation pauvre en protéines animales ; 3e secteur. Chez ces sujets, les résultats sont à interpréter avec précaution, en les confrontant avec la clinique et avec le résultat des autres examens.
Utilisation pratique des formules
(encadré)
Pour estimer le DFG à partir de la créatininémie par l’équation CKD-EPI ou MDRD, on peut utiliser le calculateur de la Société française de néphrologie, accessible en ligne : http://www.socnephrologie. org/eservice/calcul/ eDFG.htm. Le résultat, étant déjà indexé à une surface corporelle de 1,73 m2, ne doit pas être réadapté à la surface corporelle du patient. Cette indexation a pour objectif la normalisation par la masse néphronique constitutionnelle et permet ainsi la comparaison du DFG entre personnes de gabarits différents. Les populations à partir desquelles ces formules ont été élaborées ne recouvrent pas la totalité des variables susceptibles de modifier la relation entre le taux de la créatinine sérique et le DFG (DFG normal ou augmenté ou très altéré, diabète, grand âge, greffe rénale, origine ethnique, importance des masses musculaires, etc.) et il est raisonnable de considérer qu’aucune formule ne permet d’estimer à coup sûr le DFG de façon précise dans toutes les situations cliniques.
La performance de ces formules dépend beaucoup de l’âge et du DFG. De manière générale, les formules d’estimation du DFG font que les patients âgés et les patients obèses ont un DFG plus bas(14). Chez l’adolescent et l’adulte jeune, les formules habituelles surestiment le DFG mesuré avec la clairance de l’inuline. Le nombre de jeunes patients étant très limité dans les études ayant abouti aux formules de MDRD et CKD-EPI, ces deux formules ne sont pas recommandées avant 18 ans. La formule de Schwartz 2009 semble préférable(16). Chez le diabétique, les formules semblent incapables d’identifier les patients hyperfiltrants, de monitorer la progression de la maladie rénale, et donc de juger de la réponse au traitement néphroprotecteur. Le DFG est sous-estimé par toutes les formules (MDRD et CKD-EPI). De même, le déclin de la fonction rénale est sous-estimé par les formules, quel que soit le stade de la MRC(17).
Dosage de la créatinine sérique
La créatinine sérique est la variable déterminante dans les formules CG, MDRD et CKDEPI. Le dosage de la créatinine sérique revêt donc une importance primordiale(18). La mesure de la créatinine par méthode colorimétrique Jaffé sous-estime le DFG en dosant des chromogènes autres que la créatinine rendant un résultat qui surestime la créatinine(19).
Le processus de standardisation des différentes méthodes de mesure de la créatinine est assez récent. Pour la HAS, la fiabilité des méthodes enzymatiques traçables à la spectrométrie de masse avec dilution isotopique (IDMS) est meilleure quel que soit le niveau de la créatininémie. Ces méthodes sont à utiliser dans toutes les situations cliniques.
La formule de Cockcroft a été établie à partir d’une créatinine sérique mesurée par méthode Jaffé. L’équation n’a pas été réévaluée depuis la standardisation du dosage de la créatinine, et par conséquent, l’estimation obtenue par la formule de Cockcroft il y a 30 ans à partir d’un échantillon sérique peut être très différente de celle obtenue avec un dosage de créatininémie effectué sur le même échantillon de nos jours. Seules les formules les plus récentes, à savoir les formules MDRD et CKD-EPI ont été développées pour être utilisées avec une créatinine calibrée dite « IDMS traceable ».
Recommandations pour évaluer la MRC
Toutes les sociétés savantes s’accordent à dire que pour diagnostiquer une insuffisance rénale chronique chez l’adulte, la fonction rénale doit être évaluée à partir de la créatininémie, par l’estimation du DFG (MDRD ou CKD-EPI), et non plus par l’estimation de la clairance de la créatinine (CG).
Les KDIGO favorisent l’utilisation de la formule CKD-EPI en lieu et place de la formule MDRD en raison d’une meilleure performance pour prédire la mortalité alors que sa performance intrinsèque pour estimer le DFG en cas de MRC est sensiblement identique à celles de MDRD (voire inférieure dans certaines sous-populations).
L’estimation du degré d’insuffisance rénale par la détermination du DFG a fait l’objet de recommandations par la HAS en 2012. L’équation CKD-EPI pour estimer le DFG et la méthode enzymatique standardisée IDMS pour doser la créatinine, qui sont les procédés les plus performants, sont à utiliser.
Recommandations pour adapter les posologies médicamenteuses
À ce jour, il n’y a aucune étude prospective comparant les doses, les effets secondaires, les éventuels échecs thérapeutiques en fonction de la formule utilisée. Le problème du choix de l’équation se pose principalement chez les patients qui présenteront des DFG estimés très différents selon que Cockcroft ou CKD-EPI est utilisé. D’une manière générale, le profil type du patient pour lequel Cockcroft sous-estime CKDEPI est le suivant : une créatinine proche de la normale et un patient maigre. Le profil type du patient pour lequel Cockcroft surestime CKD-EPI est le suivant : le patient en surcharge pondérale.
Jusqu’en 2008, la formule de Cockcroft était encore la seule à être recommandée par la Food and Drug Administration (FDA) pour les études visant à déterminer les éventuelles adaptations posologiques d’un nouveau médicament en fonction du DFG. Depuis cette date, la FDA accepte l’utilisation de MDRD dans ce type d’étude. L’European Medicines Agency (EMA) est sur une ligne similaire, ne faisant pas de choix clair en faveur d’une formule d’estimation. Les KDIGO ont une position plus tranchée en faveur du CKD-EPI et recommandent implicitement de ne pas utiliser la formule de Cockcroft pour adapter les posologies d’un médicament selon la fonction rénale. La position française telle qu’exprimée par l’assurance maladie dans la version 2014 de la nomenclature des actes de biologie médicale (http://www.codage.ext.cnamts. fr) est celle d’un compromis : utilisation de l’équation CKDEPI pour l’évaluation de la fonction rénale dans le cadre du diagnostic et du suivi de la maladie rénale chronique OU utilisation de la formule de Cockcroft si l’évaluation de la fonction rénale est demandée dans le cadred’une adaptation posologique.
Dans le cadre de l’adaptation individuelle des posologies médicamenteuses, l’indexation peut être remise en question(20). En effet, la posologie d’un médicament doit logiquement être adaptée au DFG du patient, et non pas au DFG que ce patient aurait s’il avait un gabarit correspondant à une surface corporelle (SC) de 1,73 m2. Ceci pourrait aboutir notamment à une sous-exposition au médicament chez le sujet obèse et à une surexposition chez le sujet très maigre. L’utilisation de DFG non indexé est d’ailleurs recommandée par les KDIGO 2012(21) mais aussi par la FDA et l’EMA. Un consensus assez large semble donc se dégager en faveur de l’utilisation d’une valeur de DFG non indexée pour l’adaptation posologique. Aucune étude n’a cependant montré la supériorité d’une stratégie par rapport à l’autre en pratique clinique. Les calculateurs MDRD ou CKDEPI donnant un résultat où l’indexation à la SC est intégrée, il serait nécessaire de désindexer les résultats obtenus par la valeur de SC individuelle. Cette problématique de la désindexation du DFG n’a théoriquement de justification que pour les patients avec une SC très différente de la normalité, à savoir les sujets obèses ou, à l’inverse, les sujets très maigres.
Problématique chez le sujet âgé
La performance de MDRD et CKD-EPI a été étudiée dans la population âgée. Pour la population âgée ayant une fonction rénale normale (c’est moins le cas en cas de MRC), ces deux formules ont tendance à surestimer le DFG vrai, donnant un résultat plus haut par rapport à Cockcroft. Certains gériatres proposent donc d’adapter les doses de médicament en fonction du Cockcroft sur la base d’un principe de précaution, pour éviter les effets indésirables d’un surdosage. Néanmoins, une sous-estimation erronée du DFG peut dans certaines situations constituer une perte de chance pour le patient, en contre-indiquant abusivement un médicament potentiellement bénéfique. L’intérêt d’équations spécifiquement développées à partir d’une population gériatrique comme la formule BIS (pour « Berlin Initiative Study ») pourrait avoir un intérêt dans le contexte de l’adaptation posologique(22).
Compte tenu de la difficulté d’évaluer correctement le DFG chez la personne âgée (risque de sur- ou sous-estimation très difficile à anticiper à l’échelon individuel) et de la prévalence très élevée d’accidents iatrogènes dans cette population, on recommande l’utilisation de médicaments dont la concentration sanguine ou l’effet est facilement évaluable. En l’absence d’une telle alternative thérapeutique, le recours à une méthode de mesure directe du DFG est recommandé.
En pratique
Les nouvelles formules d’estimation du DFG, MDRD et CKD-EPI, sont actuellement utilisées pour dépister et surveiller la MRC. Comparativement à Cockcroft, elles ont l’avantage d’avoir été développées puis validées sur des milliers de patients. Elles n’intègrent pas le poids, ce qui permet au laboratoire de rendre un résultat de DFG estimé automatiquement. Enfin, ces formules, contrairement à Cockcroft, estiment un DFG réellement mesuré. Selon les recommandations de la HAS, il faut privilégier l’équation CKD-EPI pour le diagnostic et l’évaluation de la sévérité de la MRC, ainsi que pour l’adaptation posologique.
Le recours à un DFG désindexé pour la SC est recommandé dans le contexte de l’adaptation posologique, en cas de morphotype particulier. L’argument du « principe de précaution » chez la personne âgée de la sousestimation du DFG par la formule de Cockcroft ne peut être retenu, car contredit notamment en cas de poids « normal » ou excessif. Il faut néanmoins noter que des études prospectives, randomisées, avec des critères de jugements cliniques « durs » sont probablement nécessaires chez la personne âgée pour définitivement valider le choix d’une équation par rapport à une autre.
Il est illusoire d’espérer une précision absolue des formules d’estimation, basées sur une approche probabiliste. Aucune formule n’est complètement sensible ni spécifique pour détecter la MRC. Les utilisateurs de ces formules doivent donc garder un esprit critique pour leur interprétation en fonction des données cliniques notamment.
Lorsque les traceurs endogènes, comme la créatinine, apparaissent pris en défaut par les circonstances cliniques (poids extrême, 3e secteur, âge extrême), il est utile de savoir poser l’indication à une mesure du DFG par une technique de référence faisant appel à un traceur exogène.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :