Valvulopathies
Publié le 14 mar 2016Lecture 9 min
Traitement percutané : la fin des valves mécaniques ?
D. HIMBERT, CHU Bichat-Claude Bernard, AP-HP, Paris
JESFC
Au cours des deux dernières décennies, l’utilisation des prothèses mécaniques a régulièrement diminué au profit de celle des bioprothèses. La première explication tient à l’évolution des valvulopathies, moins souvent rhumatismales et plus souvent dégénératives, atteignant des sujets de plus en plus âgés. La seconde est liée aux progrès technologiques récents, avec l’augmentation de la durabilité des bioprothèses et surtout les perspectives offertes par les implantations valvulaires percutanées et en particulier la possibilité d’implantations valve-in-valve.
Les recommandations actuelles
Elles donnent trois critères de décision principaux pour le choix entre prothèses mécaniques et biologiques :
La préférence du patient correctement informé
C’est la première recommandation et la seule de classe I (niveau C). Cette préférence est probablement mieux prise en compte actuellement qu’il y a 10 ou 20 ans et explique en partie l’utilisation croissante des bioprothèses. En effet, les inconvénients des prothèses mécaniques liés à l’anticoagulation au long cours (restriction des activités physiques et professionnelles, des voyages, etc.) avec leur impact psychologique et plus globalement leur retentissement sur la façon de vivre poussent de plus en plus de patients à choisir une bioprothèse.
Le niveau de risque d’une future réopération
Une réopération estimée à haut risque doit favoriser le choix d’une prothèse mécanique (IIa, C). Les progrès chirurgicaux des dernières décennies ont diminué ce risque, ce qui explique là encore que de plus en plus de patients acceptent cette perspective et optent pour une bioprothèse.
L’âge des patients
La zone frontière entre prothèses mécaniques et bioprothèses est de 60 à 65 ans en position aortique et de 65 à 70 ans en position mitrale (IIa, C). De plus en plus de patients sont opérés au-delà de ces âges et reçoivent donc des bioprothèses.
Tout ceci explique que tous les registres nationaux et internationaux montrent, depuis la fin des années 90, une diminution régulière de l’utilisation des prothèses mécaniques au profit des bioprothèses. Cette tendance s’est accentuée et accélérée depuis la diffusion du TAVI à partir de 2006-2007. Aujourd’hui, en Allemagne, les prothèses mécaniques représentent à peine 10 % des implantations, les 90 % restants se partageant entre prothèses biologiques chirurgicales et percutanées (figure 1).
Figure 1. Évolution des remplacements valvulaires aortiques isolés en Allemagne de 1994 à 2013.
La littérature récente chez les sujets « jeunes » (50-69 ans)
Elle porte sur le seul débat encore utile puisque, chez les sujets plus âgés, l’utilisation des bioprothèses est devenue indiscutable. Elle comporte essentiellement une étude prospective randomisée(1), une dizaine de comparaisons rétrospectives non randomisées, dont les 4 plus importantes sont les plus récentes, parues ces 2 dernières années dans le JAMA(2-4) et l’Eur Heart J(5), et des registres prospectifs avec des suivis prolongés de volumineuses cohortes, dont 2 sont français, provenant des équipes de Rennes(6) et de Tours(7). Toutes ces études aboutissent globalement aux mêmes conclusions.
L’espérance de vie à long terme est identique avec les prothèses mécaniques et les bioprothèses
C’est vrai pour la survie globale après remplacement valvulaire aortique dans l’étude randomisée de Stassano et dans le registre de Chiang (figure 2). Dans le registre suédois de Glaser, la survie cardiovasculaire est identique avec les 2 types de prothèses, mais la survie globale meilleure après prothèse mécanique (figure 3). Cette contradiction s’explique par le fait que l’appariement des patients comparés n’a pas permis de compenser entièrement le profil de risque plus sévère de ceux recevant une bioprothèse, responsable d’une mortalité non cardiovasculaire plus élevée que chez les patients éligibles pour une prothèse mécanique. Après remplacement valvulaire mitral, la survie globale à 15 ans est identique pour les 2 types de prothèses(4) (figure 4).
Figure 2. Survie à 15 ans après remplacement valvulaire aortique par prothèse mécanique ou bioprothèse chez des patients âgés de 50 à 69 ans.
Figure 3. Registre suédois portant sur la survie à 15 ans après remplacement valvulaire aortique par prothèse mécanique ou bioprothèse chez des patients âgés de 50 à 69 ans.
Figure 4. Survie à 15 ans après remplacement valvulaire mitral par prothèse mécanique ou bioprothèse chez des patients âgés de 50 à 69 ans.
Le risque de réopération est plus important avec les bioprothèses et celui d’accident hémorragique grave avec les prothèses mécaniques
C’est une constante dans toutes les études publiées. Les registres prospectifs comportant des suivis prolongés permettent de quantifier ce risque et de répondre de façon précise et concrète aux questions des patients. Par exemple, dans le registre de Ruggieri, après remplacement valvulaire aortique par une prothèse de Carpentier Edwards, un patient opéré à l’âge de 50 ans a un risque de réopération à 20 ans de 45 %.
Le risque d’accident vasculaire cérébral est plus important avec les prothèses mécaniques qu’avec les bioprothèses en position mitrale
(figure 5)
Figure 5. Risque d’accident vasculaire cérébral après remplacement valvulaire mitral par prothèse mécanique ou bioprothèse chez des patients âgés de 50 à 69 ans.
Cette observation du registre de Chikwe est évidemment fondamentale à faire connaître aux patients et à prendre en compte dans le choix de la prothèse.
L’apport des implantations valvulaires percutanées
Le développement du TAVI à partir de la fin des années 2000 est venu renforcer la tendance préexistante en faveur des bioprothèses. Il a permis à de nombreux patients à haut risque, auparavant récusés, d’être discutés en milieu hospitalier par une Heart team et d’être traités par voie percutanée mais aussi pour certains chirurgicalement. Surtout, il est rapidement apparu que les patients âgés atteints de dégénérescence de leur bioprothèse aortique constituaient une niche clinique très intéressante pour le TAVI, les implantations par cathéter valve-in-valve leur permettant d’éviter une chirurgie redux à haut risque (figure 6). Plus encore, la perspective de pouvoir remplacer une réopération chirurgicale par une simple intervention percutanée a incité à proposer les bioprothèses à des patients plus jeunes.
Figure 6. Implantation valvulaire aortique par cathéter valve-in-valve. À gauche : SAPIEN. À droite : CoreValve.
L’expérience actuelle
Les données concernant le valve-in-valve en position aortique sont encore jeunes et le recul faible, mais elles sont déjà solides. Plusieurs registres multicentriques nationaux et internationaux portant sur plus de 1 000 patients sont en cours, avec des résultats encourageants. Le registre PARTNER II Valve in Valve a inclus 200 patients à haut risque. Leur mortalité à 1 mois est de 4 % et à 1 an de 13 % et se compare donc favorablement aux résultats du TAVI sur valves natives (figure 7). On observe une courbe d’apprentissage avec une amélioration des résultats obtenus chez les 100 derniers patients par rapport aux 100 premiers. Ce registre confirme que le valve-in-valve aortique offre une alternative thérapeutique favorable par rapport à la chirurgie redux. Les données concernant le valve-in-valve en position mitrale sont moins nombreuses mais également encourageantes. La voie d’abord la plus souvent utilisée est la voie transapicale. L’expérience de Bichat porte sur une quarantaine de patients traités par valve-in-valve mitral par voie transseptale entre 2011 et 2015 (figure 8). Tous ces patients étaient à très haut risque (EuroSCORE logistique : 30 %, EuroSCORE II : 15 %), en classe III ou IV de la NYHA, certains en choc cardiogénique. La survie à 1 mois est de 92 %. La figure 8 montre l’amélioration de l’hémodynamique, avec une diminution par 2 du gradient transprothétique mitral, et de l’état fonctionnel des patients, 90 % d’entre eux restant en classe I ou II de la NYHA au dernier suivi (figure 9).
Figure 7. Registre PARTNER II Valve in Valve. En haut : survie globale à 1 mois et 1 an après TAVI valve-in-valve. En bas : survie à 1 an en fonction du diamètre de la bioprothèse chirurgicale.
Figure 8. Implantation valve-in-valve mitrale par voie transseptale. À gauche : déploiement de la prothèse SAPIEN. À droite : après implantation.
Figure 9. Résultats après implantation valve-in-valve mitrale par voie transseptale. À gauche : résultats hémodynamiques. À droite : résultats fonctionnels.
Les améliorations nécessaires
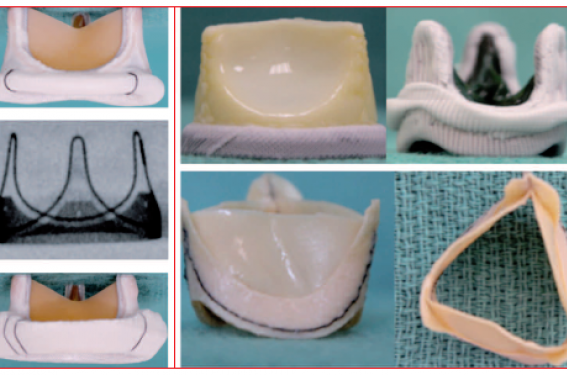
La facilité, le risque et les résultats des implantations valve-in-valve par voie percutanée dépendent en grande partie du type de bioprothèse chirurgicale en place. Certaines précautions systématiques doivent donc être prises lors de l’intervention chirurgicale initiale dans l’optique d’un futur valve-in-valve. La première, simple, est de savoir choisir les « bonnes » bioprothèses, c’est-à-dire celles qui ont fait la preuve de leur durabilité et qui se prêteront facilement et sans risque à la future implantation. Leurs principales caractéristiques sont :
- d’être entièrement radioopaques (anneau et montants métalliques) ;
- d’avoir des feuillets péricardiques suturés à l’intérieur de ces montants ;
- d’avoir des feuillets courts, ne montant pas trop haut dans la racine de l’aorte.
Ces caractéristiques facilitent l’implantation et évitent le risque d’obstruction coronaire. À l’inverse, il faut donc éviter les prothèses stentées radiotransparentes, celles dont les feuillets sont cousus à l’extérieur des montants, d’autant plus qu’ils sont longs, augmentant le risque d’obstruction coronaire, et toutes les prothèses stentless, qui cumulent tous les inconvénients (figure 10). La seconde condition d’un futur valve-in-valve cliniquement et durablement efficace est de mettre en place la bioprothèse chirurgicale la plus large possible, car tous les registres montrent que la survie après valve-in-valve est d’autant meilleure que la bioprothèse initiale est plus large (figure 7, à droite). Dans certains cas, en fonction du risque opératoire, une plastie d’élargissement pourrait se discuter chez les patients ayant de petits anneaux aortiques.
Figure 10. Choix d’une bioprothèse chirurgicale dans l’optique d’un futur valve-in-valve. À gauche : bioprothèses à privilégier. À droite : bioprothèses à éviter.
L’avenir
Les implantations valvulaires percutanées bénéficient de progrès technologiques extrêmement rapides. La prochaine décennie va voir se développer des dispositifs spécifiquement dédiés aux implantations valve-in-valve et des valves recapturables et repositionnables, permettant d’assurer des implantations parfaites, sans fuite périprothétique ni risque d’obstruction coronaire. La voie fémorale va continuer à augmenter et les interventions à se simplifier, pour aboutir à des procédures stent like, avec des durées d’hospitalisation n’excédant pas 2 à 3 jours.
Il n’y a pas aujourd’hui d’alerte sur la survenue de dégénérescence de prothèses percutanées, mais les suivis les plus longs restent inférieurs à 10 ans. Lorsque cela arrivera, il sera simple pour l’immense majorité des patients de réaliser l’implantation d’une seconde prothèse percutanée à l’intérieur de la première. Et à plus long terme, il est raisonnable d’envisager l’éventualité d’implantations valve-in-valve-in-valve chez certains patients sélectionnés. Ce type de procédure a déjà été réalisé, sans obstacle technique particulier et avec un bon résultat clinique et hémodynamique à moyen terme (figure 11).
Figure 11. Implantation valve-in-valve-in-valve en position aortique. *Bioprothèse Medtronic Freestyle posée chirurgicalement en 2002. Flèche blanche : 1re CoreValve implantée en 2012 pour dégénérescence de la Medtronic Freestyle (valve-in-valve). Flèche bleue : 2e CoreValve implantée en 2013 pour insuffisance aortique massive sur endocardite aiguë (valve-in-valve-in-valve). Nguyen et al. Cathet Cardiovasc Interv 2015 ; 86 : 200 ‐4.
Conclusion
L’utilisation croissante des techniques d’implantation valvulaire percutanée permet à de plus en plus de patients d’être traités efficacement, malgré des valvulopathies de plus en plus sévères. Ces progrès s’accompagnent d’une diminution continue de l’utilisation des prothèses mécaniques au profit des bioprothèses chirurgicales et percutanées, qui se partagent aujourd’hui plus de 90 % du marché.
En pratique
Chez les sujets jeunes, la survie à long terme est identique après remplacement valvulaire par prothèse mécanique ou bioprothèse.
Le risque de complication hémorragique grave est plus élevé chez les porteurs de prothèses mécaniques.
Le risque d’accident vasculaire cérébral est plus élevé chez les porteurs de prothèses mécaniques en position mitrale.
La qualité de vie est meilleure chez les porteurs de bioprothèses.
Les implantations percutanées valve-in-valve sont une alternative bénéfique à la chirurgie redux pour les dégénérescences de bioprothèses chirurgicales.
L’utilisation croissante des techniques percutanées, parallèle à la diminution de celle des prothèses mécaniques, permet d’offrir un traitement efficace à un plus grand nombre de patients souffrant de valvulopathies plus sévères.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :