Publié le 15 mai 2023Lecture 7 min
Hypertension pulmonaire en échocardiographie
Raphaël COHEN, unité de recherche INSERM U9970, mécanisme immuno-métabolique des maladies cardiovasculaires
L’échographie Doppler est le premier examen non invasif à disposition du cardiologue pour évoquer le diagnostic d’hypertension pulmonaire (HTP). De plus, l’échographie Doppler permet dans certains cas le diagnostic étiologique, d’étudier son évolution avec ou sans traitement et d’en stratifier le risque. En effet, l’étude morphologique et fonctionnelle des cavités cardiaques, mais aussi des valves, permet une approche indirecte, de l’hémodynamique cardiaque.
Diagnostic positif : évaluation de la pression artérielle pulmonaire
Flux d’insuffisance tricuspide (IT)
Bien que le cathétérisme droit soit l’examen de référence pour faire le diagnostic d’HTP, le Doppler cardiaque permet d’approcher la PAPs grâce au flux d’insuffisance tricuspide (IT) et l’application de l’équation de Bernoulli simplifiée.
Cette mesure se fait en multipliant les fenêtres d’exploration et donc les incidences (parasternale grand axe modifiée dégageant les cavités droites, petit axe centré sur la valve tricuspide, apicale 4 cavités) en Doppler continu couplé à l’imagerie et avec une sonde Pedoff en cas de signal de qualité insuffisante.
Principe de la mesure :
– en Doppler continu, mesure de la vitesse maximale du flux d’IT pour en déduire un gradient de pression entre le VD et l’oreillette droite (OD) (réglage au maximum des filtres de paroi) ;
– à ce gradient VD - OD, on ajoute la pression dans l’OD (POD) ;
– la POD estimée à partir de la détermination du diamètre et de la compliance au cours du cycle respiratoire de la VCI (figure 1, tableau 1).
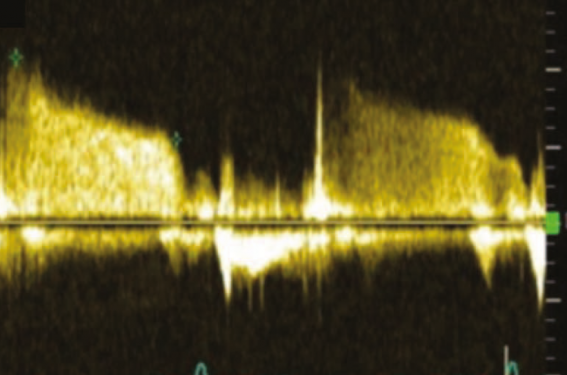
Figure 1. Flux d’insuffisance pulmonaire permettant de mesurer PAPm et PAPd.
Point clé : cette mesure n’est pas valable en cas :
– d’IT laminaire ;
– de sténose pulmonaire (car dans ce cas la pression télésystolique dans le VD sera différente de la PAPs) ;
– de shunts intra- ou extra-cardiaques.
Par ailleurs :
– l’absence d’IT n’élimine pas le diagnostic d’HTP et incite à multiplier les incidences d’exploration, à utiliser la sonde Pedoff et à rechercher systématiquement un flux d’insuffisance pulmonaire, reflet des pressions pulmonaires diastolique et moyenne ;
– en cas de fibrillation atriale : nécessité de moyenner les mesures sur 10 cycles.
Ainsi, un flux d’IT véloce (> 3,4 m/s) sera très évocateur d’un diagnostic d’HTP (figure 2, tableau 2).
Figure 2. L’algorithme de l’ESC permet d’évaluer la probabilité de présenter une HTP.
Figure 3. (A) Aspect du flux systolique pulmonaire en Doppler pulsé avec présence d’une encoche
Flux d’insuffisance pulmonaire (IP)
Le flux pulmonaire doit être systématiquement enregistré en Doppler pulsé (approche de l’évaluation des résistances vasculaires pulmonaires, voir ci-dessous).
En Doppler continu, le flux d’IP permet une estimation des pressions pulmonaires diastolique (PAPd) et moyenne (PAPm). Ainsi, la PAPm est déterminée par la vitesse protodiastolique de l’IP : PAPm (4[Vproto IP]2 + POD).
La PAPd est déterminée par la vitesse télédiastolique de l’IP : PAPd = (4[Vtele IP]2 + POD). De manière indirecte, le flux d’IP permet également une estimation de la PAPs selon la formule : PAPS = 3PAPm - 2PAPd.
Une vitesse maximale de l’IP supérieure à 2,2 m/s est corrélée à un niveau de pression pulmonaire élevé.
Il est donc possible de vérifier, au moins en phase de perfectionnement de l’opérateur, que la Vmax de l’IT a bien été enregistrée en confrontant la valeur de la PAPs déterminée par l’IT puis par l’IP. Une valeur moindre de la PAPs par l’IT incite à recherche en multipliant les fenêtres d’exploration un meilleur signal en Doppler continu.
Arguments indirects en faveur d’une HTP
Devant la difficulté technique d’obtenir de façon systématique les paramètres précédents, d’autres paramètres permettent d’évoquer une HTP.
Temps d’accélération pulmonaire et aspect du flux pulmonaire systolique en Doppler pulsé enregistré dans l’incidence parasternale petit axe centrée sur l’artère pulmonaire :
– ce temps se mesure entre le début (clic) et le pic de ce flux ;
– un temps d’accélération pulmonaire court (< 105 ms) est un marqueur d’élévation des pressions pulmonaires ;
– la présence d’une encoche méso- ou télésystolique (a « notched » [mid or late]) est en faveur de l’élévation du niveau de pression pulmonaire. Ce signe témoigne d’une élévation des résistances vasculaires pulmonaires (RVP) et de la faible compliance du lit artériel pulmonaire. On retrouvera donc ce signe en cas d’HTP précapillaire.
La mesure du diamètre de l’artère pulmonaire en incidence parasternale petit axe :
– la mesure s’effectue en télédiastole au niveau du tronc de l’AP à mi-chemin entre la valve et la bifurcation artérielle pulmonaire ;
– un diamètre > 25 mm est considéré comme pathologique, sans préjuger de la cause, surcharge en pression et/ou en volume.
Approche des résistances vasculaires pulmonaires
Les résistances artérielles pulmonaires (RVP) peuvent être estimées par échocardiographie- Doppler en calculant le rapport suivant (Abbas) :
Ce rapport est bien corrélé dans la littérature aux résistances artérielles pulmonaires évaluées par cathétérisme.
La valeur normale de ce rapport est inférieure à 0,15.
Les résistances artérielles pulmonaires peuvent être estimées en multipliant ce rapport par 10 (en négligeant le facteur de correction égal à 0,16).
Ainsi, un rapport supérieur à 0,2 suggère des résistances artérielles pulmonaires supérieures à 2 unités Wood (UW).
Retentissement de l’HTP sur les cavités droites et gauches
La mesure de ces paramètres permet d’évaluer le retentissement de l’HTP sur les cavités cardiaques et d’en apprécier le pronostic.
Surface de l’OD en incidence apicale 4 cavités :
– mesure est effectuée en télésystole juste avant l’ouverture de la valve tricuspide ;
– l’OD est dilatée pour une surface > 18 cm2 ;
– la détermination du volume de l’OD est préconisée (25+7 mL/m2 chez l’homme et 21+6 mL/m2 chez la femme).
Mesure du diamètre basal du VD en coupe apicale 4 cavités :
– en télédiastole à l’extrémité des feuillets tricuspides.
Mesure du rapport diamètre basal VD/diamètre basal VG :
– un diamètre basal > 41 mm et un rapport > 1 témoigne d’une dilatation du VD.
Mesure de la pression dans l’OD via la mesure du diamètre de la VCI et de la PAPs.
Éléments pronostiques de l’HTP
Épanchement péricardique
Sa présence est de mauvais pronostic dans l’HTAP et est corrélée à une défaillance cardiaque droite. La résorption liquidienne se fait par l’intermédiaire d’un réseau veineux et lymphatique localisé dans la région sous-épicardique et se drainant dans l’OD. L’élévation des pressions de l’OD gêne le retour veineux et conduit à la formation d’un épanchement. Figure 4
Figure 4. (A) Coupe parasternale grand axe montrant une dilatation du VD. (B) Coupe parasternale petit axe montrant un épanchement péricardique postéro au niveau du ventricule gauche (VG), avec aplatissement du septum interventriculaire.
Dimensions et fonction ventriculaire droite (VD)
Diamètres VD en apicales 4 cavités en télédiastole : (figure 5A)
– diamètre basal du VD : un diamètre supérieur à 41 mm est considéré comme pathologique ;
– diamètre médian du VD : mesuré au niveau des muscles papillaires du VD pathologique si > 35 mm ;
– diamètre longitudinal du VD : mesuré entre le plan de la valve tricuspide et l’apex du VD. Un diamètre supérieur à 83 mm est pathologique.
Figure 5. (A) Diamètres basal, médian et longitudinal du VD.
Fonction du ventricule droit (tableau 4)
La fonction longitudinale du ventricule droit :
– fraction de raccourcissement du VD : une FRVD < 35 % témoigne d’une dysfonction systolique du VD (figure 5B) ;
Figure 5. (B) Aires diastolique et systolique du VD permettant la mesure de de la fraction de raccourcissement VD.
– onde S’ systolique : en Doppler tissulaire (DTI) en mode pulsé au niveau de l’anneau tricuspide latéral en systole. Une vitesse maximale inférieure à 9,5 cm/s est en faveur d’une dysfonction systolique ventriculaire droite (figure 6A) ;
– excursion systolique du plan de l’anneau tricuspide (TAPSE) : mesure de l’amplitude de déplacement longitudinal systolique de l’anneau tricuspide latéral en coupe apicale 4 cavités en mode M. Le TAPSE est mesuré entre la télédiastole et le pic systolique. Une valeur inférieure à 17 mm suggère une dysfonction systolique longitudinale du VD (figure 6B).
Figure 6. (A) Onde S’ à l’anneau tricuspide en Doppler tissulaire pulsé. (B) TAPSE en mode échographique temps-mouvement.
Strain longitudinal du VD (figure 7)
Figure 7. Strain longitudinal ventriculaire droit.
Cette méthode permet la détection précoce d’une dysfonction systolique ventriculaire. Un strain longitudinal global inférieur à 19 % est considéré comme anormal, et < à 11 % est associé à une mortalité accrue à 1 an.
Suivi
Une fois le diagnostic d’HTP posé, un suivi tous les 6 à 12 mois semble nécessaire, voire tous les 3 à 6 mois si des modifications thérapeutiques doivent être apportées et plus précocement en cas d’aggravation de la symptomatologie.
Pour en savoir plus
• Humbert M et al. 2022 ESC/ERS Guidelines for the diagnosis and treatment of pulmonary hypertension. Eur Heart J 2022 ; 43(38) : 3618 731.
• Augustine DX et al. Echocardiographic assessment of pulmonary hypertension: a guideline protocol from the British Society of Echocardiography. Echo Res Pract 2018 ; 5(3) : G11 24.
• Topyła-Putowska W et al. Echocardiography in pulmonary arterial hypertension: comprehensive evaluation and technical considerations. J Clin Med 2021 ; 10(15) : 3229.
• Hassoun PM. Pulmonary Arterial Hypertension. Taichman DB, éditeur. N Engl J Med 2021 ; 385 (25) : 2361 76. Montané BE et al. Optimal Tricuspid Regurgitation Velocity to Screen for Pulmonary Hypertension in Tertiary Referral Centers. Chest 2021 ; 160(6) : 2209- 19.
• Martelli G et al. Echocardiographic assessment of pulmonary capillary wedge pressure by E/e’ ratio: a systematic review and meta-analysis. J Crit Care 2023 ; 76 : 154281.
• Amsallem M et al. Addressing the controversy of estimating pulmonary arterial pressure by echocardiography. J Am Soc Echocardiogr 2016 ; 29(2) : 93-102.
• Lang RM et al. Recommendations for cardiac chamber quantification by echocardiography in adults: an update from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. Eur Heart J Cardiovasc Imaging 2015 ; 16(3) : 233-7.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :