Imagerie
Publié le 20 juin 2023Lecture 6 min
Quelle imagerie dans la cardiomyopathie arythmogène du ventricule droit ?
Nicolas PIRIOU, CHU de Nantes ; Centre de compétence cardiomyopathies, Institut du thorax, Nantes
Contrairement aux autres cardiomyopathies (hypertrophiques, dilatées et restrictives), la cardiomyopathie arythmogène du ventricule droit (CAVD) n’est pas définie par une anomalie morphologique ou fonctionnelle du myocarde, mais par une anomalie histologique, à savoir un remplacement progressif du myocarde par un tissu fibreux et adipeux, générateur de troubles du rythme ventriculaire potentiellement graves, dont les premières descriptions ont été faites au niveau du « triangle de la dysplasie » c’est-à-dire entre la chambre d’admission, l’apex et la voie d’éjection du ventricule droit(1). L’avènement des techniques d’imagerie multimodales, en particulier l’IRM capable de mettre en évidence la fibrose myocardique, a ensuite permis d’identifier des patients présentant des atteintes ventriculaires gauches associées ou isolées, conduisant à employer la terminologie plus large de cardiomyopathies arythmogènes(2).
La prévalence de la maladie est estimée entre 1:2 000 et 1:5 000 dans la population générale. Elle est une des causes les plus fréquentes de mort subite du sujet jeune. Une cause génétique est retrouvée dans environ 50 % des cas, affectant essentiellement des protéines de la jonction intercellulaire (desmosome) en cas de formes ventriculaires droites, avec un spectre plus large en cas de formes gauches dominantes (desmosome, filament intermédiaire, réticulum sarcoplasmique et même laminopathies). Le phénotype de cardiomyopathie arythmogène peut également être rencontré dans des pathologies non génétiques, telles que la sarcoïdose cardiaque par exemple. Il apparaît donc essentiel de pouvoir diagnostiquer le plus tôt possible toutes formes de cardiomyopathies arythmogènes et d’en faire le diagnostic étiologique pour optimiser la prise en charge du patient, et éventuellement de sa famille. L’imagerie multimodale tient une place majeure dans ce contexte.
Imagerie et diagnostic de la cardiomyopathie arythmogène du ventricule droit : évolution des critères diagnostiques
Depuis la première édition des critères diagnostiques en 1994, réactualisés en 2010, le diagnostic de cardiomyopathie arythmogène ventriculaire droite repose sur la présence de critères majeurs ou mineurs basés sur l’ECG, l’histoire familiale ou la génétique, l’anatomopathologie, et l’imagerie. Ces critères soulignent la place importante de l’imagerie comme critère majeur dans le diagnostic de CAVD, mais également l’importance d’y associer d’autres arguments diagnostiques, en particulier l’électrocardiogramme, pour en améliorer la spécificité et éviter les surdiagnostics. Les critères d’imagerie de 2010 reposent soit sur l’échocardiographie bidimensionnelle, soit sur l’angiographie, soit sur l’IRM et sont définis par l’association d’une dilatation anormale du VD ou une altération de sa fonction globale plus une anomalie de sa cinétique segmentaire (tableau 1). À l’usage, ces critères d’imagerie ont démontré quelques limites. L’analyse échographique bi-dimensionnelle du ventricule droit peut souffrir d’un défaut de spécificité et surtout de sensibilité, notamment due à un manque de résolution spatiale pour l’analyse de cette cavité cardiaque qui rend difficiles à la fois la réalisation de mesures fiables des diamètres et de la fraction de raccourcissement en surface et l’analyse fine des anomalies de la cinétique segmentaire. L’échocardiographie tri-dimensionnelle permettant de mesurer des volumes et une fraction d’éjection, et surtout le développement de l’échocardiographie de déformation (2D-strain) pour améliorer la détection des troubles de cinétique segmentaire par la mesure de la dispersion mécanique des pics de déformation en systole des différents segments de la paroi libre du VD (figure 1) permettent d’améliorer la sensibilité du critère échocardiographique.
Figure 1. Mesure de la dispersion des pics de déformation systolique des segments de la paroi libre du VD en échocardiographie utilisant le 2D-strain, permettant d’augmenter la sensibilité des critères échocardiographiques(6).
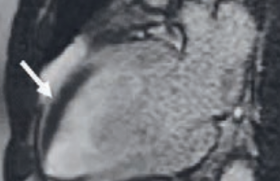
L’IRM cardiaque est un élément incontournable des critères diagnostiques d’imagerie. Elle dispose d’une meilleure résolution spatiale que l’échocardiographie pour améliorer la détection des troubles de cinétique VD (figure 2) et est l’imagerie de référence pour la mesure des volumes et de la fraction d’éjection. Son développement a fait tomber l’angiographie en désuétude.
Figure 2. Image ciné-IRM 4 cavités arrêtée en fin de systole, montrant 3 zones dyskinétiques pseudo-anévrismales (bulging) de la paroi libre du ventricule droit, représentant un composant du critère majeur d’imagerie, ou un nouveau critère mineur s’il est isolé.
Néanmoins, quelle que soit la modalité utilisée, les critères d’imagerie de 2010 peuvent pécher par excès de spécificité et manquer de sensibilité. En conséquence, de nouveaux critères ont été proposés en 2020 par l’école de Padoue après une évaluation critique des critères de 2010 par des experts internationaux(2,3). Ces nouveaux critères proposent d’ajouter comme critère mineur la présence d’anomalies cinétiques isolées du VD. Surtout, ils incorporent désormais comme critère majeur la présence de rehaussement tardif en IRM après injection de gadolinium, équivalent à la mise en évidence du remplacement fibro-adipeux par biopsie endomyocardiaque historiquement requis dans les critères initiaux (tableau 1, figure 3).
Figure 3. Image IRM de rehaussement tardif après injection de gadolinium montrant sur deux coupes orthogonales (petit axe à gauche, 4 cavités à droite) des plages de rehaussement tardif de la paroi libre du VD moyenne et de la paroi inférieure, représentant un nouveau critère majeur d’imagerie pour le diagnostic de CAVD.
Imagerie et diagnostic de l’atteinte ventriculaire gauche
L’analyse histologique de cœurs de patients décédés ou transplantés porteurs de cardiomyopathie arythmogène révèle une atteinte ventriculaire gauche dans 76 % des cas(4). L’atteinte ventriculaire gauche peut être visible en imagerie sous la forme d’une atteinte morphologique ou fonctionnelle du VG (altération de la FEVG ou trouble de la cinétique segmentaire avec ou sans dilatation ventriculaire). Néanmoins, l’atteinte ventriculaire gauche s’exprimant fréquemment uniquement sous la forme d’un remplacement fibreux du myocarde VG sans altération de fonction globale ou régionale, le critère majeur d’atteinte gauche dans les cardiomyopathies arythmogènes consiste en la mise en évidence en IRM avec injection de gadolinium d’un rehaussement tardif médiopariétal ou sous-épicardique d’au moins un segment VG confirmé sur deux coupes orthogonales (figure 4). On définit ainsi 3 formes phénotypiques de cardiomyopathies arythmogènes : cardiomyopathie arythmogène ventriculaire droite, cardiomyopathie arythmogène biventriculaire, et cardiomyopathie arythmogène ventriculaire gauche dominante. Le critère majeur d’atteinte ventriculaire gauche étant peu spécifique, car présent également notamment dans des pathologies inflammatoires et infectieuses (myocardites, sarcoïdose, maladie de Chagas), la mise en évidence d’une anomalie génétique pathogène dans un gène connu de cardiomyopathie arythmogène est requise pour confirmer le diagnostic de CAVG, contrairement à la cardiomyopathie arythmogène du VD (figure 5).
Figure 4. Image IRM de rehaussement tardif après injection de gadolinium montrant des plages de rehaussement tardif médiopariétal septal et sous-épicardique latéral représentant le critère majeur de diagnostic de l’atteinte VG dans les cardiomyopathies arythmogènes.
Figure 5. Définitions des différents phénotypes de cardiomyopathie arythmogène selon l’imagerie, d’après(7).
Diagnostic précoce des apparentés dans les formes héréditaires
L’utilisation des nouveaux critères diagnostiques d’imagerie (échocardiographie avancée 3D et surtout de déformation, IRM de rehaussement tardif VD et VG) doit être encouragée pour le dépistage présymptomatique de cardiomyopathie arythmogène chez les apparentés de sujets atteints afin d’en augmenter la sensibilité et mettre en place le plus précocement possible les mesures thérapeutiques et de prévention éventuellement nécessaires.
Imagerie et diagnostic des « phénocopies » de cardiomyopathies arythmogènes
Des pathologies non génétiques, notamment certaines cardiomyopathies inflammatoires, peuvent mimer tous types de phénotypes de cardiomyopathie arythmogène. C’est le cas de la sarcoïdose cardiaque, dont le diagnostic différentiel est d’une importance majeure, car nécessitant un traitement spécifique immunosuppresseur urgent. La réalisation d’une TEP au 18FFDG doit être évoquée devant tout phénotype de cardiomyopathie arythmogène non expliqué par l’analyse génétique ou l’histoire familiale (figure 6).
Figure 6. TEP-scanner cardiaque au 18F-FDG après extinction de la fixation physiologique du myocarde par régime sans glucides et riche en graisse et jeune prolongé, permettant de mettre en évidence des zones d’inflammation myocardique focales de la paroi libre du VD et du septum basal, ainsi que des adénopathies médiastinales, en rapport avec une sarcoïdose.
Imagerie et évaluation du pronostic
La stratification du pronostic, notamment du risque rythmique, reste une question difficile et débattue chez les patients porteurs de cardiomyopathie arythmogène. La place des différents critères d’imagerie pour établir le pronostic reste à établir, mais la présence d’une atteinte biventriculaire ou ventriculaire gauche dominante marquée semble être un facteur de mauvais pronostic rythmique(5).
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :