Imagerie
Publié le 19 déc 2024Lecture 6 min
Qu’attendre de l’IRM cardiaque dans le post-infarctus ?
Jérôme GAROT, Institut cardiovasculaire Paris Sud (ICPS), hôpital privé Jacques Cartier, Ramsay Santé, Massy
L’infarctus du myocarde représente environ 80 000 nouveaux cas/an en France et reste un fléau majeur de santé publique. En effet, près de 10 % des patients décèdent dans l’heure suivant la survenue des symptômes. Les progrès des thérapeutiques médicamenteuses et interventionnelles ont permis une réduction de la mortalité hospitalière à 30 jours de 10 % à 2 % au cours des 25 dernières années. L’imagerie par résonance magnétique est devenue une technique d’imagerie incontournable dans le diagnostic et l’évaluation pronostique de nombreuses pathologies cardiovasculaires. Cette modalité n’a que peu de contreindications absolues et peut être réalisée en moins de 30 minutes pour la plupart des indications, au sein de structures spécialisées. Elle joue un rôle majeur dans la prise en charge de l’infarctus du myocarde au stade initial, mais également à plus long terme, permettant d’orienter la prise en charge des patients.
Place de l’IRM lors de la phase initiale
La réalisation d’une IRM cardiaque en post-infarctus nécessite l’utilisation d’une machine de génération récente 1,5 T ou 3 T, munie d’un système de gradients récents, ainsi que des séquences modernes adaptées à l’imagerie cardiaque. Les acquisitions sont synchronisées à un électrocardiogramme et le post-traitement s’effectue sur des stations dédiées. Dans les premières heures de l’infarctus, le patient doit être dirigé sans délai vers une salle de cathétérisme pour la réalisation d’une coronarographie et angioplastie directe. Aucune technique d’imagerie ne doit allonger ce délai. Après la revascularisation urgente, l’IRM apporte des éléments importants.
Évaluation de la reperfusion myocardique à l’étage tissulaire
L’IRM permet une analyse dynamique fine (résolution spatiale ~1,5-2 mm) de la perfusion myocardique par la distribution intramyocardique d’un agent de contraste (chélate de gadolinium). L’IRM peut être réalisée dès J0 ou J1 après la revascularisation, la mise en place récente de stents ne constituant pas une contre-indication. Ainsi, 2 situations opposées peuvent être mises en évidence :
– une absence de défect de perfusion myocardique, indiquant une bonne reperfusion tissulaire ;
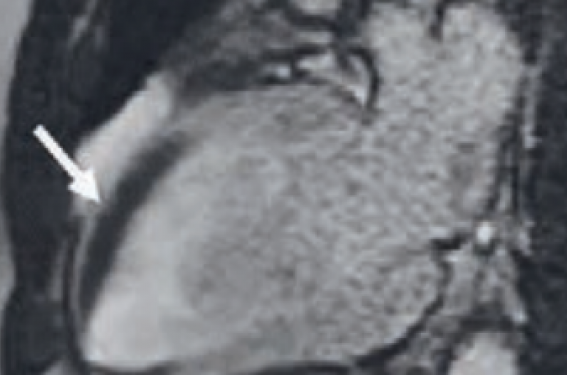
– une présence d’un défect de perfusion myocardique, indiquant une obstruction microvasculaire précoce. Cette obstruction microvasculaire peut être présente malgré la restauration d’un flux coronaire TIMI 3 lors de l’angioplastie de l’artère coupable (figure 1).
Figure 1. Patient de 59 ans ayant présenté un infarctus antérieur aigu avec angioplastie de l’IVA à H6. L’IRM à J1 met en évidence un défect marqué de perfusion myocardique dans le territoire antéro-septo-apical (flèches) malgré la restauration du flux coronaire.
Cette situation fréquente s’accompagne d’un pronostic défavorable en termes de remodelage VG et d’évènements cliniques, surtout lorsqu’elle est associée à une obstruction microvasculaire tardive sur les images de rehaussement tardif 10 minutes plus tard (figure 2)(1).
Figure 2. Patient de 64 ans ayant présenté un infarctus latéral. Angioplastie de la marginale à H5. Défect de perfusion myocardique au premier passage de l’agent de contraste (gauche, flèche), avec obstruction microvasculaire tardive à 10 minutes (droite, flèche).
Fonction VG, taille de l’infarctus, et index de sauvetage myocardique
Le ciné-IRM permet une analyse dynamique de la fonction VG en vues grand axe et petit axe, donnant accès aux volumes VG, à la fraction d’éjection VG/VD, ainsi qu’à la localisation et au nombre de segments akinétiques/17. Au stade initial, les anomalies de cinétique VG ou VD sont indicatives de l’étendue de la sidération myocardique. La caractérisation tissulaire du myocarde autorise la quantification de l’étendue de l’œdème myocardique grâce aux séquences pondérées T2 (séquences sang noir en spinécho, cartographies T2 du myocarde) (figure 3). La comparaison de l’étendue de l’œdème myocardique, assimilé à la zone à risque, et de la taille finale de l’infarctus en rehaussement tardif à 10 mi nutes, permet de calculer l’index de sauvetage myocardique(2) :
IS = [(ZAR – LGE)/ZAR] x 100 ou : IS : index de sauvetage myocardique, ZAR : zone à risque, LGE : rehaussement tardif.
Un index de sauvetage myocardique maximal de 100 % résulte en l’absence d’infarctus définitif.
Figure 3. Exemples de présence d’un œdème myocardique transmural sur les séquences T2 spin-écho sang noir réalisées à J2 chez un patient ayant présenté un infarctus inféro-apical aigu (gauche, flèche), et chez un autre patient après un infarctus latéral basal aigu (droite, flèche).
Cartographies T1 et T2 du myocarde
Ces séquences récentes permettent une mesure spatialement résolue (par pixel) des temps de relaxation T1 et T2 du myocarde. Les cartographies T1 sont utiles pour une délimitation précise de l’infarctus, tandis que les cartographies T2 délimitent l’œdème par l’augmentation du temps de relaxation transverse (figure 4). Les valeurs normales ne sont pas transposables d’une machine à l’autre. Les plages de normalité et les déviations standards doivent être établies localement pour chaque machine(3).
Figure 4. Cartographies T1 (gauche) et T2 (droite) à J3 chez un patient ayant présenté un infarctus inférieur aigu, montrant une élévation des temps de relaxation (flèches).
Complications mécaniques aiguës
L’IRM est bien adaptée à la mise en évidence des complications mécaniques aiguës en postinfarctus (figure 5), les seules potentielles limites étant le caractère d’urgence et l’instabilité hémodynamique. L’IRM permet le diagnostic des thrombus précoces du VG, en mesurant leur taille, le caractère pédiculé ou sessile, leur mobilité, identifiant ainsi le risque embolique. Elle visualise un épanchement péricardique aigu, un anévrisme précoce du VG, le différenciant d’une rupture cloisonnée du VG avec faux anévrisme (zone de rupture, collet étroit, péricarde externe). Une insuffisance mitrale par rupture d’un chef de pilier peut être visualisée et quantifiée, ainsi qu’une communication interventriculaire.
Figure 5. Complications mécaniques post-infarctus. A. Thrombus apical. B. Anévrisme inféro-basal. C. Rupture septo-apical avec faux anévrisme apical. D. Insuffisance mitrale. E. Épanchement péricardique, tamponade.
Indications de « Life-Vest »
Par l’étude précise de la fonction VG, l’IRM peut permettre d’aider à la décision de mise en place temporaire d’une Life-Vest chez les patients à haut risque rythmique ayant une FE VG < 30 %.
Place de l’IRM au décours de l’infarctus
Fonction VG et VD
L’IRM est la technique de référence pour l’étude de la fonction VG et VD globale. Elle permet une étude des volumes ventriculaires de manière anatomique, par la possibilité d’établir de manière automatisée les contours endocardiques ventriculaires sur une série de coupes ciné petit axe couvrant ’ensemble des 2 ventricules. Ces coupes petit axe sont acquises de manière perpendiculaire au grand axe VG. La résolution temporelle doit être < 50 ms. Ainsi, l’IRM joue un rôle important pour la détermination précise de la FEVG en post-infarctus et pour la décision d’implantation d’un défibrillateur au terme du 3e mois.
Taille définitive de l’infarctus, viabilité myocardique
Par l’étude du rehaussement tardif 10 minutes après l’injection de Gadolinium, l’IRM permet une imagerie directe de la zone infarcie qui apparaît en hypersignal en raison de la diffusion du Gadolinium au sein de la zone de nécrose. Ainsi la taille définitive de l’infarctus peut être exprimée au 3e mois par le nombre de segments infarcis (N/17), ou de manière quantitative grâce à la planimétrie semi-automatique de la zone de nécrose par le pourcentage ou la masse de myocarde infarci (en % ou en g).
L’analyse du rehaussement tardif permet aussi de déterminer la transmuralité de l’infarctus qui est une mesure directe de la viabilité myocardique (figure 6). Un infarctus qui s’étend sur plus de 50 % de l’épaisseur myocardique, a fortiori s’il est transmural, ne comporte plus de viabilité myocardique locale significative. À l’opposé, un infarctus qui intéresse moins de 50 % de l’épaisseur myocardique est sous-endocardique avec une bonne probabilité de récupération fonctionnelle(4).
Figure 6. Rehaussement tardif. Séquelle d’infarctus antérieur étendu transmural sans viabilité (gauche). Séquelle d’infarctus antérieur non transmural avec viabilité (transmuralité 25-50 %, droite).
Remodelage VG, anévrismes VG, pseudo-anévrismes VG, thrombus VG, insuffisance mitrale
Au décours de l’infarctus, l’IRM permet l’étude de l’évolution des volumes et des fractions d’éjection ventriculaires, et donc une étude fine du remodelage VG. Les diverses séquences de ciné, de perfusion et de rehaussement tardif sont utiles au diagnostic différentiel entre vrai et faux anévrisme du VG. La séquence de rehaussement tardif est la plus sensible pour la détection des thrombus VG. L’IRM permet de quantifier l’insuffisance mitrale en soustrayant le volume d’éjection aortique obtenu par fluximétrie du volume d’éjection VG obtenu par volumétrie (volume régurgitant).
EN PRATIQUE
• L’IRM apporte de nombreuses informations importantes en phase initiale ou au décours de l’infarctus du myocarde.
• La difficulté principale reste la disponibilité dans le contexte clinique d’infarctus du myocarde.
L’auteur déclare n’avoir aucun conflit d’intérêts en relation avec le contenu de l’article.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :