Publié le 08 juin 2004Lecture 8 min
Détérioration structurelle des bioprothèses
J.-N. FABIANI, hôpital européen Georges Pompidou, Paris
Les deux principales complications des bioprothèses sont la détérioration structurelle au fil du temps et les accidents thromboemboliques. Ces derniers sont relativement rares avec ce type de valve, faisant ainsi de la détérioration structurelle le souci majeur.
Depuis leur première utilisation au début des années 1970 jusqu’à nos jours, les observations ainsi que nos connaissances concernant ce type de complications ont constamment évolué, notamment avec les améliorations continues dans la conception même de ces valves. La détérioration structurelle des bioprothèses est provoquée essentiellement par deux facteurs :
- la position de la valve : mitrale ou aortique ;
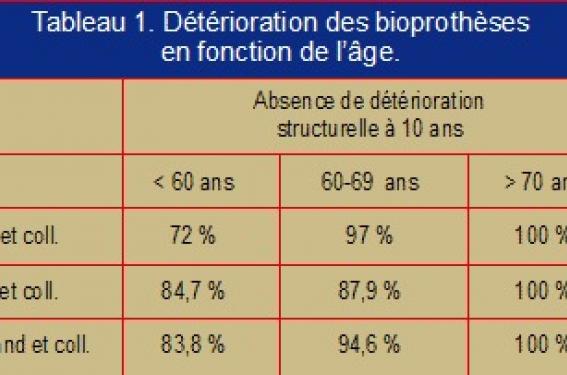
- l’âge du malade (tableau 1) au moment de l’implantation de la bioprothèse.
Bioprothèses porcines
1re génération
Les bioprothèses porcines de Hancock et de Carpentier-Edwards standard (en position intraannulaire) ont été les premières à être utilisées, dès le début des années 70. Elles disposent par conséquent du suivi le plus long, jusqu’à 21 ans, et ce notamment grâce aux travaux de Jamieson et coll. L’absence de détérioration des valves porcines Carpentier-Edwards standard (CE standard) en position aortique et mitrale était de 40,6 % et 8,5 % respectivement à 18 ans. Ces taux variaient significativement en fonction de la position de la bioprothèse et surtout en fonction de l’âge des patients au moment de l’implantation (tableau 2 ; figure 1).
Figure 1A. Absence de détérioration structurelle en fonction du temps, des CE Standard en fonction de la position (aortique vs mitrale). Jamieson et al. Ann Thorac Surg 1998 ; 66(6 Suppl) : S40-3.
Figure 1B. Absence de détérioration structurelle en fonction du temps, des CE standard en position aortique, par groupe d’âge. Jamieson et al. Ann Thorac Surg 1998 ; 66(6 Suppl) : S40-3.
Figure 1C. Absence de détérioration structurelle en fonction du temps, des CE Standard en position mitrale, par groupe d’âge. Jamieson et al. Ann Thorac Surg 1998 ; 66(6 Suppl) : S40-3.
La détérioration structurelle des bioprothèses porcines survenait à tous les âges et d’autant plus précocement que le sujet était jeune. Ces détériorations étaient essentiellement à type de déchirure des cusps chez le sujet âgé. Les calcifications survenaient essentiellement chez le sujet jeune. Les déchirures étaient attribuées aux contraintes physiques auxquelles étaient soumises ces valves, ce qui expliquait en partie une durabilité nettement moindre lorsque celles-ci étaient placées en position mitrale.
2e génération
Étant donné le taux élevé d’échecs à moyen terme des premières bioprothèses porcines, notamment chez les sujets âgés de moins de 60 ans, et surtout lorsque celles-ci étaient placées en position mitrale, des modifications structurelles ont donné naissance à la 2e génération de bioprothèses porcines, comme celle de Carpentier-Edwards supra-annulaire.
• Les résultats de la Carpentier-Edwards supra-annulaire à 15 ans étaient encourageants, avec une absence de détérioration chez 84 % des patients âgés de 60 à 70 ans, et chez 97 % des patients âgés de plus de 70 ans (figure 2).
Figure 2. Absence de détérioration structurelle en fonction du temps, de la CE supra-annulaire porcine, par groupe d’âge (actuarielle). Jamieson et al. Ann Thorac Surg 2001 ; 71(Suppl) : S224-7.
• Pupello et coll. ont suivi pendant 18 ans des bioprothèses porcines de tous genres chez des patients âgés de plus de 65 ans. Ils ont rapporté une absence de détérioration structurelle de la valve chez 84 % des patients. Ce taux était de 81 % dans le groupe de patients âgés de 65 à 74 ans ; il passait à 97 % dans le groupe de patients de plus de 75 ans au moment de l’implantation.
• Fann et coll. ont rapporté des résultats similaires à 20 ans pour les bioprothèses porcines, avec des taux de survie et de détérioration structurelle différents en fonction des groupes d’âge des patients et de la position d’implantation de la valve.
Bioprothèse péricardique
La bioprothèse péricardique de Carpentier-Edwards de 1re génération offrait une meilleure performance hémodynamique que la porcine. Toutefois, un taux initial de défaillances structurelles assez élevé, lié surtout à des problèmes d’ordre mécanique, a conduit à la conception des bioprothèses péricardiques de 2e génération, dont la Carpentier-Edwards Perimount (CE-P). Cette dernière se distinguait essentiellement de la première par une technique particulière de montage sur le stent.
Effets liés à l’âge
• Le suivi à 12 ans de la CE-P a montré des résultats très satisfaisants, d’après les travaux de Marchand ; ainsi, selon l’âge du patient et la position de la valve, on notait :
- en position aortique, un bon fonctionnement de la bioprothèse à 12 ans chez 89 % des patients de moins de 60 ans et chez 98 % des patients de plus de 60 ans (p < 0,03) ;
- en position mitrale, un bon fonctionnement de la bioprothèse à 12 ans chez 70 % des patients de moins de 60 ans et chez 100 % des patients de plus de 60 ans (p < 0,01).
• Jamieson et Marchand ont même montré une durabilité supérieure de la bioprothèse péricardique CE-P en position mitrale comparativement à la bioprothèse porcine (tableau 3 ; figures 3 et 4). Cet avantage était probablement dû à une plus grande résistance des bioprothèses péricardiques quant aux contraintes mécaniques (ce qui explique le fait que 18 % seulement des détériorations structurelles de la CE Perimount soient dues à des déchirures de cups comparativement à 27 % pour les porcines).
Figure 3. Absence de détérioration structurelle en fonction du temps, des CE-P vs CE supra-annulaires, en position mitrale, pour le groupe d’âge 61-70 ans. Courbe actuarielle. Jamieson et al. J Thorac Cardiovasc Surg 1999 ; 118 : 297-304. CE-P = Carpentier-Edwards Perimount ; CE-SAV = CE porcine supra-annulaire.
Figure 4. Absence de détérioration structurelle en fonction du temps, des CE-P vs CE supra-annulaires, en position mitrale, pour le groupe d’âge < 60 ans. Courbe actuarielle. Jamieson et al. J Thorac Cardiovasc Surg 1999 ; 118 : 297-304. CE-P = Carpentier-Edwards Perimount ; CE-SAV = CE porcine supra-annulaire.
• Banbury et coll. ont rapporté leur suivi à 15 ans des bioprothèses péricardiques CE, en fonction de l’âge des patients au moment de l’implantation et de la taille de la valve. Ils ont montré que le risque de détérioration structurelle de la bioprothèse augmente exponentiellement avec le temps, avec une survie sans explantation de la bioprothèse de l’ordre de 99 % à 5 ans, 94 % à 10 ans et 77 % à 15 ans. Chez les patients âgés de plus de 65 ans au moment de l’implantation de la bioprothèse, le risque de réopération à 15 ans pour dégénérescence structurelle de la bioprothèse était < 10 %. Ce risque passait à 55 % chez les patients opérés à l’âge de 45 ans. Le seul facteur de risque de détérioration structurelle de la bioprothèse dans leur série était l’âge jeune au moment de l’implantation de la valve (figure 5).
Figure 5. Détérioration structurelle de la bioprothèse péricardique CE en fonction de l’âge des patients au moment de l’implantation.
A = Survie sans détérioration structurelle dans chaque groupe d’âge. B = Survie sans détérioration structurelle à 15 ans, à travers le spectre des groupes d’âge au moment de l’implantation. Banbury et al. Ann Thorac Surg 2001 ; 72 : 753-7.
• Cette différence de survie des bioprothèses péricardiques en fonction de l’âge au moment de l’implantation a été aussi retrouvée par Aupart et coll. et par Poirier et coll.
• Pomar et coll. ont obtenu des résultats qui vont dans le même sens pour la bioprothèse péricardique aortique Mitroflow, en rapportant un taux de détériorations de 1,2 %/patients-années chez les patients âgés de plus de 70 ans, comparativement à 3,13 %/patients-années chez les patients âgés de 60 à 69 ans.
Effets de la taille de la bioprothèse
La petite taille des bioprothèses (n° 19) pourrait, selon certains auteurs, jouer un rôle accélérateur dans leur détérioration.
• En effet, Banbury et coll. ont constaté dans leur série une tendance non significative à une détérioration accélérée des bioprothèses de petit diamètre (de 19 mm).
• Cette tendance n’a pas été confirmée par l’étude prospective faite par Carrier et coll. : en comparant les bioprothèses de 19 mm aux autres bioprothèses de plus grand diamètre, ces derniers n’ont pas retrouvé de relation entre la petite taille de la valve, d’une part, et la mortalité à 7 ans, la survenue d’événements liés à la valve et les taux de réopérations liés à la valve, d’autre part.
• Cette affirmation est confortée par les résultats de plusieurs études qui ont évalué, in vivo et in vitro, le gradient transvalvulaire associé aux bioprothèses de petit diamètre. Les gradients transvalvulaires moyens associés aux bioprothèses péricardiques 19 variaient de 12 à 22 mmHg et l’orifice effectif d’ouverture de ces valves allait de 1,1 à 1,55 cm2. Takakura et coll. ont même montré que la surface d’ouverture de la bioprothèse augmente sous Dobutrex®, au prix d’une augmentation très modérée du gradient transvalvulaire.
• Khan et coll. ont montré une diminution de la masse musculaire du ventricule gauche après remplacement valvulaire aortique par une bioprothèse péricardique CE n° 19.
• D’un autre côté, Poirier et coll. n’ont pas retrouvé de différence entre la bioprothèse péricardique CE 19 et la bioprothèse stentless Medtronic Freestyle 19 au niveau du gradient et au niveau des orifices effectifs d’ouverture.
• La survie sans réopération pour les bioprothèses péricardiques CE de petites tailles étaient de 89 % à 12 ans d’après Nakajima et coll. et de 99 % à 10 ans d’après Aupart et coll.
• Selon ces mêmes auteurs, la survie sans détérioration structurelle variait de 92 à 98 % à 10 ans.
Effet du « miss-match » valve/patient
En fait, si la petite taille de la bioprothèse n’influence pas la survie à long terme, c’est plutôt le « miss-match » entre la taille de la valve et la surface corporelle du patient qui aurait un effet péjoratif sur la survie. Ce miss-match serait responsable, non pas d’une détérioration plus rapide de la bioprothèse, mais plutôt d’une persistance du gradient en postopératoire et, par conséquent, d’une mortalité plus élevée à long terme.
Rao et coll. ont étudié le rapport entre l’orifice effectif de la bioprothèse et la surface corporelle du patient. Ils ont montré qu’un rapport < 0,75 est un facteur prédictif de mortalité, car associé à la persistance en postopératoire du gradient transvalvulaire et de l’obstruction de la chambre de chasse du ventricule gauche. Cela augmenterait le risque de mort subite, notamment chez les patients avec une atteinte coronarienne associée. Ces auteurs ont recommandé l’élargissement de l’anneau aortique chez les patients jeunes et/ou obèses, afin d’éviter le miss-match entre la taille de la bioprothèse et la surface corporelle du patient.
En conclusion
Les bioprothèses peuvent être proposées aux patients âgés de plus de 65 ans avec d’excellents résultats à 15 et à 20 ans. Le risque de réopération dans ce groupe de patients est < 10 % en 15 ans. En cas de petit anneau aortique, l’élargissement de l’anneau (grevé d’une majoration du risque opératoire) n’est pas toujours nécessaire ; une bioprothèse 19 est un bon choix, pourvu que le rapport orifice d’ouverture/surface corporelle soit > 0,85, et ce d’autant plus que le patient est âgé.
La petite taille de la bioprothèse ne compromet pas sa durabilité.
Une bibliograpnie sera adressée aux abonnés sur demande au journal.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :