Publié le 04 avr 2006Lecture 6 min
Embolie pulmonaire : stratégie des examens complémentaires devant une suspicion d'EP
N. MÉNEVEAU, CHU Jean Minjoz, Besançon
L’approche diagnostique de l’embolie pulmonaire (EP) a beaucoup évolué au cours de ces dernières années avec l’avènement de stratégies séquentielles faisant appel à des moyens diagnostiques non invasifs. Les algorithmes décisionnels utilisant la probabilité clinique, le dosage des D-dimères, l’échographie veineuse, la scintigraphie pulmonaire et plus récemment le scanner spiralé ont permis de réduire très significativement le recours à l’angiographie pulmonaire, avec un rapport coût-efficacité très satisfaisant.
Probabilité clinique
L’évaluation clinique de l’EP doit s’intégrer à des examens paracliniques de dépistage comme l’ECG, la radiographie pulmonaire et la gazométrie artérielle. Les signes cliniques de l’EP sont peu sensibles et peu spécifiques. Associés à la présence de facteurs de risque et aux antécédents du patient, ils permettent l’évaluation empirique ou standardisée de la probabilité clinique d’EP. Les scores de Wells et de Genève, basés sur des évaluations standardisées, définissent trois niveaux de risque (faible, intermédiaire ou élevé) correspondant à des prévalences respectives de l’EP de 10, 35, et 70 %. Ces deux scores ont été récemment comparés et leurs performances se sont révélées similaires pour prédire la prévalence de l’EP dans un collectif de patients se présentant aux urgences (tableaux 1 et 2).
D-dimères
Un dosage de D-dimères < 500 µg/l selon la technique ELISA a une valeur prédictive négative > 95 %, qui permet d’exclure le diagnostic d’EP chez environ un tiers des patients ambulatoires. Toutefois, la spécificité médiocre des D-dimères en limite fortement l’utilité clinique chez les patients âgés et/ou hospitalisés.
Échographie de compression veineuse
Près de 90 % des EP proviennent d’une thrombose veineuse profonde (TVP) ; inversement, la fréquence des EP asymptomatiques chez les sujets ayant une TVP est de l’ordre de 50 %. Ainsi, la découverte d’une TVP chez un patient suspect d’EP est aujourd’hui suffisante pour affirmer le diagnostic d’EP. Pour ce faire, l’échographie veineuse s’est imposée comme le meilleur examen morphologique avec une excellente spécificité. Toutefois, en raison d’une sensibilité voisine de 50 %, une échographie veineuse normale ne permet pas d’écarter le diagnostic d’EP.
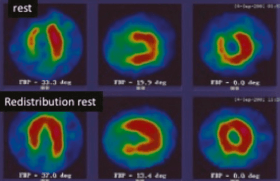
Scintigraphie de ventilation-perfusion
La scintigraphie de ventilation-perfusion a longtemps eu un rôle prépondérant dans la stratégie diagnostique de l’EP et reste déterminante quand elle permet d’exclure ou de confirmer l’EP en cas d’examen normal ou de forte probabilité. Malheureusement, plus de 50 % des scintigraphies pulmonaires se révèlent non diagnostiques, en particulier chez les patients âgés ou ayant des anomalies radiologiques. En outre, sa disponibilité reste insuffisante dans un grand nombre de centres hospitaliers généraux. Pour toutes ces raisons, la scintigraphie a progressivement cédé la place au scanner spiralé dans l’algorithme décisionnel de l’EP.
Scanner spiralé
L’apport du scanner spiralé constitue une avancée déterminante dans la démarche diagnostique de l’EP. À l’inverse de la scintigraphie pulmonaire, le scanner spiralé permet la visualisation directe du thrombus et la détection d’anomalies parenchymateuses qui peuvent s’intégrer dans le diagnostic d’EP ou au contraire fournir une alternative diagnostique.
La sensibilité du scanner spiralé varie entre 57 et 100 % et sa spécificité entre 78 et 100 %. Cette variabilité importante est liée en partie à l’utilisation dans les essais cliniques de scanners de différentes générations et à la localisation des thrombi dans l’arbre artériel pulmonaire. Sensibilité et spécificité sont ainsi > 90 % dans la détection des thrombi proximaux et lobaires.
La visualisation d’EP segmentaires ou sous-segmentaires est, en revanche, plus difficile et associée à une sensibilité variant entre 71 et 84 %. Cela signifie qu’un scanner positif avec présence de thrombus proximal est un bon critère d’EP, alors qu’un scanner normal ne permettrait pas d’en exclure le diagnostic.
Toutefois, utilisé dans des stratégies diagnostiques bien conduites, le scanner spiralé est un outil très performant. Sa valeur prédictive négative (VPN) est > 96 % (IC95% : 88-99 %) chez les patients ayant une probabilité clinique élevée d’EP et une scintigraphie pulmonaire non diagnostique.
Le taux de récidives thromboemboliques à 3 mois des patients ayant un scanner spiralé normal, une échographie veineuse des membres inférieurs négative et une probabilité clinique faible ou intermédiaire n’excède pas 1,8 %. Deux métaanalyses récentes regroupant une vingtaine d’essais et près de 4 000 patients, ont établi que le taux d’événements thromboemboliques observés à 3 mois en l’absence de traitement anticoagulant chez les patients avec scanner spiralé négatif est de 1,4 % (IC95 % : 1,1-1,8 %). Chez ces mêmes patients, le taux d’EP fatales à 3 mois était de 0,51 % (IC95 % : 0,33-0,76 %). Ces chiffres sont tout à fait superposables à ceux rapportés après angiographie pulmonaire normale ou dans les stratégies diagnostiques utilisant la scintigraphie pulmonaire.
Il est admis aujourd’hui que l’arrêt du traitement anticoagulant est sûr et justifié chez les patients ayant un scanner spiralé normal couplé à une échographie veineuse des membres inférieurs négative, à l’exception des patients ayant une probabilité clinique élevée.
Plus récemment encore, Perrier et coll. ont évalué une nouvelle stratégie diagnostique s’appliquant aux patients non hospitalisés et ayant une probabilité clinique faible ou intermédiaire d’EP. Cette stratégie repose sur la simple association d’un dosage des D-dimères et la réalisation d’un scanner spiralé multibarettes de dernière génération, sans faire appel à l’écho-Doppler veineux des membres inférieurs. Les résultats font état d’un risque d’événements thromboemboliques à 3 mois de 1,5 % (IC95% : 0,8-3 %). D’autres travaux confirmatifs sont toutefois nécessaires avant que cette stratégie ne soit validée en pratique clinique courante.
Échocardiographie Doppler transthoracique
Si l’échocardiographie Doppler permet rarement d’affirmer le diagnostic d’EP, en visualisant la présence d’un thrombus dans l’artère pulmonaire ou les cavités droites, elle permet en revanche d’apporter des informations pronostiques utiles à la stratification du risque. Son intérêt est déterminant dans la prise en charge de l’EP massive définie par la présence d’un choc cardiogénique ou d’une hypotension artérielle systémique < 90 mmHg.
Devant un tableau clinique d’instabilité hémodynamique chez un patient suspect d’EP, la présence de signes échocardiographiques de cœur pulmonaire aigu permet d’instaurer, sans attendre, un traitement approprié.
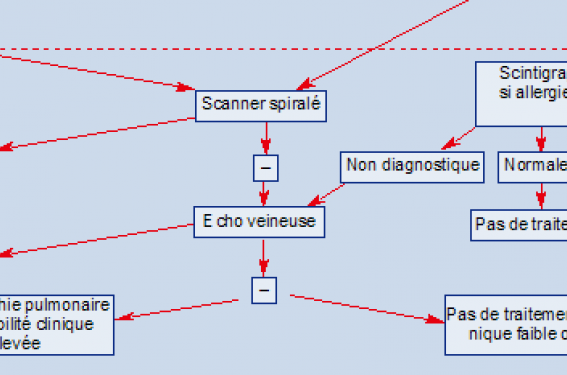
Schémas 1 et 2. Stratégies diagnostiques possibles dans la prise en charge de l’EP massive et non massive.
Stratégie diagnostique
Les arbres décisionnels (schémas 1 et 2) résument les stratégies diagnostiques possibles dans la prise en charge de l’EP non massive et massive. Ces stratégies ne prennent pas en compte le dosage de la troponine ou du BNP (brain natriuretic peptide), dont l’intérêt s’inscrit plutôt dans une démarche de stratification du risque évolutif, au même titre que la présence de signes échographiques de dysfonction ventriculaire droite dans l’EP submassive.
La première étape du diagnostic chez les patients suspects d’EP non massive repose sur l’évaluation de la probabilité clinique, suivie d’un dosage des D-dimères chez les patients non hospitalisés. Un dosage de D-dimères négatif (< 500 µg/l) permet d’écarter le diagnostic d’EP.
Les patients hospitalisés et les patients ambulatoires ayant un taux de D-dimères élevés, doivent bénéficier d’un scanner spiralé. Cette étape confirme le diagnostic en cas de visualisation d’un thrombus proximal, mais ne permet pas d’écarter le diagnostic d’EP en cas de scanner spiralé normal.
Il convient dans ce cas de réaliser une échographie veineuse des membres inférieurs. La confirmation d’une TVP chez un patient suspect d’EP justifie que soit débuté le traitement anticoagulant sans autre examen.
Le recours à l’angiographie pulmonaire se limite aux patients ayant un scanner négatif et une échographie veineuse normale, associés à une probabilité clinique élevée.
En cas de signes cliniques de TVP, l’échographie veineuse des membres inférieurs peut être réalisée avant le scanner spiralé.
Dans cet algorithme, les indications de scintigraphie pulmonaire se limitent aux patients allergiques aux produits de contraste, à ceux ayant une insuffisance rénale, ou en cas de grossesse évolutive.
L’existence de signes échographiques de cœur pulmonaire aigu chez un patient suspect d’EP massive avec état de choc peut justifier de débuter une fibrinolyse sans autre confirmation diagnostique.
En pratique
Les stratégies diagnostiques actuelles de l’EP comportent :
- l’évaluation de la probabilité clinique,
- le dosage des D-dimères,
- l’échographie de compression veineuse des membres inférieurs,
- le scanner spiralé,
- et, en dernier recours, l’angiographie pulmonaire.
La scintigraphie de ventilation-perfusion, qui a été pendant de nombreuses années la clé de voûte diagnostique, est aujourd’hui supplantée par le scanner spiralé mais garde tout son intérêt pour les patients avec insuffisance rénale, allergie aux produits de contraste iodés, ou au cours de la grossesse et de la surveillance de l’efficacité du traitement mis en œuvre.
L’évaluation de la probabilité clinique est fondamentale car elle permet de sélectionner, parmi les patients ayant une prévalence élevée d’EP, ceux qui nécessiteront en cas d’examens non invasifs négatifs, la réalisation d’une angiographie pulmonaire.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :