Valvulopathies
Publié le 01 juin 2010Lecture 14 min
Implications pronostiques et techniques chirurgicales de l'insuffisance mitrale ischémique
E. MESSAS(1) C. SZYMANSKI(1,2), C. TRIBOUILLY(2), A. HAGEGE(1), (1) Hôpital Européen Georges Pompidou, Paris, (2) CHU Amiens Sud
La présence en postinfarctus d’une fuite mitrale fonctionnelle secondaire au remodelage ventriculaire, double la morbi-mortalité cardiovasculaire à long terme. Le risque opératoire de ce type de fuite est plus élevé car survenant par définition sur cœur infarci avec le plus souvent dysfonction ventriculaire gauche. La technique chirurgicale de référence est l’annuloplastie sous-dimensionnée préconisée par Steven Bolling ; elle donne des résultats variables à long terme avec un pourcentage important de récidive (jusqu’à 30 %).
Afin d’améliorer le résultat de la réparation mitrale et de diminuer son risque opératoire de nombreuses techniques chirurgicales ou de cardiologie interventionnelle alternatives ont vu le jour ciblant plus précisément le remodelage ventriculaire. Elles ont pour ambition d’améliorer in fine le pronostic de ces patients.
L’avènement de la plastie mitrale a révolutionné le pronostic et la prise en charge des fuites mitrales organiques(1). Cependant, ces résultats, valables pour la fuite mitrale organique, restent encore décevants pour la fuite mitrale fonctionnelle du postinfarctus surnommée « insuffisance mitrale ischémique » (IMI). Cette fuite apparaît, par définition, sur une valve structurellement normale et son mécanisme est directement lié au remodelage ventriculaire du postinfarctus. Sa fréquence importante (20 % des infarctus) et sa gravité (doublement de la mortalité tardive(2)) souligne l’intérêt potentiel de l’amélioration des moyens de détection et de prise en charge de ce type de fuite.
Épidémiologie et pronostic
L’évaluation de la fréquence et du pronostic de l’IMI pose un problème évident de méthodologie avec de nombreuses études sur le sujet, pour la plupart rétrospectives avec des méthodes d’évaluation différentes. En phase aiguë d’infarctus, détectée à l’auscultation ou au Doppler, sa présence double la mortalité à un an(3). L’étude de la Duke University sur 1 480 patients avec détection de la fuite mitrale par angiographie à H6 de l’infarctus retrouve une mortalité de 52 % à un an chez les patients avec IM > grade 2 et une mortalité cardiovasculaire double de celle des patients avec IM < grade 2(4).
En phase subaiguë, un sous-groupe de l’étude SAVE avec fuite mitrale détectée par angiographie dans les 16 jours de l’infarctus a été étudié par Lamas(2). Ces 727 patients ont une fraction d’éjection (FE) < 40 % et présentent en moyenne une IM modérée qui, dans plus de 90 % des cas, n’est pas détectée à l’auscultation.
Ces patients ont aussi un terrain plus grave avec un taux plus important d’infarctus récidivants, d’atteintes pluritronculaires, d’infarctus postérieurs et sont plus souvent de sexe féminin et plus âgés.
Au niveau ventriculaire, il existe une dilatation plus importante des volumes télédiastoliques et télésystoliques avec index de sphéricisation plus élevé alors que la FE et la pression télédiastolique ventriculaire gauche (PTDVG) restent identiques à celles du groupe sans fuite mitrale. À 4 ans, il existe une augmentation significative de la mortalité cardiovasculaire dans le groupe fuite mitrale (figure 1). Ces résultats ne sont pas influencés par la prise d’inhibiteurs de l’enzyme de conversion.
Figure 1. Signification pronostique et survie post-IDM en fonction de la présence d’une fuite mitrale ischémique. Sous-groupe de l’étude SAVE avec fuite mitrale détectée par angiographie dans les 16 jours de l’infarctus. À 4 ans, on note une augmentation significative de la mortalité cardiovasculaire dans le groupe avec IM (d’après Lamas GA, Circulation 1997; 96: 827-33). IMI = insuffisance mitrale ischémique.
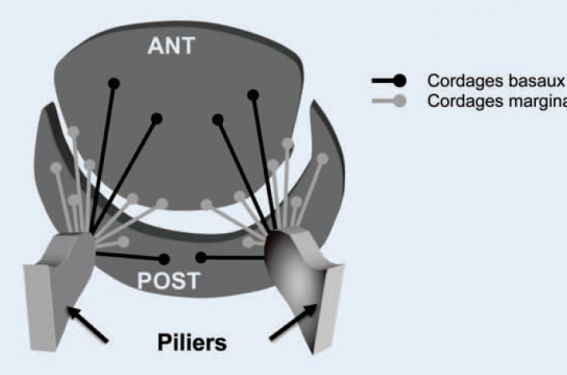
Figure 2. Classification des cordages de la valve mitrale. Les feuillets mitraux sont tenus par deux groupes de cordages : les cordages marginaux qui sont fins et s’attachent sur le bord libre des feuillets (leur rôle est de prévenir le prolapsus valvulaire) et les cordages basaux, plus épais, s’attachant sur le « corps » du feuillet près de sa base d’insertion.
En phase tardive du postinfarctus (à plus de 16 jours), une étude de la Mayo Clinic et l’équipe de Liège de Lancellotti et Piérard ont montré que l’IMI peut être considérée comme un marqueur de mauvais pronostic, mais il n’a encore jamais été clairement démontré que la correction de cette IM améliore le pronostic (lui donnant alors le statut de facteur de mauvais pronostic).
Aujourd’hui, on parle d’IM ischémique importante (en termes de pronostic), quand la surface de l’orifice régurgitant au repos est > 20 mm2 ou quand la surface de l’orifice régurgitant augmente de 13 mm2 à l’effort.
Traitement chirurgical de l’IMI fonctionnelle
En l’absence d’études randomisées, les indications chirurgicales et les techniques de correction de l’IMI restent encore controversées.
L’analyse des différentes séries publiées retrouve une mortalité opératoire significative allant de 5 à 10 % avec, quand la fuite mitrale régresse, une amélioration significative des symptômes et de la morbi-mortalité avec parfois amélioration de la FE(6). En cas d’indication à un pontage coronaire, on peut proposer d’y associer un geste sur la valve mitrale en cas de fuite mitrale significative (SOR > 20 mm2) avec fraction d’éjection VG > 30 %(6,7) (recommandation classe IC de l’ESC 2007).
Du fait de l’hétérogénéité de la présentation des patients avec IMI, il est difficile de comparer l’efficacité de la plastie à celle du remplacement valvulaire. La réalisation d’un remplacement valvulaire est préférée en cas d’équipe chirurgicale opérant peu d’IMI, de mécanisme complexe de l’IM (associant une restriction du feuillet postérieur et une dilatation annulaire avec fuite mitrale excentrée), de comorbidités importantes, de trouble de la cinétique segmentaire intéressant la paroi latérale et, enfin, en cas de « tenting » sévère des feuillets mitraux présageant d’une inefficacité de la réparation mitrale(7,8).
Le remplacement par prothèse valvulaire se fait avec préservation de l’appareil sous-valvulaire (fonction VG), impliquant moins de complications chez des patients dont le pronostic à long terme est déjà compromis.
L’annuloplastie sous-dimensionnée : le traitement de référence
L’annuloplastie mitrale sous-dimensionnée par anneau semi-rigide permet de rétablir une coaptation mitrale normale en corrigeant plus spécifiquement la dilatation postérieure de l’anneau. Cette technique semble être efficace initialement mais, dans 20 à 50 % des cas, la fuite mitrale récidive après quelques mois ou années pendant lesquels le remodelage ventriculaire continue de progresser(9). L’annuloplastie mitrale fusse-t-elle sous-dimensionnée, ne corrige qu’une partie des modifications géométriques de l’appareil sous-valvulaire mitral en cause dans l’IMI. Elle ne peut corriger le déplacement des piliers qui continue à progresser du fait du remodelage ventriculaire. Ainsi, Steve Bolling, l’un des partisans de l’annuloplastie sous-dimensionnée souligne que l’IM fonctionnelle est en fait une maladie ventriculaire(10). Califiore et coll. ont démontré que l’importance de la fuite résiduelle après annuloplastie est corrélée au degré de traction apicale des feuillets mitraux(11).
Par ailleurs, le sous-dimensionnement de l’anneau entraîne un déplacement antérieur du feuillet postérieur qui peut, par effet de bascule, favoriser le déplacement postérieur du pilier postéro-médial avec augmentation des forces de traction locales et aggravation paradoxale de la restriction du feuillet postérieur. D’après Llaneras, « Pour un nombre important de patients, le résultat de l’annuloplastie sous-dimensionnée est mitigé car la traction apicale exercée par les cordages sur les feuillets mitraux n’est pas corrigée par cette technique »(12).
Les résultats mitigés de cette technique ont motivé l’apparition de chirurgies alternatives ciblant le mécanisme prépondérant de cette fuite : le remodelage ventriculaire avec traction apicale des feuillets (apical tenting). Ces techniques alternatives ont pour but de diminuer l’excès de traction exercée par les cordages sur les feuillets mitraux en systole par :
- section des cordages basaux insérés sur les feuillets mitraux pour diminuer la restriction des feuillets et augmenter la surface de coaptation mitrale(13) ;
- repositionnement des piliers vers l’anneau mitral par différentes procédures : plicature de la zone sous-jacente aux piliers, ou insertion d’un patch à la base du pilier(14,15).
Section des cordages basaux chordal cutting : une technique déjà utilisée en pratique
Cette nouvelle approche proposée par Messas et coll. consiste à sectionner un nombre limité de cordages mitraux responsables de la restriction valvulaire, mais non nécessaires à la prévention du prolapsus(13).
L’analyse de l’anatomie de la valve mitrale et de ses modifications en cas d’IMI permet de mieux comprendre les effets de cette nouvelle thérapeutique. Les feuillets mitraux sont tenus par deux groupes de cordages : les cordages marginaux qui sont fins et s’attachent sur le bord libre des feuillets (leur rôle est de prévenir le prolapsus valvulaire) et les cordages basaux, plus épais, s’attachant sur le « corps » du feuillet près de sa base d’insertion (figure 3).
Le remodelage ventriculaire, en éloignant les piliers de l’anneau, augmente les forces de traction exercées par les cordages sur les feuillets mitraux (forces dirigées postéro-latéralement et vers l’apex ventriculaire). Ces forces sont donc maximales au centre du feuillet mitral antérieur qui modifie sa forme avec un aspect typiquement en « aile de mouette » présentant un segment basal immobilisé et tendu vers l’apex ventriculaire et un segment distal pivotant perpendiculairement et ne permettant qu’à l’extrémité du bord libre de se mettre en contact avec le feuillet postérieur. Cela entraîne une diminution de la surface de coaptation valvulaire et une fuite mitrale. La section des cordages basaux s’insérant sur le feuillet antérieur permet de réduire la tension exercée sur la grande valve en systole ; celle-ci retrouve une forme plus concave qui permet une augmentation de la surface de coaptation mitrale et une diminution de la fuite. Dans le même temps, les cordages marginaux, laissés intacts, préviennent la survenue d’un prolapsus valvulaire (figure 4)(13).
Figure 3. Mécanisme d’action de la section des cordages basaux. A gauche : Schéma de l’appareil valvulaire et sous-valvulaire mitral en conditions physiologiques : coaptation des deux feuillets valvulaires au niveau du plan de l’anneau, sans fuite mitrale. Au milieu : Schéma du mécanisme d’IMI avec traction apicale des feuillets prédominant sur le centre du feuillet antérieur avec angulation entraînant une malcoaptation et fuite mitrale. A droite : Schéma du mécanisme d’action du chordal cutting : après section des cordages basaux, disparition de l’angulation et augmentation de la surface de coaptation avec disparition de la fuite. VG = Ventricule Gauche, OG = Oreillette Gauche, AO = Aorte, IM = Insuffisance Mitrale.
Figure 4. Description de la technique de plicature : plicature de la zone infarcie par trois séries de sutures transversales liées par deux sutures longitudinales, permettant de faire régresser l’expansion de la zone infarcie et de repositionner le pilier vers l’anneau mitral (d’après Liel-Cohen N, Circulation 2000; 101: 2756-63).
L’efficacité et l’innocuité de cette technique ont été testées expérimentalement.
Dans une étude chez l’homme récente, Borger et coll. ont appliqué cette technique chez 43 patients qui présentaient une cardiopathie ischémique avec troubles de cinétique segmentaire et fuite mitrale importante(16). Les auteurs ont comparé l’efficacité de la section des cordages des deux feuillets + annuloplastie partielle vs annuloplastie seule. Cette étude a montré une réduction significative du taux de récidive d’IM en faveur du groupe section de cordage après 2 années de suivi (37 % dans le groupe annuloplastie vs 15 % dans le groupe section de cordages, p = 0,03). La section des cordages basaux des deux feuillets associée à l’insertion d’un anneau prothétique, a permis une normalisation de la cinétique des feuillets. Il n’a pas été constaté de prolapsus valvulaire mitral ni de dégradation de la fonction ventriculaire secondaire à la section des cordages.
Wakiyama et coll. ont aussi appliqué cette technique chez des patients avec dysfonction VG globale et fuite mitrale ischémique sévère avec des résultats qui semblent prometteurs(17).
Repositionnement des piliers mitraux : une technique encore expérimentale
L’intérêt du repositionnement des piliers dans l’IMI est double : faire régresser de façon effective la fuite mitrale (ce qui diminue indirectement le remodelage) et avoir un effet antiremodelage direct par son effet de contrainte externe indépendamment de son effet sur l’IM. Les premières tentatives de repositionnement des piliers ont consisté en une incision de la partie infarcie avec ouverture et réimplantation des piliers en zone saine(20). Expérimentalement, on peut faire régresser la traction apicale des feuillets en modifiant la forme de la zone d’insertion des piliers par plicature de la zone infarcie permettant une régression du remodelage local(21) ou par application d’un patch avec ballon, dont l’expansion peut être guidée par échographie cardiaque(22).
Ces deux approches expérimentales ont pour but de rapprocher le pilier de l’anneau mitral antérieur afin de diminuer les forces de traction et la fuite mitrale.
Plicature ventriculaire gauche
Liel Cohen en écho 3D a démontré que la distance pilier-anneau mitral est le paramètre le plus puissant de prédiction de la fuite mitrale(21). À partir de ces résultats, l’équipe de Levine a décrit une technique chirurgicale permettant de rapprocher le pilier vers le plan de projection de l’anneau mitral diminuant ainsi la distance pilier-anneau mitral et améliorant la coaptation et la fuite. Cette technique consiste à plicaturer la zone infarcie par trois séries de sutures transversales liées par deux sutures longitudinales, évitant les coronaires, ce qui permet de faire régresser l’expansion de la zone infarcie et de repositionner le pilier vers l’anneau mitral (figure 5).
Figure 5. Mécanisme d’action du ballon-patch. L’inflation du ballon guidée par échographie permet de rapprocher le pilier vers l’anneau mitral avec diminution des forces de traction et amélioration de la coaptation (d’après Hung J, Circulation 2004 ; 110 : II85-II90).
Cette technique a été testée sur 10 moutons avec infarctus inféro-latéral qui ont développé une fuite mitrale ischémique au bout de 8 semaines. La plicature fait régresser la fuite parallèlement à la diminution de la distance pilier-anneau mitral (p < 0,0001), alors que la FE, le volume télésystolique et la surface de l’anneau mitral ne varient pas de façon significative. Ces résultats persistent 2 mois après la chirurgie. Le seul facteur prédictif de la fuite mitrale est la distance pilier-anneau mitral.
Application d’une contrainte externe
Une autre solution à cœur battant est l’application d’un dispositif externe qui repositionne les piliers et réduit la fuite mitrale(22). Un patch en dacron est placé à cœur battant sur la région du pilier infarci et un ballon est inséré entre le patch et le myocarde. L’inflation du ballon permet de déplacer antérieurement le pilier postérieur vers l’anneau mitral avec diminution de la traction des feuillets sous visualisation échocardiographique (figure 6).
Les contraintes externes passives utilisées ici pour traiter l’insuffisance cardiaque sont en général bien tolérées et n’entraînent pas de constriction. Elles sont bénéfiques sur le remodelage VG et l’expansion de la zone infarcie. L’augmentation de contractilité retrouvée après patch + ballon dans cette expérience est comparable à celle retrouvée après ventriculotomie partielle(23).
Figure 6. Description des insertions du dispositif Coapsys (d’après Fukamachi K, ASAIO J 2005; 51:17-21). A gauche : Haut : visualisation de l’insertion de l’électrode et rapports avec la circonflexe. Bas : visualisation de l’insertion des électrodes antérieure et postérieure et rapports avec l’artère coronaire droite et la circonflexe. A droite : Haut : Vue chirurgicale du petit axe ventriculaire en coupe transmitrale : Localisation de l’extrémité postérieure du dispositif au niveau de l’anneau en regard du segment médian de la petite valve. Bas : Coupe grand axe du VG avec visualisation de la tige transventriculaire du dispositif se positionnant sous les feuillets mitraux. L’extrémité antérieure s’insère sur le septum interventriculaire sous l’insertion ventriculaire droite.
Cx = Circonflexe, CD = Coronaire Droite, FMA = Feuillet Mitral Antérieur, FMP = Feuillet Mitral Postérieur
Ainsi, un dispositif externe placé au niveau de la zone infarcie peut faire régresser la distance de traction des feuillets et la fuite mitrale en ajustant par échographie le niveau d’inflation du ballon à la forme de la valve mitrale. Cette technique a l’avantage d’éviter une CEC et pourrait pallier la variabilité des résultats observés après annuloplastie. Ce patch pourrait éventuellement être étendu jusqu’à l’anneau mitral afin de corriger une dilatation annulaire concomitante.
Système Coapsys
Une technique testée par l’équipe de Fukamachi utilise le dispositif Coapsys® (Myocor, Inc, Maple Grove, Minnessota)(24). Il autorise une approche trans-péricardique, ne nécessitant ni auriculotomie ni circulation extracorporelle. Il consiste à implanter deux palettes épicardiques antérieure et postérieure, reliées par une tige transventriculaire. Le principe est de diminuer le diamètre antéro-postérieur ventriculaire et annulaire en rapprochant le pilier du plan de projection de l’anneau mitral, diminuant ainsi les forces de traction et la fuite mitrale (figure 7). À un an, on retrouve une nette diminution de la fuite mitrale dans le groupe Coapsys (degré de la fuite à un an : 1,15 ± 0,99 vs 2,00 ± 0,82 dans le groupe contrôle, p < 0,05).
Ces résultats intéressants doivent être confirmés par de futures études multicentriques. Cependant, les images échographiques montrent une nette akinésie septale en regard du stabilisateur du dispositif. On sera donc attentif à la conservation de la FE dans les études futures.
Autres techniques chirurgicales
Plusieurs autres techniques adjuvantes ont été proposées dans la littérature afin d’améliorer les résultats de la plastie mitrale en cas d’IMI.
Les techniques d’exclusion de la zone infarcie par la procédure de Dorr ou de réduction ventriculaire peuvent, elles aussi, participer à la diminution de la fuite mitrale ischémique(25).
Certaines équipes préconisent une extension de la hauteur du feuillet postérieur avec pose d’un patch péricardique à la base du feuillet afin d’améliorer la coaptation et pérenniser les résultats de l’annuloplastie mitrale.
Plus récemment, un nouvel anneau prothétique développé par le Pr Carpentier (Carpentier-McCarthy-Adams IMR ETlogix®) et dédié au traitement de l’IMI a fait son apparition dans le domaine clinique(26). Ses caractéristiques répondent aux mécanismes de la fuite mitrale ischémique. Il permet de corriger l’augmentation de diamètre antéro-postérieur de l’anneau et l’aspect asymétrique de l’IM prédominant au niveau de la commissure postérieure. En effet, il présente un aspect asymétrique avec un ratio diamètre antéro-postérieur sur diamètre inter-commissural plus faible et une épaisseur accentuée au niveau de son insertion postérieure. Les résultats postopératoires immédiats et à 6 mois semblent être prometteurs.
Traitement percutané de l’IMI fonctionnelle
Ce thème justifiant à lui seul un article à part entière ; on se limitera à mentionner les deux techniques dont le développement est le plus avancé : l’annuloplastie percutanée(34) et la technique utilisant le dispositif Evalve(28).
L’annuloplastie percutanée utilise le sinus coronaire comme site de réception du dispositif et a pour but de diminuer le diamètre antéro-postérieur de l’anneau mitral afin d’améliorer la coaptation des feuillets mitraux et diminuer ainsi la fuite mitrale. Après quelques problèmes techniques liés aux dispositifs et à l’atteinte de l’artère circonflexe proche, une étude de phase II est en cours de recrutement.
Le dispositif Evalve consiste à clipper la partie centrale des deux feuillets de façon percutanée, selon le même principe que la technique chirurgicale d’Alfieri (Edge to Edge repair). Cette technique est en cours d’évaluation avec une étude de phase II randomisée, multicentrique EVEREST 2 comparant l’efficacité de cette approche à la chirurgie mitrale conventionnelle(28). La phase de recrutement a été récemment terminée avec plus de 250 patients inclus.
Si ces alternatives thérapeutiques moins invasives semblent séduisantes, elles ne sont pas simples à réaliser techniquement et nécessitent un temps d’apprentissage non négligeable. Il est donc raisonnable d’attendre les données à plus long terme de ces dispositifs afin de mieux identifier la population cible de patients pouvant bénéficier de ce type de traitement.
En pratique
L’insuffisance mitrale ischémique fonctionnelle ne doit pas être sous-estimée car elle aggrave le pronostic des patients en postinfarctus. Son apparition est secondaire au remodelage ventriculaire gauche, qu’elle majore à son tour par sa présence, créant ainsi un véritable cercle vicieux qui rend sa prise en charge thérapeutique difficile. Le traitement médical de cette fuite mitrale est souvent insuffisant.
L’annuloplastie avec anneau semi-rigide sous-dimensionné reste la technique de référence. Cette technique est, certes, efficace initialement mais, dans de nombreux cas, la fuite mitrale récidive au bout de quelques mois ou années. L’émergence de nouvelles techniques de réparation valvulaire chirurgicales, guidées par la meilleure compréhension des mécanismes de l’IM ischémique, permettra, on l’espère, d’améliorer dans un avenir proche, le pronostic de ces patients.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :







