Prévention et protection
Publié le 20 nov 2007Lecture 6 min
Pré- et postconditionnement : deux approches de la protection myocardique - De la réalité expérimentale aux espoirs cliniques
L. ROCHETTE, C. VERGELY, M. ZELLER et Y. COTTIN* LPPCE, Faculté de Médecine, Dijon
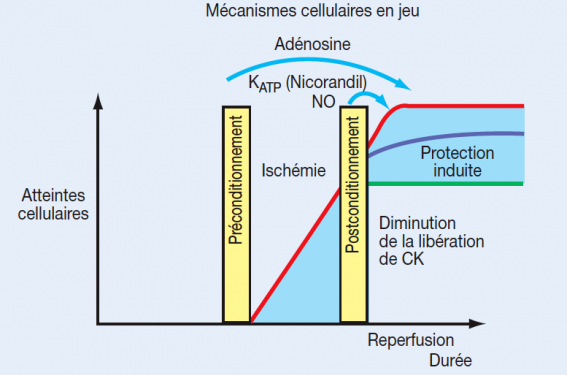
Le fait que le myocarde subisse des ischémies itératives de courtes durées, avant un épisode d’ischémie prolongé, conduit à une protection du myocarde : en l’occurrence, une limitation de l’amplitude des atteintes. On peut alors envisager que le myocarde est capable de « mémoriser » des événements intimes qui vont mettre en jeu des défenses vis-à-vis d’une situation à venir hautement délétère. Mais il apparaît deux situations tout à fait différentes :
• le préconditionnement avec une sollicitation des défenses qui précèdent l’ischémie réversible,
• le postconditionnement avec une sollicitation de défenses (identiques ou différentes) qui sont mises en jeu immédiatement lors de la reperfusion (figure 1).
Le pré-conditionnement
De nombreuses approches expérimentales ont été envisagées afin de mieux préciser les conditions dans lesquelles ce préconditionnement était efficace. Il faut bien noter que l’installation de cette protection n’est efficace que dans des conditions spaciales et temporelles très précises, et en particulier, si la reperfusion survient dans des délais bien définis.
Il est surprenant de constater que de nombreuses situations mécaniques, physiologiques ou pharmacologiques sont capables d’induire un préconditionnement. Que ce soit des stimulations de récepteurs (exemples adrénergiques) ou l’inhibition de ces mêmes récepteurs, dans les deux cas, on aboutit à une protection myocardique. Il a été évoqué que toute modification d’un « état » de la cellule qui met en éveil des processus d’alerte par l’intermédiaire de relais intimes de type protéique (protéines de stress : HSP) ou non protéiques (voies de sauvegarde ou de sécurité), conduit à un préconditionnement. Les mécanismes mis en œuvre sont multiples (tableau 1) mais trois voies prioritaires pourraient être décrites :
• l’adénosine qui apparaît comme un composé cardioprotecteur majeur ; récemment une revue (Peart and Headrick)(2) a fait le point sur le rôle des récepteurs à l’adénosine de type A1, A2A, A2B et A3 ;
• la protéine kinase PKC apparaît également jouer un rôle « charnière » dans la médiation (Obadia et Coll.)(3). En effet, les antagonistes de la PKC abolissent la limitation de l’infarctus suite au préconditionnement, alors que les activateurs reproduisent un effet bénéfique ;
• enfin, le rôle de canaux mitochondriaux de type KATP a été démontré dans de nombreuses études, mettant en jeu des régulations des homéostasies ioniques, en particulier du calcium et du potassium. Il apparaît aussi que ces canaux modulent la transition de perméabilité membranaire mitochondriale. Ce processus associé à l’ouverture irréversible d’un pore au sein de la membrane interne de la mitochondrie, pourrait constituer un starter majeur dans l’initiation du processus de mort cellulaire par apoptose. De nombreuses études utilisent le glibenclamide, un antagoniste des canaux potassiques ATP-dépendant, qui bloque le préconditionnement. Des données cliniques intéressantes, associées au concept du préconditionnement, ont été rapportées dans l’étude de Ikeda et al., qui avait mis l’accent sur le bénéfice apporté par le nicorandil comparativement au dinitrate d’isosorbide administré immédiatement après angioplastie sur la récupération fonctionnelle. L’effet sur la normalisation du segment ST était significativement plus marqué dans le groupe nicorandil que dans le groupe nitré(4).
Si, sur le plan expérimental, le préconditionnement est le processus le plus performant et surtout le plus facile pour limiter la taille de l’infarctus. En revanche, l’extrapolation aux situations cliniques est réellement impossible car les patients hospitalisés suite à un infarctus du myocarde présentent déjà tous les signes d’une souffrance myocardique constituée. On ne peut malheureusement pas « remonter le temps ».
Le post-conditionnement
Plus récemment, en 2003, Zhao et coll.(5) ont décrit un nouveau concept de protection myocardique : le postconditionnement. Dans ce cadre, des ischémies itératives qui font suite à un épisode d’ischémie réversible de longue durée susceptible d’induire des altérations du myocarde, vont entraîner une limitation du processus d’atteintes irréversibles. Le phénomène de postconditionnement présente, lui, un intérêt clinique majeur ; en effet, il est possible d’envisager la mise en place d’un protocole clinique de postconditionnement lors de la reperfusion coronaire par angioplastie réalisée dans la phase aiguë de l’infarctus du myocarde.
Sur le plan clinique et de l’effet protecteur du postconditionnement, il est important de rappeler l’étude pilote publiée en 2005 par Laskey(6). Son objectif, bien défini, était d’explorer les conséquences physiologiques d’un postconditionnement, c’est-à-dire une intervention durant la phase initiale de la reperfusion, chez des patients présentant un infarctus du myocarde, qui bénéficiaient d’une dilatation. Le protocole adopté était le suivant : le ballonnet était avancé jusqu’au segment sténosé et une séquence d’inflation/déflation était réalisée avec des périodes de reperfusion de quelques minutes (3 à 5 minutes). Sur cette petite série, l’auteur démontrait déjà un impact favorable du postconditionnement sur la résolution du segment ST. Sur ce protocole, et compte-tenu des paramètres fonctionnels et biologiques qui étaient étudiés, Laskey concluait son article par cette phrase : « Briefs periods of balloon occlusion followed by reperfusion during percutaneous coronary intervention for acute myocardial infarction (ischemic conditioning) accelerate the rate of ST segment resolution ». Les modalités de réalisation du conditionnement ischémique différaient toutefois de celui qui avait été adopté par Zhao et coll.(5) et Kin et coll.(7).
L’intérêt clinique majeur du postconditionnement s’est confirmé par l’étude de Staat et coll.(8), qui a d’ailleurs fait l’objet d’un commentaire dans Circulation de W.-K. Laskey félicitant les auteurs de ce travail pour la pertinence et l’élégance du protocole adopté. L’étude de Staat et coll. a été conduite dans les CHU de Lyon, Montpellier et Dijon. Le protocole de postconditionnement adopté lors d’une angioplastie coronaire chez des patients souffrant d’un infarctus du myocarde, a consisté en 4 épisodes d’inflation/déflation durant les 8 premières minutes de reperfusion (4 réinflations de 1 min séparées par 1 min de reperfusion). Ce choix était dicté à partir de certaines données expérimentales et la perfusion myocardique était évaluée par la cinétique des concentrations plasmatiques en CK durant les 72 h. L’âge des patients (56 ± 3 ans) était voisin de celui des patients de l’étude de Laskey (58 ± 12 ans), les temps qui séparent l’installation de la douleur de la reperfusion étaient également voisins : 341 ± 181 min dans l’étude Laskey et 318 ± 38 min dans l’étude de Staat et coll. L’étude de Staat et coll. a montré que l’aire sous la courbe de la libération de CK était réduite de 36 % par rapport aux patients « témoins » ne profitant pas d’un postconditionnement ischémique.
Parallèlement à cette approche « mécanique », de nombreuses études expérimentales ont bien montré que l’adénosine et les canaux KATP sont impliqués dans les mécanismes qui sous-tendent le postconditionnement ischémique. Il est possible d’envisager une utilisation potentielle de ces approches pharmacologiques dans la phase postischémique en clinique (Kloner and Rezkalla)(9) (figure 1).
Figure 1. Le pré- et postconditionnement en clinique.
Le pré- et le postconditionnement
Dans les mécanismes d’initiation de phénomènes délétères myocardiques et/ou de protection des cardiomyocytes, le rôle des espèces radicalaires est régulièrement évoqué. Alors que le préconditionnement ischémique ou induit par le TNF-alpha met en jeu une sollicitation de la production radicalaire (Lecour et coll.(10)). En revanche, le postconditionnement serait associé à une réduction de la production radicalaire durant les épisodes itératifs d’ischémie-reperfusion (figure 2). Il apparaît donc une distorsion entre les mécanismes mis en jeu dans le préconditionnement et ceux associés au postconditionnement, si l’on considère des niveaux de stress oxydatif radicalaire.
Figure 2. Pré- et postconditionnement : deux processus conduisant à une limitation des atteintes cellulaires associées à une séquence ischémie-reperfusion.
Enfin, une composante expérimentale importante doit être notée dans cette protection liée au pré- ou postconditionnement. En effet, des cœurs isolés perfusés, donc non soumis à influence nerveuse et hormonale, sont capables d’être préconditionnés et postconditionnés. Le myocarde possède donc de manière endogène tous les processus susceptibles d’initier cette cardioprotection.
Conclusion
Depuis la description du préconditionnement par l’équipe de Jennings, de nombreuses questions ont été posées, de nombreuses réponses ont été apportées, mais l’adéquation entre les faits expérimentaux et les applications cliniques est difficile à établir. L’ouverture clinique existe, mais elle doit maintenant être renforcée pour préciser dans quelles conditions le cœur humain soumis à une séquence ischémie-reperfusion peut être protégé à court terme et à plus long terme par un postconditionnement, qu’il soit de type ischémique ou pharmacologique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :







