Mise au point
Publié le 01 déc 2021Lecture 4 min
Ablation par ballon laser dans la fibrillation auriculaire
Cyrus MOÏNI, Antony et Denis AMET, Paris
La prévalence et l’impact de la fibrillation atriale (FA) augmentent à l’échelle mondiale, obligeant à mettre l’accent sur l’amélioration des techniques d’ablation grâce à l’innovation. Ainsi, une nouvelle source d’énergie, le laser, déjà utilisée dans le domaine de l’extraction des sondes endocavitaires, a été proposée pour l’isolation antrale des veines pulmonaires.
Les techniques alternatives à la radiofréquence (RF) telle la cryothérapie (CR) ou le laser font suite essentiellement à deux écueils : une courbe d’apprentissage longue et des délais de procédures prolongés.
L’efficacité clinique et les effets indésirables semblent comparables à la RF des FA paroxystiques (FAP) voire persistantes (FAPe)(2,3).
Technique
Le système d’ablation endoscopique laser de 3e génération (HeartLight, CardioFocus) est le seul dispositif actuellement disponible sur le marché et se compose : d’une gaine (12 F), d’un ballon gonflable et d’une fibre optique délivrant une énergie laser. Par ailleurs, la navigation et l’identification du site des lésions se font par une visualisation anatomique directe via un endoscope incorporé de 2 F. L’ensemble (figure 1) est relié à une console qui permet de contrôler :
– la source lumineuse,
– le système d’affichage visuel endoscopique,
– la puissance et la durée d’application du laser,
– la taille et la forme du ballon : elles sont également ajustées par l’opérateur afin de traiter des veines(4) de 8 à 40 mm.
Figure 1.
L’énergie laser est émise perpendiculairement au cathéter via un générateur de lésions qui traite les tissus de façon circonférentielle en mode manuel ou automatique en couvrant un arc de 30°. Ce générateur de lésions est logé dans le ballon et utilise l’oxyde de deutérium (D2O) comme fluide de gonflage et de conduction(5) tout en évitant l’autoéchauffement. L’énergie délivrée varie de 5,5 à 15 W pour des durées d’application de 20 à 30 secondes en réglage manuel.
Le traitement laser agit selon 3 réactions :
• Photochimique avec inactivation cellulaire sans augmentation de température.
• Photothermique avec conversion de l’énergie lumineuse en chaleur par le tissu.
• Photoplasmique avec rupture tissulaire par ondes de choc.
L’ablation laser s’effectue par application d’un faisceau d’énergie photonique ciblé de façon séquentielle ou continue sur la surface antrale proximale des VP. La particularité de cette technologie est d’éviter la lésion de l’endothélium et, par voie de conséquence, la formation de caillots et le risque thromboembolique. Par ailleurs, la visualisation anatomique via le fibroscope réduit le risque de reconnexion et de sténose pulmonaire(6).
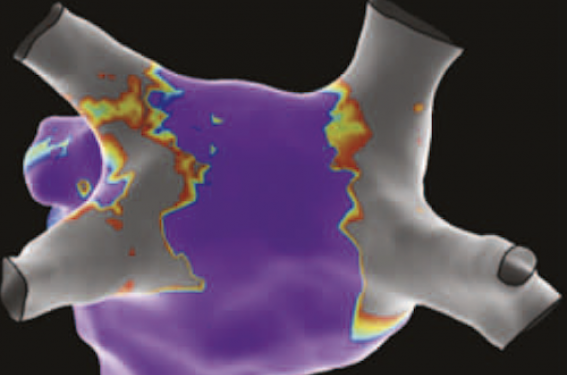
La figure 2 illustre l’une de nos procédures pour laquelle nous avons couplé une cartographie 3D à la vue anatomique (fibroscope) et radioscopique afin de valider l’efficacité de la lésion postablation. On distingue l’ensemble du matériel mis en place ainsi que la bonne déconnexion des VP (ici la VPSG).
Figure 2.
Résultats cliniques
Une métaanalyse portant sur 17 publications de 2018(3) regroupant 1 188 patients a retrouvé un taux de succès initial de 98,8 % (âge moyen 61 ans, 80 % de FAP). Le suivi note l’absence de récidive à 12 mois dans 74,3 % des FAP (IC 95% : 59,9-86,4) et 72,9 % des FA combinées (65,3 à 79,9). La complication perprocédure rapportée est une atteinte du nerf phrénique dans 2,6 % (IC 95 % : 1,4-3,9).
Deux facteurs identifiés permettent d’optimiser la réussite d’une procédure d’IAVP par laser : l’apposition adéquate du ballon à l’ostia des VP et un haut niveau d’énergie utilisé. Un taux de succès d’ablation de près de 90 % est retrouvé lors de l’application de 8,5 W sur la paroi postérieure et de 10 W en antérieur sans majoration du risque de dommages œsophagiens(7).
Des études comparatives laser versus RF et CR rapportent des résultats prometteurs. Une étude de non-infériorité incluant 353 patients atteints de FA résistante au traitement médical note une récurrence symptomatique à 12 mois similaire dans les deux groupes (laser : 61,1 % vs RF : 61,7 %) et un taux de complication identique avec néanmoins une sténose VP inférieure (0 % vs 2,9 % ; p = 0,003). Cette même étude confirme une courbe d’apprentissage rapide pour le laser(8).
Dans l’étude RATISBONA, 50 patients atteints de FAP ont été randomisés en deux groupes (laser vs RF) pour analyser les connexions dormantes ou reconnexions à la phase aiguë par l’utilisation de l’APT (adenosine provocation test). Le résultat penche en faveur du laser (10,8 vs 30,9 %)(9).
Enfin, une étude européenne multicentrique sur 135 patients en FAPe (durée médiane 14 mois) a comparé laser et RF(10). Le critère principal était l’absence de récidive entre 90 jours et 1 an. Aucune différence n’a été relevée (laser : 71,2 % vs RF : 69,3 % ; p = 0,4). Il en va de même pour le taux de complications.
Une métaanalyse portant sur 595 patients comparant laser et CR note un taux de récidive à 1 an légèrement plus faible (p=0,09) mais un temps de procédure plus long pour le laser(11).
D’autres objectifs tels le temps de procédure et l’exposition aux rayons devront être évalués. Bien sûr, d’autres technologies sont en cours d’étude dont l’ablation à haute puissance et courte durée ainsi que l’électroporation.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


