Publié le 15 déc 2018Lecture 7 min
Resynchronisation par sonde ventriculaire gauche endocardique - Expérience monocentrique
Christophe D’IVERNOIS, Lofti LAROUCHI, Jean-Paul BERNIS, Nicolas LEGROS, J.-T. AUBERT, CH de la Côte Basque, Bayonne
La resynchronisation est un traitement validé de l’insuffisance cardiaque avec altération sévère de la fonction systolique VG et bloc de branche gauche (BBG)(1). Il existe toutefois un certain nombre de situations où le traitement ne peut être appliqué du fait de l’impossibilité de trouver un site stable dans une branche du sinus coronaire, avec un seuil de stimulation acceptable à long terme.
Dans ces cas, il a pu être proposé d’implanter, la sonde VG en endocardique après un abord transseptal auriculaire(2). Nous rapportons ici notre expérience de cette approche.
Observation
M. Min-Da a présenté en 2001, à 51 ans un infarctus antérieur étendu. En 2008, au décours d’une tachycardie ventriculaire soutenue, du fait d’une fraction d’éjection (FE) à 26 % et d’un BBG complet, un défibrillateur est implanté avec resynchronisation (CRT-D), du côté gauche.
En 2010, devant une menace d’extériorisation l’ensemble du matériel est retiré. Le patient est réimplanté du côté droit avec un défibrillateur double chambre car il est impossible de placer une nouvelle sonde dans une veine coronaire.
Pendant 6 ans, l’évolution sera stable et satisfaisante (NYHA 2) mais en juin 2016, le patient consulte en stade 4 NYHA. L’échocardiographie montre un diamètre télédiastolique VG (DTDVG) de 65 mm, une OG à 57 mm, une FEVG à 12 %, une vaste akinésie antéro-septoapicale, une insuffisance mitrale (IM) de grade 4/4, et un temps de remplissage VG réduit à 25 % du cycle RR.
On propose au patient une réintervention pour ajouter une sonde de stimulation VG endocardique, en se référant à la technique Jurdham(3). Brièvement, après abord axillaire veineux droit on descend un lasso dans la veine cave inférieure. Par un abord veineux fémoral droit, on passe un guide à travers la boucle du lasso puis on ponctionne le septum inter-auriculaire et une gaine Mullins 12 F de 65 cm est placée dans l’OG puis le VG. Une sonde Medtronic CapSureFix 5076 de 85 cm à l’extrémité proximale de laquelle est fixée une suture de 2 m de long est vissée en paroi latérale VG après vérification de bons paramètres électriques. La gaine Mullins est retirée jusque dans la veine iliaque primitive en même temps que la sonde est poussée hors de la gaine par son dilatateur. Lorsque la sonde est entièrement sortie de la gaine, la boucle du lasso est serrée sur la suture et le lasso est retiré progressivement, ce qui permet à l’extrémité proximale de la sonde de sortir par l’introducteur valvé axillaire droit de 10,5 F. La suture est sectionnée et la sonde de stimulation endocardique est reliée au port VG d’un CRT-D.
Le patient a accepté l’intervention qui a été réalisée le 26 juillet 2016, sous anesthésie générale, sans complication (onde R VG 17 mV, seuil VG 0,4 V, durée 3 h 30, scopie 32 mn). Le patient étant déjà sous warfarine pour sa fibrillation auriculaire (FA), on a insisté pour équilibrer l’INR entre 2,5 et 3,5.
Deux mois plus tard, le patient était transformé, à nouveau en stade 2 NYHA. Les QRS stimulés mesuraient 156 ms, le seuil VG est à 0,7 V, avec 99 % de stimulation biventriculaire. L’INR était autour de 3,5. À 6 mois, la FE était calculée à 25 % avec une IM grade 2/4. À 1 an, on a observé quelques brefs passages en FA asymptomatiques. À 2 ans, la FA est devenue quasi permanente depuis 3 mois, mais est restée bien tolérée (NYHA 2).
Notre expérience de la resynchronisation avec une sonde VG endocardique
De décembre 2014 à novembre 2016, cinq patients ont bénéficié dans notre centre d’une resynchronisation par sonde VG endocardique implantée selon la technique Jurdham(3). Il s’agissait de 5 hommes, d’âge moyen 71 ± 6 ans, en stade NYHA 3 (2 cas) ou 4 (3 cas). La cardiopathie était ischémique 4 fois, et rythmique 1 fois. La FE était de 17 ± 3 %, le DTDVG de 67 ± 6 mm. Deux patients étaient en FA permanente ; les QRS étaient le plus souvent stimulés par la sonde VD chez 4 patients (206 ± 9 ms) ou spontanés à type de BBG (200 ms) chez 1 patient. Quatre étaient sous anti-vitamine K avant l’intervention pour des antécédents de FA. L’indication de la sonde VG endocardique était liée 2 fois à l’impossibilité anatomique d’accéder à une veine coronaire, 1 fois à une instabilité répétée de la sonde, 2 fois à une élévation récidivante du seuil VG épicardique. L’abord pectoral était réalisé 3 fois du côté droit et 2 fois à gauche. Quatre fois il s’agissait d’une reprise chirurgicale, une fois d’une primo-implantation. La procédure était réalisée 4 fois sous anesthésie générale, 1 fois sous sédation profonde. Chez un patient, nous avons procédé dans le même temps opératoire à l’extraction de 2 anciennes sondes VG (l’une par voie haute, l’autre par voie basse). En peropératoire, la détection VG était mesurée à 14 ± 3 mV, le seuil VG à 0,8 ± 0,3 V. La prothèse était 2 fois un CRT-P, 3 fois un CRT-D. La durée de la procédure était de 214 ± 13 min, la durée de scopie de 31 ± 2 min.
Une tamponnade est survenue 1 heure après l’intervention, chez le patient le plus âgé (86 ans), le seul qui n’était pas anticoagulé préalablement ; malgré le drainage péricardique immédiat, le patient décèdera 24 heures plus tard de choc cardiogénique avec troubles de coagulation.
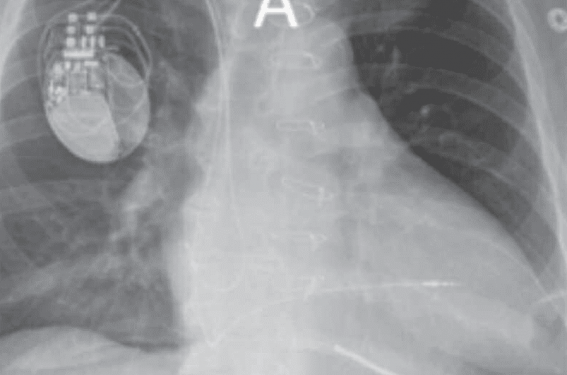
Les 4 autres patients ont pu quitter le service à J2-J4 (figures 1 et 2), le traitement par antivitamine K étant renforcé avec un INR cible entre 2,5 et 3,5. Un patient n’a pas montré d’amélioration clinique évidente et est décédé à M4 dans un tableau d’aggravation hémodynamique avec orage rythmique. Un deuxième s’est amélioré rapidement (NYHA 2) mais est décédé à M12 dans un tableau d’orage rythmique malgré une procédure d’ablation endo- et épicardique réalisée dans un centre expert. Enfin, les deux derniers patients sont toujours vivants et significativement améliorés 2 ans après l’intervention. Dans tous les cas, le seuil VG est resté inférieur à 1 V pendant le suivi et il n’y a pas eu de problème thromboembolique.
Figure 1. Radiographies du premier patient de notre série. A : face. B : oblique antérieur gauche. C : oblique antérieur droit.
Figure 2. ECG dans différents modes de stimulation. A : AAI. B : DDD avec délai AV à 240 ms et stimulation VD seule. C : DDD avec stimulation VG seule. D : DDD avec stimulation biventriculaire et délai VV nul. E : DDD avec stimulation biventriculaire et délai VG-VD de -40 ms. La largeur du QRS est indiquée en dessous de chaque mode.
Discussion
En cas d’échec répété de la resynchronisation conventionnelle avec une sonde VG placée dans une branche du sinus coronaire, on propose le plus souvent l’implantation chirurgicale d’une sonde VG épicardique par thoracotomie latérale.
Il s’agit d’un geste invasif avec sa morbidité propre. Une alternative consiste à implanter une sonde VG endocardique après avoir franchi le septum interauriculaire puis la valve mitrale. P. Jaïs et al. ont décrit les premiers cette technique en 1998(2). Plusieurs variantes ont été rapportées(3-8) de même qu’une approche chirurgicale de stimulation endocardique VG après abord transsapical(9).
Quand nous avons débuté en 2014, c’est la technique Jurdham(3) qui nous a paru la plus simple à appliquer : pas de matériel spécifique et des gestes familiers aux électrophysiologistes qui pratiquent implantations, explantations de sondes et ponctions transseptales auriculaires. Parmi les avantages de la stimulation endocardique VG, il faut citer la possibilité de choisir le site de stimulation et le fait d’entraîner une dépolarisation VG plus physiologique et plus rapide, de l’endocarde vers l’épicarde, le réseau spécialisé de Purkinje étant envahi plus précocement qu’après stimulation épicardique. La stimulation VG endocardique serait ainsi moins arythmogène et plus efficace sur le plan hémodynamique(10).
L’inconvénient majeur est la nécessité d’assurer une anticoagulation efficace dès l’implantation afin d’éviter le risque thromboembolique systémique lié à la présence de la sonde ; un INR entre 2,5 et 3,5 est recommandé, comme chez les porteurs d’une prothèse mécanique mitrale. Enfin, l’intervention reste complexe, longue, et nécessite au moins deux opérateurs. De plus, il persiste des incertitudes à long terme sur le devenir de ces sondes (lésions mitrales, risques infectieux, risques d’une éventuelle extraction, etc.).
Depuis 2016, de nouvelles approches de la stimulation VG endocardique ont été proposées. ALSYNC est une étude multicentrique qui rapporte chez 138 patients l’intérêt d’un système téléscopique de ponction du septum interauriculaire et de délivrance de la sonde VG par voie haute(11). Une technique de ponction transseptale ventriculaire par voie haute a également été décrite(12). Enfin, l’étude SELECT-LV a montré la faisabilité d’une resynchronisation avec stimulation VG délivrée sans sonde par une électrode endocardique VG, activée par un générateur sous-cutané lui-même déclenché par la stimulation VD(13).
À noter qu’une nouvelle option thérapeutique se précise avec la stimulation directe du faisceau de His dont le but est de corriger un délai de conduction intra-hissien (par exemple, un BBG) en assurant une dépolarisation simultanée des 2 branches du faisceau de His(14). Il apparaît ainsi déjà possible d’assurer une resynchronisation sans nécessité de placer une sonde ni dans une veine coronaire ni au niveau de l’endocarde VG(15). La technique reste encore peu diffusée et le succès n’avoisine que 80 % entre les mains les plus expérimentées.
Conclusion
En cas d’échec ou de non-réponse à la resynchronisation conventionnelle avec une sonde VG placée dans une veine coronaire, la stimulation VG endocardique peut représenter une alternative thérapeutique intéressante.
Les progrès techniques en cours et les études à venir permettront certainement de faciliter la procédure d’implantation et d’en préciser les indications notamment par rapport à la stimulation directe du faisceau de His. Y penser rapidement et proposer un traitement rapide et adapté est le principe de base de la MR pour améliorer sur le long terme le pronostic de ces patients.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :