Vincent PHAM, Patrice DE CASSIN, Arthur PETIT, Arnaud JEGOU, Grégoire DAMBRIN, Joseph ANCONINA, Département de cardiologie et radiologie Interventionnelle, Hôpital Privé Parly 2, Le Chesnay
Cependant, les essais contrôlés randomisés comparant le TAVI (quel que soit le type de prothèse) ont montré les meilleurs résultats en cas d’abord fémoral possible et les patients présentant des anévrismes de l’aorte abdominale ont donc souvent été exclus. En effet, le risque de rupture anévrismale, de dissection aortique ou d’embolisation périphérique doit être pris en compte. Certains cas ont été rapportés dans la littérature avec la description d’une procédure d’endoprothèse aortique préalablement au TAVI permettant de restaurer un abord vasculaire iliofémoral(1).
Nous présentons ici le cas d’un patient pris en charge pour un anévrisme de l’aorte abdominale par voie endovasculaire ayant permis lors de la même intervention et le même abord fémoral d’implanter une prothèse aortique percutanée autoexpansible.
PRÉSENTATION CLINIQUE
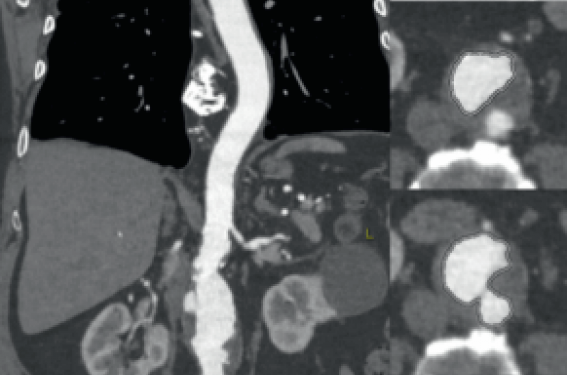
Le patient âgé de 80 ans a été adressé en hospitalisation pour un bilan préthérapeutique d’un cancer du poumon. Ce patient était suivi pour une bronchopneumopathie obstructive (BPCO) sévère. L’échographie cardiaque réalisée dans le cadre du bilan a retrouvé une fraction d’éjection ventriculaire gauche (FEVG) conservée et associée à un rétrécissement aortique serré sur une valve tricuspide et calcifiée. Le gradient moyen et la vitesse maximale du flux en Doppler étaient de 40 mmHg et 4 m/s, soit une surface d’environ 0,8 cm2. Un scanner pré-TAVI a été réalisé montrant une valve très calcifiée avec une calcification importante de la chambre de chasse (surface et périmètre d’anneau de 506,4 mm2 et 81 mm ; figure 1). L’angioscanner des axes artériels périphériques a mis en évidence un volumineux anévrisme de l’aorte abdominale irrégulier de 51 mm sur une aorte poly-ulcérée avec un risque de rupture et d’embolie important (figure 2).
Figure 1. A : Angioscanner TAVI avec mesure de la taille de l’anneau aortique. B : Coupe scanner aortique mettant en évidence une calcification de la chambre de chasse du ventricule gauche (flèche). C : Coupe 3D du scanner permettant de déterminer l’incidence de travail. D : Coupe scanner mettant en évidence des calcifications valvulaires importantes (étoile).
Figure 2. Angioscanner aortique et des axes iliofémoraux mettant en évidence un volumineux anévrisme de l’aorte abdominale sous-rénale présentant des bords irréguliers de plaque ulcérée.
Après discussion médicochirurgicale en Heart Team et avec l’équipe d’oncologie, compte tenu de la contre-indication chirurgicale sur un terrain de BPCO sévère, une indication de TAVI a été retenue.
IMPLANTATION D’UNE ENDOPROTHÈSE AORTIQUE BIFURQUÉE
À travers l’introducteur fémoral La première partie de l’intervention consistait en la mise en place d’une endoprothèse aortique bifurquée par voie percutanée. L’intervention est réalisée sous anesthésie locale et sédation. Un double abord artériel fémoral droit et gauche est réalisé après ponction échoguidée avec un introducteur 16 F dans l’artère fémorale commune droite et un introducteur 12 F dans l’artère fémorale commune gauche après mise en place d’un preclosing par ProStyle™ (Abbott) dans chaque abord. Un abord radial gauche est également mis en place.
Après la montée d’un guide Lunderquist® Extra Stiff (Cook Medical) dans l’aorte ascendante, une prothèse bifurquée Zenith Alpha™ (Cook Medical) de 28 mm est amenée et positionnée dans l’aorte abdominale. U n guide de 0,35’’ Half Stiff est récupéré au lasso à travers le jambage iliaque gauche et extériorisé par le désilet fémoral gauche (figure 3, A). Une extension iliaque gauche est d’abord mise en place (prothèse de 16 mm de diamètre). Une extension iliaque droite est ensuite positionnée par l’abord fémoral droit. Une postdilatation est réalisée à la partie proximale de la prothèse ainsi que dans les deux jambages à l’aide d’un ballon Reliant™ 12 F (Medtronic, figure 3, B à D) permettant l’application de la prothèse. Le résultat final est satisfaisant avec l’absence d’endofuites de type 1 et une endofuite minime de type 2.
Figure 3. Procédure d’implantation d’endoprothèse aortique bifurquée. A : Récupération du guide intraprothétique par un lasso. B : Postdilatation de l’extension iliaque gauche. C : Postdilatation de l’extension iliaque droite. D : Postdilatation de l’endoprothèse.
IMPLANTATION DU TAVI
À travers l’introducteur fémoral droit Sentrant™ 16 F (Medtronic) laissé en place, la procédure de remplacement valvulaire aortique est débutée. Après franchissement de la valve aortique et la mise en place d’un guide Safari2™ Small (Boston Scientific) dans le ventricule gauche, le désilet est échangé afin de placer un introducteur DrySeal® 18 F (Gore) au travers de l’endoprothèse aortique sans difficuletés et sous contrôle scopique (figure 4, A). Le système cathéter de largage Evolut PRO+ (Medtronic) de 29 mm est monté et mis en place.
Figure 4. A : Vérification de la prothèse Evolut PRO+. B : Déploiement de la prothèse Evolut PRO+. C : Retrait du cathéter au travers de l’endoprothèse aortique. D : Postdilatation de la prothèse Evolut PRO+.
La valve est déployée progressivement après stimulation rapide sur le guide à 140 battements par minute. Le résultat angiographique montre la présence d’une fuite aortique grade 2/4 motivant la réalisation d’une postdilatation. Le système de largage Evolut PRO+ est retiré à travers l’endoprothèse sur le guide Safari™ dont l’extrémité est maintenue dans le ventricule gauche. La postdilatation est ensuite réalisée sur le guide Safari™ en repassant à travers l’endoprothèse aortique avec un résultat final satisfaisant. La fermeture vasculaire est effectuée par 2 ProStyle™ mis en place en début de procédure. Devant la persistance d’un saignement, un Angio-Seal™ 8 F (Terumo) est ajouté permettant une hémostase efficace. La quantité totale de produit de contraste délivrée a été de 200 ml avec une dosimétrie de 1 500 mGy.
CONTRÔLE POST-PROCÉDURAL
Un angioscanner de l’aorte et des axes iliaques est réalisé à J2 afin de contrôler le résultat de l’endoprothèse aortique et les axes iliofémoraux (figure 5). Ce dernier montre l’absence d’endofuites de type 1 ou de complications au niveau des axes fémoraux, mais révèle une endofuite modérée de type 2.
Concernant la valve aortique, la surveillance en soins intensifs n’a pas objectivé de troubles de la conduction. L’échographie cardiaque de contrôle retrouve un gradient moyen à 17 mmHg sans fuite périprothétique. Le patient est rentré à domicile à J5.
Figure 5. Angioscanner aortique de contrôle.