Cas clinique
Publié le 30 mar 2022Lecture 5 min
Angioplastie des occlusions chroniques calcifiées - Utilisation du RotablatorTM
Philippe DURAND, Romain CADOR, Hôpital Paris Saint-Joseph
L’angioplastie des CTO se heurte dans 7 à 10 % des cas à un écueil important : l’impossibilité ou une difficulté majeure de franchissement par les ballons. C’est encore plus vrai lorsque l’occlusion est massivement calcifiée avec un risque d’échec ou de résultat sub-optimal important.
Si le microcathéter a franchi l’occlusion et permet l’échange de guide, le RotablatorTM s’impose car il est rapide et simple à mettre en œuvre.
Le franchissement de la fraise n’est cependant pas constant avec un taux d’échec de l’ordre de 5 % et nécessite un très bon appui du cathéter guide.
▸ OBSERVATION
Monsieur J.L. est un patient âgé de 59 ans tabagique, diabétique de type 2 et obèse. Il a une artériopathie oblitérante très sévère des membres inférieurs, revascularisée à plusieurs reprises par chirurgie et techniques endovasculaires.
Un an auparavant, il a présenté un syndrome coronarien aigue ST- qui a fait l’objet d’une angioplastie avec stent actif sur la circonflexe.
Il se plaint actuellement d’un angor réfractaire au traitement médical optimal, et très invalidant.
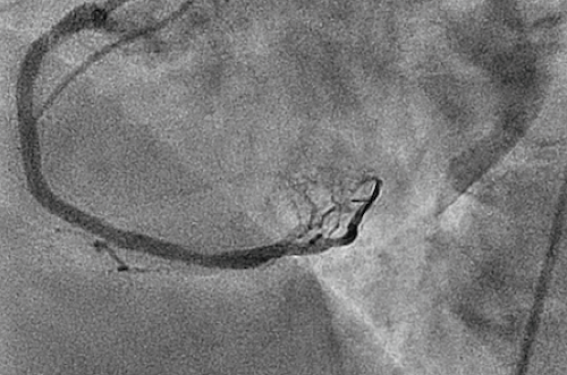
La coronarographie montre une occlusion longue massivement calcifiée de la coronaire droite moyenne (figure 1) avec un flux à peine TIMI 1 en aval.
Une première tentative de désocclusion se solde par un échec. Le patient est adressé dans notre centre pour une nouvelle angioplastie de la CTO.
Le seul abord artériel raisonnablement possible est un abord fémoral droit car les deux artères radiales et l’artère iliaque gauche sont occluses et les cubitales peu fiables.
▸ STRATÉGIE
Contraints et forcés, nous décidons de n’utiliser qu’un abord artériel fémoral droit 7 F.
Un cathéter guide AL1 7 F est mis en place dans la coronaire droite.
Un microcathéter Corsair ProTM XS (Asahi) est amené en amont de l’occlusion sur un guide BMW 0,014’’.
On utilise un guide FielderTM XT (Asahi) de première intention pour franchir l’occlusion devant l’existence d’un microchenal. Le guide franchit très progressivement et très difficilement l’occlusion. En raison de l’absence de guidance controlatérale, le guide a été utilisé de la façon la plus douce possible c’est-à-dire sans qu’il se déforme en distalité. Malheureusement, le microcathéter ne franchit pas l’occlusion malgré l’utilisation d’une extension de cathéter guide GuidezillaTM 7 F (Boston Scientific) amenée au contact de la lésion.
Le microcathéter est alors retiré et on utilise un ballon RyureiTM 5 x 1,0 mm (Terumo) pour tenter d’ouvrir le microchenal. En forçant, le ballon avance de quelques millimètres dans l’occlusion et permet une prédilatation de la chape proximale. Il ne progresse pas au-delà malgré une tentative avec un deuxième ballon neuf.
Le microcathéter est alors réutilisé et franchit très difficilement l’occlusion puis est avancé dans le segment distal de la coronaire droite.
Le guide est retiré et un guide RotaWireTM (Boston Scientific) est mis en place dans l’artère rétroventriculaire postérieure (RVP).
On fraise alors durant 30 secondes avec une fraise 1,25 mm à 200 000 tr/min avec le GuidezillaTM en place (figure 2). La fraise franchit très difficilement l’occlusion. Le GuidezillaTM est retiré et on utilise alors une deuxième fraise de 1,75 mm durant 20 secondes à 180 000 tr/min (figure 3). La lésion est ensuite prédilatée sans problème un ballon NC 20 x 3, 0 mm puis un ballon NC 20 x 3,5 mm.
L’utilisation du ShockWaveTM – initialement envisagée en cas de résistance de la lésion – en remplacement du RotablatorTM et des ballons NC n’est finalement pas utile.
Deux stents actifs Resolute OnyxTM (Medtronic) de 26 et 18 x 3,5 mm sont implantés et postdilatés par ballon NC 4,0 mm (figure 4).
Le contrôle met en évidence une sténose serrée de la RVP (figure 5) qui sera prédilatée par ballon SC 20 x 3,0 mm puis stentée avec un stent actif Resolute OnyxTM 15 x 3,0 mm.
Le résultat final est très bon avec un déploiement optimal des stents sans image de perforation ou d’effraction vasculaire (figure 6).
Nous renonçons au contrôle OCT en fin de procédure devant l’existence d’une fonction rénale légèrement altérée chez un patient diabétique.
▸ DISCUSSION
Ce cas associe plusieurs difficultés majeures.
Tout d’abord, l’artériopathie périphérique sévère du patient nous a contraint à n’utiliser qu’un seul abord artériel sans la sécurité de la guidance controlatérale. Dans le cas décrit, il y avait un très faible flux antérograde (à peine TIMI 1) en aval de l’occlusion ce qui a permis de fixer une image de référence pour se guider durant la procédure. En l’absence totale de visualisation du lit d’aval par l’injection rétrograde, la procédure serait devenue très hasardeuse et il aurait été nécessaire d’utiliser un 2e abord, vraisemblablement huméral, dont les risques chez un patient diabétique polyvasculaire sont élevés.
Les calcifications massives de la coronaire droite induisent un risque d’échec ou de résultat sub-optimal non négligeable.
Dans les registres les plus récents de CTO, environ 3 % des procédures de CTO se soldent par un échec en raison du non-franchissement par le ballon. C’est peu grâce à l’évolution des ballons de petite taille mais c’est toujours inacceptable pour le patient et l’opérateur surtout lorsque le passage du guide a été très long et fastidieux. Le RotablatorTM s’impose alors et doit être utilisé très rapidement sans arrière-pensée.
Le risque de complications n’est pas majoré par l’utilisation du RotablatorTM. Dans le registre ERCTO, le taux de MACE est de 5 % dans l’angioplastie des CTO avec ou sans RotablatorTM, le risque de perforation identique, de l’ordre de 3 % environ, et le risque d’infarctus du myocarde de 0,5 %.
La mise en place du guide RotaWireTM (Boston Scientific) et de son système d’athérectomie est conditionnée par le franchissement du microcathéter. Dans le cas décrit, le microcathéter ne franchissait pas malgré un appui rendu optimal par combinaison d’un cathéter AL1 7 F et d’une extension de cathéter guide 7 F. L’utilisation d’un ballon RyureiTM 1,0 x 5 mm a permis d’ouvrir la chape proximale a minima de quelques millimètres et d’aider au franchissement du microcathéter. Cette technique plutôt contre-intuitive doit être tentée en cas de non-franchissement du microcathéter, que l’occlusion soit calcifiée ou pas.
En l’absence de non-franchissement par le microcathéter, il est toujours possible en désespoir de cause de tenter de franchir l’occlusion par un guide RotaWireTM après avoir retiré le guide de CTO mais, par expérience, la probabilité de réussir n’atteint pas 50 %...
L’utilisation du RotablatorTM dans une extension de cathéter 7 F n’est pas usuelle mais elle est pourtant sûre et efficace grâce à un excellent support et à la possibilité d’avance l’extension dans l’artère et donc de faciliter l’avancée de la fraise jusqu’à la lésion cible.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


