Mise au point
Publié le 30 mar 2025Lecture 11 min
Cangrélor - Données scientifiques, utilisation pratique et perspectives
Nassim BRAIK, Centre cardiologique d’Évecquemont ; ACTION Cœur Study Group
La bithérapie antiplaquettaire associant l’aspirine et un antagoniste oral des récepteurs P2Y12 à l’adénosine diphosphate (ADP) est la norme pour la prévention des événements ischémiques chez les patients pris en charge pour un syndrome coronarien aigu (SCA) ou bénéficiant d’une angioplastie coronaire(1-5).
La voie orale a cependant des limites chez les patients devant être traités en urgence par angioplastie ou pour qui l’intervention ne peut être différée.
Le prétraitement systématique n’étant pas recommandé dans le NSTEMI ni dans la coronaropathie stable et qui a même été remis en cause dans le STEMI dans les dernières recommandations E S C sur les SCA(6), la réalisation d’une angioplastie urgente dans un environnement antithrombotique optimal demeure un défi quotidien pour le cardiologue interventionnel.
LIMITES DE L’ANTIAGRÉGATION PAR VOIE ORALE
Les antagonistes des récepteurs P2Y12 ont des limites qui peuvent poser des problèmes en cas d’angioplastie urgente.
Dans le cas du clopidogrel et du prasugrel, il existe un délai d’action retardé lié au besoin d’absorption intestinale et à la transformation de la prodrogue en métabolite actif, ces deux médicament s réalisant une liaison irréversible avec les récepteurs plaquettaires P2Y12(7). Cette inhibition irréversible nécessite, par ailleurs, un délai de 5 à 7 jours d’interruption du médicament avant un pontage aortocoronarien ou une chirurgie non cardiaque.
La liaison réversible du ticagrélor, molécule directement active, permet une interruption plus courte, de 3 à 5 jours.
Le clopidogrel peut également avoir un effet variable et parfois limité(8). En revanche, le prasugrel et le ticagrélor ont une plus grande efficacité, sans variabilité interindividuelle, mais au détriment d’une augmentation du risque hémorragique(9).
De plus, dans l’infarctus aigu du myocarde ou en cas de défaillance hémodynamique, la biodisponibilité des médicaments administrés par voie orale peut être sévèrement altérée, ce qui réduit l’effet antiplaquettaire au moment crucial d’une angioplastie urgente(10–12).
Disponible en France depuis maintenant de nombreuses années, le cangrélor constitue une option thérapeutique potentielle. Cette mise au point vise donc à en préciser les règles d’utilisation en pratique, les données pharmacologiques et scientifiques, sans en ignorer les limites ni les alternatives.
MÉCANISME D’ACTION DU CANGRÉLOR
(figures 1 et 2)
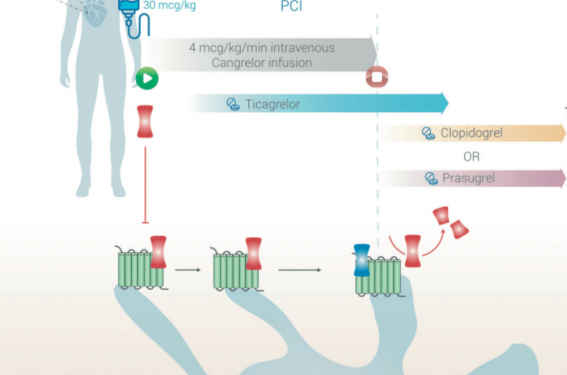
Figure 1. Pharmacologie comparative de l’inhibition des récepteurs P2Y12 par voie orale versus cangrélor(19).
Mécanisme d’action des inhibiteurs des récepteurs P2Y12 oraux et intraveineux sur les récepteurs plaquettaires (A) et transition vers les inhibiteurs oraux du récepteur plaquettaire P2Y12 chez les patients traités par cangrélor (B).
CAD : coronary artery disease ; CYP : cytochrome P450 ; PCI : percutaneous coronary intervention ; PLT : plaquettes.
Figure 2. Résultats des deux études SWAP-5 et 6, ayant évalué les interactions entre le cangrélor et les inhibiteurs oraux des récepteurs P2Y12(20,21).
Interactions médicamenteuses entre le cangrélor et le ticagrélor (SWAP-5) et entre le cangrélor et le prasugrel (SWAP-6) confirmant une interaction significative entre le cangrélor et la thiénopyridine (prasugrel).
Le cangrélor est un inhibiteur direct et réversible du récepteur P2Y12 à l’ADP de courte durée d’action.
Il s’agit d’un analogue intraveineux de l’ATP qui bloque l’activation plaquettaire en inhibant avec une grande affinité le récepteur P2Y12(13-14), le médicament est directement actif car il ne nécessite pas de conversion hépatique.
Il a une excellente biodisponibilité en atteignant la concentration maximale en 2 minutes(15). Sa durée d’action et donc le retour à une activité plaquettaire efficace se fait en 30 à 60 minutes après l’arrêt de la perfusion.
Ces propriétés en font une option thérapeutique efficace pour avoir un effet antiplaquettaire couvrant la procédure, mais offrant également une sécurité en cas de complication hémorragique et de nécessité de chirurgie urgente.
Clopidogrel et prasugrel
Les métabolites actifs des thiénopyridines (clopidogrel et prasugrel), sont instables et ont une demi-vie limitée, de 30 minutes à 1 heure respectivement. Si ces médicaments sont administrés pendant la perfusion de cangrélor ou lorsque le cangrélor est encore présent à une forte concentration dans le sang, les métabolites actifs ne pourront pas se lier au récepteur P2Y12, les empêchant d’atteindre tout effet antiplaquettaire(16).
Les thiénopyridines, en particulier le clopidogrel, doivent donc être administrées immédiatement après l’arrêt de la perfusion de cangrélor.
Ticagrélor
A contrario, le ticagrélor est un dérivé de l’ATP non thiénopyridine, ayant une demi-vie allant de 8 à 12 heures et il réalise une liaison réversible avec une forte affinité au récepteur P2Y12. Il peut donc être administré avant ou pendant la perfusion de cangrélor sans donner lieu à interaction ou à une perte d’efficacité antiplaquettaire(17,18).
ÉTUDES SCIENTIFIQUES
L’efficacité et la sécurité du cangrélor ont été comparées au clopidogrel dans trois essais cliniques randomisés impliquant des patients naïfs d’inhibiteurs P2Y12 et bénéficiant d’une une angioplastie coronaire pour des indications stables ou de syndromes coronariens aigus(22–24).
Dans ces essais cliniques du programme CHAMPION, le clopidogrel a été administré 30 minutes avant procédure dans CHAMPION PCI(22), ou en fin de procédure (CHAMPION PL ATFORM(23) et CHAMPION PHOENIX(24).
Les résultats des deux premiers essais étaient négatifs avec un signal sur la thrombose de stent et l’infarctus périprocédural.
La méta-analyse de ces trois essais randomisés, publiée dans The Lancet, a montré un bénéfice anti-ischémique du cangrélor, principalement sur la thrombose de stent ou la suspicion de thrombose de stent qui correspond à la visualisation d’un possible thrombus angiographique, ainsi que sur la réduction significative de l’infarctus périprocédural, au prix d’une augmentation des complications hémorragiques mineures (figure 3)(25).
Figure 3. Graphique des critères d’évaluation principaux, secondaires clés, secondaires à 48 h et globaux dans chacun des trois essais.
IDR : revascularisation induite par l’ischémie. IDM : infarctus du myocarde. ST : thrombose de stent.
Il est également important de noter que le bénéfice du cangrélor en ce qui concerne les événement ischémiques a été atténué dans CHAMPION PCI avec l’administration précoce du clopidogrel.
Le cangrélor n’a été évalué qu’en comparaison au clopidogrel et n’a pas été comparé au ticagrélor ou au prasugrel ce qui constitue évidemment une limite à l’heure où ces deux médicaments sont majoritairement prescrits dans les syndromes coronariens aigus.
Période périopératoire
L’essai clinique prospectif, randomisé, en double aveugle, BRIDGE(26), a été mené chez 210 patients traités par une thiénopyridine en attente d’un pontage aortocoronarien à une posologie réduite de 0,75 μg/kg par minute.
Dans cet essai, la perfusion a été maintenue pendant au moins 48 heures et jusqu’à 7 jours pendant le sevrage de la thiénopyridine orale ; la perfusion a été interrompue 1 à 6 heures avant le pontage aortocoronarien.
L’utilisation du cangrélor par rapport au placebo a entraîné un taux plus élevé de maintien de l’inhibition plaquettaire sans différence significative en termes d’hémorragie majeure.
Cette indication n’est pas retenue par la FDA (Food and Drug Administration) ni l’EMA (European Medicines Agency) et elle n’est pas non plus retenue par la HAS, mais elle est décrite comme une option possible dans différents consensus(27-29). Les options thérapeutiques pour la gestion périopératoire des antiplaquettaires ont été bien résumées dans un article publié en 2021 dans le JACC (figure 4)(29).
Figure 4. Approche pratique de relais par antiplaquettaires en cas de chirurgie(29).
L’association cangrélor et anti-GPIIb/IIIa
Cette association ne peut se concevoir qu’en cas de complication thrombotique, les antiGPIIb/IIIa ne sont recommandés qu’en bail-out(6). Dans une analyse post-hoc des trois essais CHAMPION, l’administration d’anti-GPIIb/IIIa était associée à plus de saignements majeurs indépendamment du bras de randomisation(30).
PLACE DU CANGRÉLOR DANS LES RECOMMANDATIONS ET AMM EN FRANCE
Depuis mars 2016, le cangrélor est autorisé en France avec une AMM assez restrictive.
L’indication HAS(31)
Le médicament doit être strictement limité aux patients qui doivent bénéficier d’une angioplastie en urgence :
• Chez qui l’administration orale d’un inhibiteur des récepteurs P2Y12 n’est pas faisable, à savoir les patients qui ne peuvent avaler (patients intubés ou sous sédation, dans un contexte tel que l’arrêt cardiaque ou le choc cardiogénique) et ceux dont l’absorption digestive est fortement altérée ;
• ET chez les patients qui n’ont pas reçu d’inhibiteur oral des récepteurs P2Y12 avant cette intervention.
À noter que ces patients, survivants d’arrêt cardiaque ou en choc cardiogéniques ont été exclus des essais cliniques princeps publiés.
Les recommandations ESC 2023(6) et américaines ACC/ AHA de 2025(32)
• Les syndromes coronariens aigus
Elles préconisent le cangrélor en indication 2B chez les patients pris en charge pour un syndrome coronarien aigu justifiant une angioplastie et n’ayant pas été prétraités par un anti-P2Y12. L e s recommandations de s sociétés savantes ne limitent pas l’indication du cangrélor à l’impossibilité de la voie orale, en absence d’études randomisées validant cette attitude.
• Les patients stables
L’essai clinique ALPHEUS(33), n’a pas montré de bénéfice du ticagrélor versus clopidogrel pour prévenir l’infarctus périprocédural dans l’angioplastie. Les sous-études pour les procédures complexes(34) et les patients traités pour syndromes coronariens chroniques(35) ne montrent également pas de bénéfice du ticagrélor.
L’angioplastie du patient stable avec anatomie complexe, ne devrait probablement pas se faire en ad hoc, ce qui permettrait une meilleure information du patient et de sa famille ainsi qu’une préparation technique et antiplaquettaire par clopidogrel en amont de la procédure. Une discussion au cas par cas avec une décision personnalisée est à privilégier.
UTILISATION EN PRATIQUE
Médicament introduit en salle de cathétérisme
Indication
Angioplastie coronaire chez les patients n’ayant pas reçu d’inhibiteur des P2Y12, en association avec l’aspirine et pour qui la voie orale n’est pas réalisable ou souhaitable.
Contre-indications
Antécédent d’AVC ou d’AIT. Saignement actif. Coagulopathie.
Présentation et dilution
– Flacon de 50 mg de poudre à diluer.
– Reconstituer chaque flacon de 50 mg avec 5 ml d’eau stérile (tournoyer doucement sans agiter vigoureusement).
– Diluer le flacon reconstitué avec 250 ml de sérum physiologique 0,9 % ou G5 %.
– Concentration obtenue de 200 µg/ml.
Mode d’emploi
Le bolus et la perfusion doivent être instaurés avant l’intervention, en salle de cathétérisme.
• Bolus de 30 µg/kg à administrer en moins de 1 minute.
• Suivi immédiatement d’une perfusion de 4 µg/kg/min. Remplir une seringue de 50 ml avec la solution diluée puis adapter la vitesse du PSE au poids du patient.
Durée de la perfusion : au moins 2 heures, ou toute la durée de la procédure selon la durée la plus longue, jusqu’à 4 heures.
Transition vers le traitement per os
• Une dose de charge d’inhibiteur de P2Y12 doit être administrée :
– Ticagrélor (Brilique®, AstraZeneca) 180 mg peut être donné en début de procédure ;
– Prasugrel (Efient®, Substipharm) 60 mg : administrer dès la fin de la procédure, au plus tôt 30 minutes avant la fin de la perfusion ;
– Clopidogrel (Plavix®, Sanofi) 600 mg : en cas de contre-indication au ticagrélor ou au prasugrel à la fin de la perfusion.
• Le reste du traitement antithrombotique (aspirine, HNF ou HBP M) est à instaurer comme d’habitude en fonction des recommandations ; pas de modification significative.
Surveillance et adaptation thérapeutique
• Pas de surveillance biologique particulière.
• Pas d’adaptation de la posologie en fonction de l’âge, de la fonction rénale ou hépatique.
LIMITES
Le cangrélor n’a été comparé qu’au clopidogrel, le bénéfice démontré porte sur les complications périprocédurales avec des définitions non standardisées de la thrombose de stent.
Dans les essais CHAMPION PHOENIX et PLATFORM, le clopidogrel a été donné en fin de procédure donc avec un délai d’action allongé pour le clopidogrel.
Il n’y a pas eu d’essai clinique dédié à l’infarctus du myocarde, en particulier le STEMI.
Le coût du médicament : un flacon de cangrélor coute 350 € HT versus 52 € pour un flacon de tirofiban à titre d’exemple.
Un effet rapide des anti-P2Y12 oraux peut également être obtenu (en 30 min à 1 h) en cas d’administration de comprimés écrasés, machés ou orodispersibles(36).
PERSPECTIVES ET NOUVEAUTÉS DE L’ANTIAGRÉGATION PLAQUETTAIRE
L’essai clinique DAPT-SHOCKAMI(37) est en cours, évaluant le cangrélor en comparaison au ticagrélor « crushé », dans le choc cardiogénique compliquant l’infarctus du myocarde. C’est une étude très prometteuse parce qu’elle va étudier la place du cangrélor dans l’indication qui semble idéale mais qui n’a pour l’instant pas de données randomisées pour l’étayer.
D’autres essais cliniques sont en cours pour évaluer de nouvelles pistes thérapeutiques : le selatogrel, un inhibiteur réversible des récepteurs P2Y12 par voie sous-cutanée avec un stylo auto-injecteur Cette molécule est étudiée dans l’essai clinique SOS-AMI où elle sera évalué en automédication en cas de symptômes évocateurs d’infarctus(38-39).
L’essai clinique CELEBRATE(40) évaluant le zalunfiban, un nouvel inhibiteur de la glycoprotéine IIb/IIIa, administré par voie sous-cutanée et conçu pour une administration préhospitalière. Il permet d’obtenir une inhibition plaquettaire rapide et efficace qui dépasse celle des inhibiteurs de P2Y12, sans les risques de thrombocytopénie. Sa durée d’action est de 1 à 2 heures, ce qui en fait également une solution potentiellement très prometteuse pour l’infarctus en phase aiguë ou en cas de complication hémorragique ou de nécessité de chirurgie urgente. Les pistes thérapeutiques en cours d’évaluation pour optimiser l’environnement antiplaquettaire de l’infarctus du myocarde et de l’angioplastie coronaire sont schématisées dans la figure 5(41).
Figure 5. Exemples de nouveaux antiplaquettaires et de leurs mécanismes d’action.
ADP : adénosine diphosphate ; AMP : adénosine monophosphate ; CD : cluster de différenciation ; GP : glycoprotéine ; P2Y12 : récepteur plaquettaire de l’ADP ; PAR : récepteur activé par la protéase ; PDI : protéine disulfure isomérase ; PI3Kb: phosphoinositide 3-kinase ; TP a : récepteur a du thromboxane ; TxA2 : thromboxane A2 ; vWF : facteur de von Willebrand.
CONCLUSION
• Le cangrélor est une option thérapeutique efficace pour assurer une inhibition plaquettaire perprocédure en association avec l’aspirine pour réduire les complications ischémiques, au prix d’une augmentation des saignements mineurs.
• Il est autorisé en France en cas d’administration orale impossible d’un inhibiteur oral des récepteurs P2Y12.
• Sa demi-vie très courte et sa durée d’action en font un médicament de la procédure, dont l’arrêt en cas de complication ou de nécessité de chirurgie permet une disparition de l’effet en 30 à 60 min maximum.
• L’utilisation protocolisée est relativement facile : pas d’adaptions en fonction de l’âge, de la fonction rénale, pas de thrombopénie mais des contre-indications à connaître.
• Son coût relativement important comparativement aux anti-GPIIb/IIIa ou aux inhibiteurs oraux des P2Y12 est un point limitant, mais ses indications ne sont pas les mêmes : le coût est donc à mettre en perspective avec celui d’une procédure reportée ou d’un séjour prolongé pour permettre un prétraitement.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


