Cas clinique
Publié le 15 oct 2023Lecture 14 min
Faux anévrisme de l’artère radiale postangioplastie coronaire - Traitement endovasculaire par stent coronaire couvert via un abord radial distal
Jean-Marc PERNES, Pôle Cardiovasculaire interventionnel 77, Clinique les Fontaines, Melun
Mme L… est une femme de 87 ans se plaignant de douleurs thoraciques en étau survenant au repos depuis 2 semaines. Elle est traitée par apixaban pour une fibrillation auriculaire chronique. L’ECG objective des ondes T négatives dans les dérivations antérieures, il n’y a pas d’anomalie dynamique du cycle de troponine et l’échoscopie cardiaque est sans particularité. Devant une forte probabilité prétest de sténose coronaire, la patiente est adressée directement pour coronarographie.
L’exploration effectuée par cathétérisme de l’artère radiale droite proximale (désilet et sondes 4 F) met une évidence une sténose très serrée, isolée, de l’interventriculaire antérieure (IVA) ostiale. Pour des raisons personnelles, – socio-environnementales, son chien est tout seul à la maison –, la patiente refuse l’angioplastie ad hoc qui lui est proposée, souhaitant absolument retourner à son domicile, mais consent à se présenter 72 heures plus tard pour cette procédure. Un système d’hémostase type TR BAND® (Terumo) est positionné et il n’est pas signalé d’hématome significatif autour du point de ponction au moment de son départ.
L’angioplastie est réalisée comme convenu 3 jours plus tard, toujours par un abord radial droit proximal, après l’introduction d’un désilet 6 F, malgré la présence d’un hématome superficiel minime de l’avant-bras (< 6 cm). Le résultat est excellent, un nouveau système TR BAND® est positionné et la patiente sort 24 heures plus tard, avec un hématome important de l’avant-bras (> 8 cm), sans signe de compression péjoratif, sous une trithérapie antithrombotique prescrite pour 10 jours (apixaban-clopidogrel-acide acétylsalicylique).
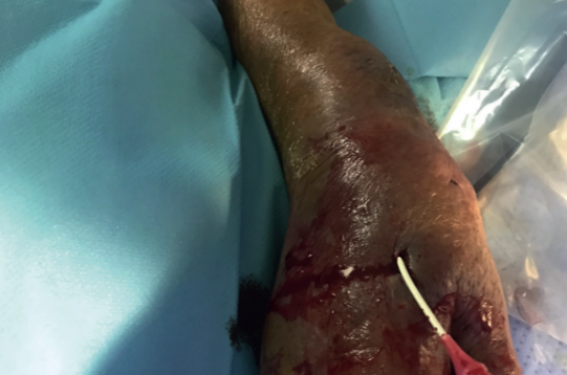
Elle se présente aux urgences 8 jours plus tard du fait d’un hématome étendu au niveau brachial et d’une tuméfaction pulsatile au niveau de l’abord radial (figure 1). Une échographie Doppler révèle la présence d’un faux anévrisme de l’artère radiale (FAAR) de 4 x 4 cm avec un collet court et de 3 mm de largeur (figure 2). Une tentative de compression externe sous guidage échographique est effectuée mais s’avère infructueuse. L’injection de thrombine in situ, échoguidée n’est pas retenue du fait du collet court et large faisant craindre une migration du matériel. Plutôt que la chirurgie, il est décidé de réaliser un traitement endovasculaire original, à savoir la mise en place d’un stent coronaire couvert par abord de l’artère radiale distale (ou dorsale), dont le pouls est bien perçu à la palpation en regard du 1er espace intermétacarpien, après positionnement optimum de la main, pouce fléchi maintenu sous les 4 autres doigts de la main.
Figure 1. Masse pulsatile ecchymotique en regard de l’artère radiale droite proximale et hématome de l’avant-bras et du bras droit (flèches bleues).
Figure 2. Aspect à l’écho-Doppler : faux anévrisme circulant de l’artère radiale droite avec collet large (> 3 mm).
Après introduction d’un désilet 5 F (figure 3), l’injection précautionneuse de contraste iodé confirme la localisation du pertuis et l’opacification du faux anévrisme (figure 4). Un guide 0,014’’ (BMW, Abbott) est poussé jusque dans l’aorte ascendante et un stent couvert coronaire (BeGraf, Bentley InnoMed) de 2,5 mm de diamètre et 12 mm de long, introduit directement dans le désilet, est largué d’emblée en regard du collet, après une inflation d’une minute à 10 bars. Le résultat immédiat est excellent (figure 5) et perdure sur le contrôle échographique à 3 mois avec persistance de la perméabilité de l’artère radiale proximale et distale.
Figure 3. Désilet 5 F après ponction de l’artère radiale distale droite.
Figure 4. Opacification angiographique du faux anévrisme et largage du stent couvert coronaire BeGraf 2,5 x 12 mm via le désilet 5 F. Le stent coronaire BeGraf (Bentley InnoMed) est un tube en PTFE, serti sur un stent cobalt chrome et fixé aux 2 extrémités du stent par un double maillage réalisant un clip tel un trombone. Il est compatible 5 F et apparaît donc de ce fait comme ayant le meilleur profil sur le marché. Il est disponible en longueur de 8 à 24 mm (6 longueurs disponibles) avec des diamètres de 2,5 à 5,0 mm.
Figure 5. Aspect angiographique et clinique postimplantation du stent couvert.
DISCUSSION
L'artère radiale est couramment utilisée pour le prélèvement sanguin artériel et la mesure des gaz du sang, la surveillance invasive de la pression artérielle (temporaire lors d’une anesthésie générale pour chirurgie ou prolongée en réanimation) et comme accès vasculaire pour le cathétérisme cardiaque.
Traditionnellement, le point de ponction standard de l’artère radiale est situé au tiers distal de la face antérieure de l’avant-bras, où sa situation superficielle proche du radius facilite sa ponction et sa compression. La voie droite est habituellement préférée, car la voie gauche est moins confortable pour l’opérateur.
L'introduction de l'utilisation de l'artère radiale proximale, à la face palmaire du poignet, comme abord vasculaire à la coronarographie par Lucien Campeau en 1989(1) et la première angioplastie coronaire via l'artère radiale par Ferdinand Kiemeneij en 1992(2), ont marqué le début d'une nouvelle ère en cardiologie interventionnelle. Cependant, il a fallu plus de 2 décennies pour établir la base fiable de l'efficacité et de la sécurité de l'abord transradial (ATR) afin qu'il puisse être reconnu comme un accès fiable pour toute angioplastie coronaire, indépendamment du tableau clinique.
En effet, de nombreuses études observationnelles et de grands essais randomisés ont démontré que l'ATR est associé non seulement à un risque réduit de saignement et de complications vasculaires au site d'accès, mais également à une réduction de la mortalité dans les sous-groupes de patients à haut risque, tels que ceux présentant un syndrome coronarien aigu (SCA)(3-8). Cela a conduit la Société européenne de cardiologie à recommander l'ATR plutôt que l'accès transfémoral comme indication de classe IA pour les patients atteints de SCA bénéficiant d’une prise en charge invasive, si elle est effectuée par des opérateurs expérimentés(9). De même, une récente déclaration de l'American Heart Association a proposé que l’ATR devienne le site d'accès par défaut chez les patients atteints de SCA aux États-Unis(10).
Bien que l’ATR utilisé pour un monitoring hémodynamique en réanimation ou pour un cathétérisme cardiaque ou périphérique soit associé à des taux de complications plus faibles que l'approche transfémorale, il n'est pas totalement dénué de risque et des complications intraprocédurales et postprocédurales sont possibles(11,12).
Les complications vasculaires et hémorragiques
E. Tatli et al.(12) ont rapporté 45 complications vasculaires et hémorragiques (hématome > 6 cm, perforation, fistule artérioveineuse, faux anévrisme) sur une série de plus de 10 000 sujets (75 % de coronarographies, 25 % d’angioplasties) entre 2010 et 2014, soit moins de 0,5 % du total. Il s’agissait très majoritairement d’hématomes (32/45), alors que 8 perforations, 4 fistules et 1 pseudo-anévrisme ont été rapportés. Seuls 3 patients sur les 45 ont justifié d’une prise en charge chirurgicale (dont le seul cas de pseudo-anévrisme), le reste ayant été géré avec succès par des manœuvres conservatrices (compression mécanique externe).
Le spasme de l'artère radiale
En raison de son petit diamètre l’artère radiale est sujette aux spasmes et présente des variations anatomiques beaucoup plus souvent que les autres artères, notamment des naissances hautes ce qui peut entraîner des complications peropératoires, une conversion d'accès et un allongement de la durée de la procédure. L'incidence rapportée des spasmes de l'artère radiale est variable, allant de 4 à 20 %, en partie en raison de l'absence d'une définition uniforme de cette complication(11). On pense que la physiopathologie est liée à l'abondance des récepteurs adrénergiques dans la paroi de l'artère radiale, qui, lorsqu'ils sont stimulés par la manipulation du cathéter, l'étirement de la paroi et les traumatismes locaux, contribuent à une vasoréactivité accrue entraînant une vasoconstriction des cellules musculaires lisses.
La perforation de l'artère radiale
C’est une complication rare, inférieure à 1 %, et lorsqu'elle se produit, elle conduit souvent à un hématome de l'avant-bras. Elle est généralement provoquée par le guide à l’origine d’une rupture dans une petite branche ou par « l'effet rasoir » causé par la pointe d'un cathéter traumatisant la paroi artérielle lors de sa progression.
L'occlusion précoce et tardive de l’artère radiale
La complication la plus courante de l'ATR reste l'occlusion précoce et tardive de l’artère radiale (OAR)(13). En 2016, une revue systématique et une méta-analyse ont rapporté les taux d'OAR en utilisant différentes méthodes et à différents intervalles de temps(14). De 1996 à 2015, un total de 66 études totalisant 31 345 participants ont été incluses dans l'analyse. Si l'on considère uniquement les essais cliniques randomisés de cette méta-analyse (5 258 patients de 12 essais), le taux précoce d'OAR était toujours de 7,7 %. Une seconde mise à jour contemporaine des études randomisées pertinentes évaluant les OAR précoces après ATR (données PubMed jusqu'en février 2019)(15) a inclus plusieurs essais randomisés ultérieurs, avec une inclusion totale de 9 847 patients, évaluant différentes stratégies préventives pour l’OAR. Elle a mis en évidence une diminution globale du taux d’OAR à 3,7 %, soulignant les améliorations dans la prévention de l’OAR au fil du temps.
La présence d'une artère radiale obstruée après cathétérisme entraîne rarissimement des conséquences ischémiques graves, ce qui a conduit au rejet complet du test Allen avant la ponction, bien que la littérature décrive des cas sporadiques d'ischémie aiguë de la main.
Le faux anévrisme de l’artère radiale
Le faux anévrisme de l’artère radiale (FAAR) iatrogène est en revanche une complication extrêmement rare(16) mais potentiellement dangereuse, liée au risque de saignement externe en raison de la rupture de sa paroi externe extrêmement fragile. Contrairement aux perforations, ils peuvent apparaître plus tardivement avec un délai très variable. Plusieurs facteurs prédisposent à la survenue d’un FAAR, notamment les tentatives de ponction multiples, l'anticoagulation systémique continue, l'hémostase ou la compression post-intervention inadéquate, l'infection du site vasculaire et l'utilisation de désilets de grande taille. L’incidence réelle du FAAR est inconnue : probablement en raison de son incidence plus faible comparée à la fémorale et à sa sous-déclaration.
Dans une récente publication avec une évaluation prospective de 2004 à 2013, seulement cinq cas de FAAR ont été détectés après 16 808 ATR (3 cathétérismes sur 10 000 soit 0,03 %)(17), ce qui est nettement inférieur à la fréquence des pseudo-anévrismes fémoraux (0,6 %) compliquant un accès fémoral.
Dans leur étude rétrospective sur la période 2003-2015 A. M. Babunashvili et al.(18) n’ont détecté que 4 cas de FAAR sur 17 204 ATR diagnostiqués et procédures de cathétérisme interventionnelles (0,02 %).
J. N. Din et al.(19) ont effectué une recherche dans la base de données d'imagerie médicale de la Vancouver Island Health Authority du 1er janvier 2008 à avril 2012 à la recherche de tous les pseudo-anévrismes de l'artère radiale et/ou fémorale survenant après un cathétérisme cardiaque. Au total, 14 968 interventions coronariennes ont été effectuées au cours de la période de recherche de 4 ans, dont 13 216 (88 %) étaient transradiales. L'incidence du pseudo-anévrisme de l'artère radiale après cathétérisme cardiaque était de 0,08 % et ne différait pas entre l'angiographie diagnostique transradiale et les actes interventionnels (0,07 % vs 0,08 % ; p = 0,90). En revanche, l'incidence du pseudo-anévrisme de l'artère fémorale était plus élevée, à 1,4 % (p < 0,0001). Les patients atteints de pseudo-anévrismes radiaux étaient généralement âgés, avec un âge médian de 77 ans, et il n'y avait pas de différence entre les sexes. Les cas se présentent habituellement sous la forme d'une masse érythémateuse pulsatile au site de ponction, parfois associée à des saignements pulsatiles par ulcération/érosion du faux anévrisme. Tous sont confirmés par échographie Doppler vasculaire. Les facteurs les plus fréquemment associés à la survenue d’un pseudo-anévrisme sont l'utilisation de l’anticoagulation par warfarine (Coumadine) pendant la procédure et la survenue d'un hématome dans l'avant-bras pendant/après la compression reflétant probablement une hémostase inadéquate après la procédure et un saignement retardé compliquant l'anticoagulation systémique.
Beaucoup de petits pseudo-anévrismes postcathétérisme ont tendance à thromboser spontanément au fil du temps. R. Totsi et al.(20) ont identifié 11 cas de FAAR résultant de la mise en place d'un cathéter artériel ou d'un accès à l'artère radiale pour des procédures cardiaques pendant la période de 2010 à 2015 : 5 étaient causés par des cathéters artériels et 6 par des procédures cardiaques. Le diagnostic a été confirmé par échographie duplex dans tous les cas. La taille du pseudo-anévrisme variait de moins de 1 à 5 cm de diamètre. Une thrombose spontanée (sur une moyenne de 27 jours) est survenue chez 4 patients (chaque FAAR était < 3 cm).
Toutefois les gros pseudo-anévrismes qui ne thrombosent pas spontanément doivent être traités, parce que potentiellement sujets à rompre.
LE TRAITEMENT DES FAAR
Il a évolué au fil des ans. Initialement, le traitement chirurgical était la forme dominante de gestion, avec d’excellents résultats immédiats et à distance. Ainsi dans la série de Tosti et al.(20), la chirurgie a été réalisée chez les 7 patients chez qui persistaient le faux anévrisme. Un seul cas a été réalisé en urgence pour syndrome aigu du canal carpien ; 80 % des 10 patients de la série de Din et al.(19) ont bénéficié d’une réparation chirurgicale avec un bon résultat clinique.
Dans la série rétrospective la plus récente de la littérature, D. Kim et al.(21) ont rapporté sur la période 2008-2018, 6 cas de FAAR (3 post-cannulation pour monitoring, 3 post-cathétérisme), tous opérés avec succès sans séquelle. Les dix patients de la série de K. Garg et al.(22) porteurs d’un faux anévrisme iatrogène de la radiale ont tous été chirurgicalement traités et ce avec une issue immédiate et à distance favorable.
Les méthodes mini-invasives
Néanmoins au cours de la dernière décennie plusieurs méthodes mini-invasives ont été introduites et qui se sont largement substituées au traitement chirurgical. Les techniques les plus courantes sont la compression guidée par ultrasons et l’injection percutanée de thrombine dans le sac sous guidage échographique.
• La compression occlusive guidée par ultrasons, juste en amont du pertuis, pendant quelques heures, est associée à un taux de réussite élevé(23-25), mais cette technique présente également des limites importantes, notamment une diminution du taux de succès pour les patients sous anticoagulation permanente nécessitant un temps de compression prolongé, entraînant souvent de l'inconfort et de la douleur(26-29). Parfois, il y a des récidives après le traitement par compression nécessitant par la suite d'autres tentatives de compression ou chirurgie(30).
• L'injection de thrombine guidée par ultrasons (1 ml, soit 500 UI) est une technique plus efficace dans presque tous les cas, même chez les patients sous traitement anticoagulant au long cours(31-33). Toutefois, l'injection de thrombine dans le sac du pseudo-anévrisme n'est pas totalement dénuée de risque(23), particulièrement lorsque le collet est large et court (> 3 mm), ce qui apparaît comme une contre-indication de la méthode.
A. M. Babunashvili, le pionnier de la ponction radiale distale, fort des constatations des limites potentielles des traitements non chirurgicaux sus-décrits a proposé une alternative pour le traitement des FAAR iatrogènes, qui va inspirer notre démarche thérapeutique. Dans le cas publié(34), il introduit par voie radiale distale un désilet long (23 cm) de 6 F, placé au-delà du collet et laissé en place 8 h, temps supposé entraîner l’étanchéité du faux anévrisme, associé à une compression douce par bandage externe en regard du collet. Il évoque même dans la discussion de son article, l’intérêt de l’insertion d’un stent couvert, mais qu’il considère comme trop aléatoire au vu des caractéristiques techniques du matériel alors à sa disposition. Quoi qu’il en soit, le contrôle angiographique effectué au retrait du désilet montrait la disparition de la fuite et la thrombose complète du faux anévrisme qui se confirmera au Doppler de contrôle réalisé 2 mois plus tard.
La gamme de stents couverts actuellement disponibles, aux profils considérablement améliorés (figure 6), particulièrement le modèle BeGraft, nous a permis de lever cette inquiétude. Ceci s’est avéré exact dans la mesure où il n’y a eu aucune difficulté technique à insérer le stent couvert via un désilet 5 F introduit par voie radiale dorsale. Une variante de notre technique est rapportée par I. Tsiafoutis et al.(35) ayant traité avec succès un FAAR par stent couvert, délivré par un accès de l’artère ulnaire ipsilatérale (désilet 6 F) et cathétérisme rétrograde de l’artère radiale au niveau de la division humérale.
Figure 6. Modèles de stents coronaires couverts actuellement sur le marché.
LA RADIALE DISTALE : UNE EXCENTRICITÉ DE « RADIALISTE » ?
Récemment, l'artère radiale distale, en regard de la tabatière anatomique sur la face dorsale de la main (« ARD distale » ou « dorsale » ou « accès à la tabatière ») est apparue comme un accès alternatif à l'artère radiale conventionnelle de l'avant-bras pour l'angiographie coronarienne et les interventions.
Elle a été « inventée » pour la cannulation de l’artère radiale en anesthésie réanimation(36) par Stephen Pyles en 1982 et proposée en cardiologie interventionnelle par A. M. Babunashvili dès la fin des années 1990, qui l’a initialement utilisé pour désobstruer de manière rétrograde des occlusions thrombotiques de l’artère radiale à l’avant-bras, survenues dans les 6 jours après une coronarographie par voie radiale traditionnelle(37). Il y a environ 10 ans, indépendamment les uns des autres, 3 cardiologues interventionnels russes (Babunashvili, Kaledin, Korotkikh) ont commencé à développer activement l’abord de l’artère radiale dans la tabatière anatomique pour les procédures endovasculaires, et en révéler certains avantages, notamment la réduction du risque de complications locales(38).
On distingue deux voies d’abord, dans la tabatière anatomique (au bord externe du poignet) et au dos de la main (voie radiale très distale) même s’il s’agit plus ou moins du même espace anatomique, qui est séparé en deux par le tendon de l’extenseur long du pouce (figure 7).
Figure 7. Espace anatomique permettant l’abord de l’artère radiale dorsale. Les flèches bleues indiquent 2 sites où un pouls radial peut être perçu, dans la tabatière anatomique et dans le premier espace inter-métacarpien. Ils représentent des points de ponction alternatifs pour la ponction distale.
Au-delà des avantages potentiels liés à l'amélioration du confort de l'opérateur, à une hémostase plus facile et plus courte due à la position plus superficielle de l'artère radiale distale, l’abord de l’artère radiale distale présente une justification physiologique et anatomique solide pour réduire le taux d’OAR de l'avant-bras(38).
En effet, une caractéristique importante de cette technique est une ponction distale à l'arc palmaire superficiel. En tant que telle, l’ATR distale a le potentiel de maintenir le flux antérograde dans l'artère radiale de l'avant-bras pendant la compression hémostatique ou en cas d'occlusion distale de l'artère radiale, réduisant ainsi le risque de formation de thrombus rétrograde. Les données actuellement disponibles sur l'abord distal se limitent à des séries de cas observationnels examinant principalement la faisabilité et les taux de réussite de cette approche(39-41). Fait intéressant, la plupart des études ont rapporté un taux d’occlusion de l’artère radiale < 1 %.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


