Focus
Publié le 10 juil 2023Lecture 16 min
L’angioplastie artérielle au CO2 : pourquoi et comment faire du neuf avec du vieux ?
Jean-Marc PERNÈS, Costantino Del GIUDICE, unités de cardiologie et de radiologie interventionnelles, Institut Mutualiste Montsouris, Paris
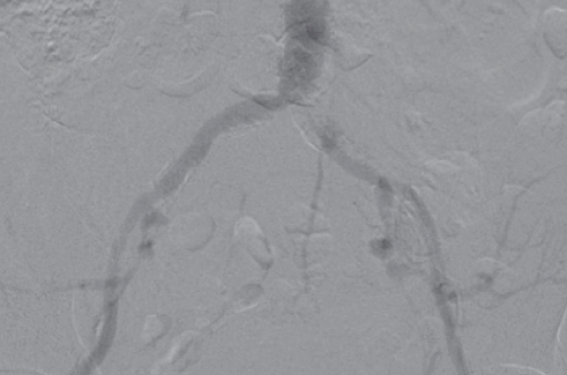
L’extension des indications d’angioplastie artérielle périphérique est une réalité. La technique s’applique à présent à des patients de plus en plus âgés et présentant de nombreuses comorbidités.
RATIONNEL D’EMPLOI DU CO2 COMME AGENT DE CONTRASTE INTRAVASCULAIRE
Les produits de contraste iodés (PCI) constituent l’agent d’opacification artérielle de référence, mais leur injection peut se compliquer de néphropathie avec parfois des lésions rénales irréversibles(1). Même si les PCI ne doivent plus être considérés comme les seuls responsables de la toxicité rénale, qui ne survient le plus souvent qu’en présence de facteurs associés, – on a remplacé l’expression insuffisance rénale aiguë (IRA) induite par le contraste par celle d’IRA postcontraste –, cette néphrotoxicité n’est pas rare après une intervention endovasculaire cardiovasculaire pouvant toucher jusqu’à 15 % des patients(2) et elle est grevée d’une augmentation de la mortalité (22 % vs 1,4 % de mortalité intrahospitalière(3)). La stratégie la plus efficace pour réduire le risque toxicité rénale est, d’une part la prévention par l’hydratation parentérale pré et perprocédure et, d’autre part, la limitation de la quantité de PCI injecté (< à 4 ml/kg)(4)). Les autres complications de l’utilisation de PCI sont les réactions d’hypersensibilité graves, dites « spécifiques », de nature immunologique vraie, certes rarissimes, mais qui demeurent une authentique problématique dans la réalité. Enfin, au-delà des contre-indications potentielles de l’utilisation des PCI se pose la question de l’impact économique sur les coûts hospitaliers de l’emploi des PCI et de l’intérêt de rechercher des alternatives avec un meilleur rapport coût-efficacité. L’utilisation de dioxyde de carbone (CO2), produit endogène dépourvu de phénomènes de néphrotoxicité et allergiques(5), est une alternative valable en angioplastie artérielle périphérique, offrant une bonne qualité d’imagerie avec un risque de complications liés à son utilisation très faible et à un coût incomparable. L’angiographie au CO2 peut être utilisée comme modalité d’imagerie seule ou comme agent adjuvant pour minimiser la quantité de PCI requise pendant l’intervention réelle(5,6).
HISTORIQUE DE L’UTILISATION DE CO2 EN IMAGERIE
L’utilisation de CO2 en imagerie remonte au début du XXe siècle où, initialement, ce gaz a été utilisé dans l’imagerie du rétropéritoine. Par la suite, dans les années 1950, le CO2 a été employé dans la détection des épanchements péricardiques et l’opacification veineuse. Ce n’est que dans les années 1970 qu’il a commencé à être injecté comme agent d’opacification artérielle à la suite des travaux de Hawkins(6). Irvin F. Hawkins, largement reconnu comme un pionnier de l’angiographie au CO2 moderne, a décrit comment sa découverte lui a permis de réaliser le potentiel de cette technique lorsqu’il a injecté par inadvertance de l’air dans le tronc cœliaque, heureusement sans conséquences néfastes (n’nième exemple de sérendipité médicale !). Cette expérience, associée à sa connaissance de la sécurité du CO2 en tant qu’agent de contraste intraveineux, l’a amené à envisager le CO2 comme agent de contraste potentiel dans le système artériel.
Ses premières expériences ont marqué le début de cette nouvelle approche pour l’imagerie intravasculaire mais malgré des propriétés prometteuses, sa diffusion a été limitée par la survenue de complications potentiellement graves, une qualité d’imagerie initialement insuffisante ainsi que la difficulté pour les opérateurs habitués à utiliser des agents d’opacification liquides à manier un agent gazeux.
Une bonne connaissance des propriétés du CO2 est donc nécessaire afin d’obtenir la meilleure qualité possible d’imagerie et minimiser le risque de complications(7) liées à la technique.
PROPRIÉTÉS DU CO2 ET CONSÉQUENCES EN IMAGERIE
Absence de toxicité ou de réactions allergiques
Le CO2 est un agent neutre, naturel qui est non néphrotoxique, non hépatotoxique et non allergène.
Clairance intravasculaire complète rapide
Le CO2 est très soluble dans le sang, avec un bolus intravasculaire de 30 ml de CO2 se dissolvant complètement en 30 à 60 secondes. La majeure partie du CO2 circulant est éliminée par les poumons en un seul passage. Il n’existe pas en théorie de limite de dose si un intervalle libre, laissant suffisamment de temps à son élimination, est respecté entre les injections (< 100 cc toutes les 2 minutes).
Flottabilité : conséquences sur l’opacification
La flottabilité est définie comme la tendance d’un corps à flotter quand il est immergé dans un fluide. Celle du CO2 est élevée et il va flotter au-dessus du sang (figure 1). Cette caractéristique clé du CO2 affecte grandement son utilisation correcte comme moyen d’imagerie vasculaire.
Figure 1. Flottabilité élevée du CO2. Par analogie avec l’injection d’hélium dans un arbre creux, le CO2 va opacifier préférentiellement les branches les plus ventrales (il va « flotter » au-dessus du sang) et le sang va se retrouver dans les branches les plus dorsales.
D’après Kyung J. Cho, Irvin F. Hawkins, Carbon dioxide angiography : principles, techniques, and practices, https://doi.org/10.3109/9781420016260).
Ainsi, le sang va se retrouver préférentiellement dans une position plus déclive que le CO2 (régions du corps dites « dépendantes » de la gravité qui sont les plus dorsales) et le CO2 dans une position plus proclive (régions dites « non dépendantes » de la gravité qui sont les plus ventrales).
Ainsi, la qualité d’opacification des vaisseaux va varier en fonction de leur localisation ventrale ou dorsale. Comme le CO2 va se retrouver préférentiellement sur les régions ventrales, le remplissage sera meilleur au niveau des artères du tronc cœliaque, mésentérique supérieure, mésentérique inférieure, plutôt que dans les artères rénales et hypogastriques. De la même manière, en ce qui concerne les extrémités, la mise en position de Trendelenburg avec surélévation des membres inférieurs de 15-20 va améliorer leur remplissage, le CO2 allant se loger dans les régions les plus ventrales.
Les précautions à prendre en conséquence à cette flottabilité élevée du CO2 sont de ne pas réaliser d’injection en décubitus ventral en raison du risque d’ischémie médullaire par passage du CO2 dans les artères médullaires et de ne pas réaliser d’injection tête surélevée car le CO2 peut flotter à contre-courant jusqu’à la circulation cérébrale ; cette propriété explique le risque de piégeage du CO2 dans une structure anatomique ventrale (artère pulmonaire, anévrisme de l’aorte abdominale).
Viscosité ultra faible/diffusibilité élevée
Le CO2 a une viscosité très faible, 400 fois inférieure à celle d’un PCI, ce qui permet une injection manuelle facile à travers des cathéters de petit calibre. Un volume de CO2 suffisant pour l’imagerie aortique peut être facilement injecté manuellement à l’aide d’un cathéter de diagnostic multitroué, 3 ou 4 F. Les propriétés gazeuses du CO2 entraînent un reflux central depuis le point d’administration. Cela permet une excellente évaluation de la maladie ostiale sans avoir besoin d’une angiographie de retrait de cathéter ou d’obliquités multiples. Cette caractéristique est très avantageuse lors d’interventions ostiales telles que la pose d’endoprothèses rénales et mésentériques.
Le CO2 est 20 fois plus soluble que l’air, le rendant beaucoup moins occlusif. Il est transporté dans le sang principalement sous forme d’ions bicarbonate. En administration intravasculaire, il est dissous en 30-60 secondes. S’il persiste au-delà de ce délai, il faut suspecter une contamination par l’air ou bien un piégeage (trapping) dans une structure anatomique.
Non miscibilité et déplacement de liquide
Lors de son injection intravasculaire, le CO2 déplace le sang au lieu de se mélanger à celui-ci. Ainsi, contrairement au PCI, il ne subit pas de dilution progressive, ce qui permet une excellente visualisation des veines centrales et d’autres structures vasculaires de grande taille et de grande capacité. La quantité de CO2 à injecter devra être suffisante afin de provoquer un déplacement complet de la colonne sanguine. Ainsi, celle-ci va dépendre de la taille du vaisseau à opacifier (plus le vaisseau à opacifier est grand, plus grande devra être la quantité injectée), pouvant atteindre jusqu’à 100 cc pour une aortographie (figure 2). Si le volume de CO2 injecté est insuffisant, la colonne sanguine va être déplacée de manière incomplète, conduisant à une sous-estimation du calibre du vaisseau (figure 3). Les vaisseaux de taille inférieure à 10 mm, sont mieux opacifiés par le CO2 que les vaisseaux plus gros(8).
Figure 2. Aortographies au CO2. A : Opacification moins bonne des hypogastriques en raison de leur naissance postérieure. B : Image artefactée par l’interposition des gaz digestifs. L’utilisation de glucagon par voie IV, diminuant le péristaltisme, peut améliorer l’imagerie.
Figure 3. Le CO2 déplace la colonne sanguine sans se mélanger avec le sang. AMS : artère mésentérique supérieure. AMI : artère mésentérique inférieure.
Incolore et inodore
C’est une caractéristique indésirable du CO2 qui le rend impossible à distinguer visuellement de l’air. Par conséquent, une mauvaise application des mesures de protection peut entraîner une contamination de l’air, avec de graves complications (phénomènes d’embolisation gazeuse). Cette contamination par l’air survient rapidement (figure 4) en raison de la diffusion rapide du CO2 et de la grande différence de pression partielle entre le système d’injection et l’atmosphère (CO2 dans l’atmosphère 0,03 %, CO2 dans la seringue 99,9 %). Ainsi en cas d’utilisation d’un système d’injection en contact avec l’atmosphère (une seringue), le CO2 va très vite diffuser à l’extérieur de la seringue et va être remplacé par de l’air à une vitesse de 0,2 cc/s (soit jusqu’à 2 cc en 10 s)(9) d’où la nécessité d’utiliser un système de délivrance clos.
Figure 4. Le CO2 est remplacé par de l’air à une vitesse de 0,2 cc/s. Contamination par l’air du système d’injection non détectable en raison de l’invisibilité du CO2 avec un risque d’embolie gazeuse.
Compressibilité
Comme il s’agit d’un agent gazeux, le CO2 est compressible, ce qui peut entraîner une accumulation de pression lorsqu’il est injecté à travers un cathéter d’administration qui n’a pas été purgé de son contenu liquide. Il obéit à la relation :
« Pression × Volume = Constante » à une température donnée. La conséquence est qu’une seringue peut être remplie par une quantité indéterminée de CO2 qui peut être comprimé par son piston. Lors de l’injection, le CO2 va se retrouver au niveau vasculaire dans un environnement de plus basse pression qu’à l’intérieur de la seringue où il était comprimé par le piston. Ceci va entraîner une expansion de son volume (Pression × Volume = Constante) qui peut occasionner une administration dite « explosive »(10). Ce phénomène peut entraîner une distension de l’adventice des vaisseaux, occasionnant des douleurs qui peuvent induire des mouvements du patient pendant l’acquisition dégradant la qualité de l’image. Très rarement peuvent survenir des phénomènes de barotraumatisme. Cette expansion des vaisseaux peut conduire parfois à une surestimation de leur calibre(11).
Faible absorption des rayons X et nécessité de post-traitement numérique
Le CO2 est moins dense que les PCI, avec un coefficient d’absorption aux rayons X plus bas. L’imagerie au CO2 nécessite une soustraction digitale et un post-traitement avec inversion et rehaussement du contraste (figure 5) car, sur les images brutes, il apparaît en négatif (« blanc »).
Figure 5. Angiographies du trépied fémoral (A, B) au CO2. À gauche, les images brutes et, à droite, après post-traitement (« inversion du contraste »).
CONSIDÉRATIONS TECHNIQUES
Quantité de CO2 à injecter
Comme vu précédemment, la quantité de gaz à injecter dépend de la taille de l’artère à opacifier :
– aorte abdominale : 60-100 ml ;
– axes iliaques : 40-80 ml ;
– axes fémoropoplités : 40-60 ml ;
– artères rénales : 20-40 ml ;
– troncs digestifs : 20-40 ml.
SURVEILLANCE
Les procédures endovasculaires au CO2 nécessitent une surveillance de la saturation en O2, la fréquence respiratoire, la pression artérielle, la fréquence cardiaque, l’électrocardiogramme (± capnographie si disponible). Il faut éviter une sédation profonde en raison des difficultés à distinguer les effets de l’anesthésie versus ceux induits par une contamination par de l’air du système d’injection (dépression respiratoire/hypotension). L’anesthésie au protoxyde d’azote (N20) est également à éviter car les bulles de protoxyde d’azote vont diffuser à l’intérieur des bulles de CO2 avec comme conséquence une augmentation de la taille des bulles de CO2 d’un facteur 5 à 6. Ainsi, une injection de 100 cc de CO2 va avoir l’effet d’une injection de 500 à 600 cc avec un caractère occlusif des bulles et un risque de piégeage.
OPTIMISATION DE L’IMAGE
En raison de la faible densité du gaz, il est nécessaire d’effectuer une soustraction digitale, et un rehaussement du rapport signal/bruit pour accentuer le contraste(12). Ces opérations de postprocessing après l’acquisition d’une séquence d’images numériques sont accessibles sur tous les systèmes contemporains équipant les salles de cathétérisme, et sont en grande partie à l’origine du revival de la méthode, dont la limite technique originelle était liée au faible contraste naturel généré. L’acquisition des séries en position Trendelenburg, possible sur les salles modernes, optimise encore la qualité des images (figure 6).
Figure 6. Occlusion de la tibiale antérieure et du tronc tibiopéronnier. Recanalisation par voie sous-intimale et angioplastie au ballon de la péronière. Des injections sélectives en position de Trendelenburg le plus proche possible de la lésion et après administration de dérivés nitrés offrent la meilleure qualité d’image.
IRRADIATION
L’imagerie au CO2 requiert d’augmenter la cadence image (4/sec) ce qui a comme effet d’accroître l’exposition aux rayons X. Mais ceci est contrebalancé par l’arrivée rapide du gaz qui va raccourcir la durée d’acquisition et diminuer l’irradiation. Ainsi, finalement, l’utilisation de CO2 comme agent de contraste intravasculaire n’augmente pas l’irradiation du patient et de l’opérateur.
EFFETS SECONDAIRES ET COMPLICATIONS
La survenue et la gravité des complications lors de l’angiographie au CO2 sont souvent directement liées à l’un des facteurs suivants : dose excessive délivrée dans un court laps de temps, contamination de l’air, piégeage dans l’arbre vasculaire où le CO2 a été délivré. L’incidence rapportée des effets indésirables avec l’angiographie au CO2 varie considérablement, de rare à 17 %. Dans une étude rétrospective monocentrique chez 951 patients sur 21 ans dont 627 en utilisation artérielle, la mortalité globale a été de 0,4 % avec absence de décès lié au CO2. Dans une étude prospective multicentrique de 98 patients insuffisants rénaux(13), l’utilisation de CO2 n’a pas entraîné de dégradation de la fonction rénale, a permis une diminution de la quantité de PCI injecté sans l’annuler complétement, mais 2 décès sont survenus, attribués à une ischémie digestive.
Heureusement, presque tous les effets indésirables signalés sont mineurs et transitoires. L’aortographie au CO2 peut provoquer des nausées et des douleurs abdominales qui durent 2 à 3 minutes. La cause est probablement due au piégeage transitoire du CO2 dans les artères mésentériques et se résout rapidement lors de la réabsorption du gaz. Aucun traitement spécifique n’est nécessaire, bien que la rotation du patient d’un côté à l’autre et le massage doux de l’abdomen puissent améliorer la réabsorption du CO2 (figure 7).
Figure 7. Piégeage du CO2 sur la partie non dépendante d’un anévrisme de l’aorte abdominale avec obstruction de l’artère mésentérique inférieure pouvant provoquer des phénomènes d’ischémie digestive. Le traitement consiste à changer de position le patient afin de mobiliser le CO2.
TC : tronc cœliaque, AMS : artère mésentérique supérieure, AMI : artère mésentérique inférieure. D’après Kyung J. Cho, Irvin F. Hawkins, Carbon dioxide angiography : principles, techniques, and practices, https://doi.org/10.3109/9781420016260).
La douleur ou les crampes aux jambes sont également un phénomène bénin courant lors de l’injection sélective de CO2 des membres inférieurs.
La contamination par l’air est l’une des complications les plus graves qui puisse survenir lors de l’angiographie au CO2. Les systèmes d’injection de CO2 automatisés dédiés qui ont des fonctionnalités intégrées pour assurer la pureté du gaz livré ont réduit drastiquement ce risque. Les manifestations ischémiques de l’embolie gazeuse dépendent du lit vasculaire et sont de gravité très variable ; les plus sévères impliquent une neurotoxicité et des phénomènes de sas aortiques, cardiopulmonaires ou abdominaux qui peuvent entraîner une ischémie intestinale ou un collapsus cardiovasculaire. La plupart des cas concerne de petites quantités de contamination de l’air et sont de nature spontanément résolutive. Lorsque les symptômes persistent ou lorsqu’il existe un risque de blessure irréversible, des mesures doivent être prises pour éliminer l’air intravasculaire : manœuvres positionnelles, massages, aspiration par cathéter multitroué, oxygénothérapie hyperbare et héparinisation pour prévenir la thrombose secondaire.
Les complications neurologiques(14) peuvent être en relation avec le passage du CO2 dans la circulation cérébrale ou bien liées à une contamination par l’air. Dans ce contexte, il est contre-indiqué d’injecter le CO2 en artériel au-dessus du diaphragme.
DE MULTIPLES OPTIONS POUR L’ADMINISTRATION DE CO2 À PARTIR DE SA SOURCE
Approche par injection manuelle
La configuration pour l’injection manuelle implique des insufflateurs à cylindre de CO2 de qualité médicale avec un filtre bactérien en ligne, des connecteurs de robinet d’arrêt à trois voies et des connecteurs de flux de contrôle unidirectionnels. Les avantages de cette méthode manuelle sont le timing optimal, le contrôle de l’injection, la capacité d’arrêter l’injection à tout moment, une grande disponibilité et un faible coût. Les inconvénients comprennent une exposition élevée aux rayonnements et la nature ouverte du système de distribution de CO2, avec le potentiel de contamination de l’air en cas de défaillance des composants ou d’erreur de l’opérateur.
CO2-Angioset
Le CO2-Angioset (Optimed) n’est pas disponible aux États-Unis, mais est populaire en Europe et dans le monde entier. Il présente les avantages de la simplicité, de la portabilité et d’une sécurité accrue par rapport aux systèmes manuels. Le kit se compose d’une cartouche de CO2 dédiée et bien marquée de qualité médicale, d’une soupape de surpression assurant la purge de toute augmentation de pression excessive, d’un filtre stérile, d’un robinet d’arrêt à trois voies et d’une seringue dédiée de 100 ml permettant d’ajuster le volume délivré par incréments de 20 ml. Il est acquis que le système est sûr, facile à utiliser et hautement diagnostique, même dans les segments artériels infrapoplités (figure 8).
Figure 8. Schéma des constituants d’un des injecteurs semi-automatiques disponibles sur le marché (Optimed).
Injecteurs automatisés Comme pour les PCI, l’injection automatisée de CO2 offre plusieurs avantages, notamment un contrôle précis du moment de l’injection, de la pression et du volume, et la réduction de l’exposition aux rayonnements de l’opérateur. Récemment, l’intérêt pour l’injection automatisée de CO2 a refait surface avec l’introduction en Europe de l’injecteur Angiodroid (Angiodroid SRL). Cet injecteur de CO2 informatisé de nouvelle génération présente l’avantage d’être fiable, polyvalent et convivial. L’appareil calcule la quantité de gaz à injecter dans le récipient et, par conséquent, purge automatiquement l’air, vérifie la pureté du CO2 et détermine le volume délivré et la pression d’injection (figure 9).
Figure 9. Système automatique Angiodroid.
ESSAIS CLINIQUES ET ANGIOPLASTIE ARTÉRIELLE AU CO2
Qualité des angiographies
À l’étage fémoropoplité, de Almeida et al. ont mis en évidence la faisabilité des angioplasties artérielles au CO2 dans les lésions TASC A et B avec une bonne concordance interobservateur du degré de sténose et une diminution des coûts liés à la non-utilisation de PCI(15).
L’essai a été prospectif, randomisé, mais la population incluse était faible (35 patients).
Des conclusions similaires ont été mises en évidence dans un essai prospectif randomisé de plus grande envergure ayant inclus 98 patients insuffisants rénaux, avec un DFG < 60 ml/min présentant 109 lésions traitées par angioplastie (31 à l’étage iliaque, 62 à l’étage fémoral superficiel et 16 à l’étage rénal) avec des angiographies interprétables respectivement dans 83,9, 98,4 et 56,2 % des cas selon le niveau anatomique.
Madhusudhan et al.(16) ont étudié 113 segments artériels chez 21 patients avec une lecture par deux observateurs en analysant les angiographies successivement par PCI et CO2. Le degré de sténose était le même entre CO2 et PCI dans 79,7 % des segments artériels étudiés ; 15,5 % des segments artériels étaient mieux évalués par les PCI et 4,9 % par le CO2. En excluant les segments infrapoplités, 91,8 % des segments artériels sont correctement évalués. En ce qui concerne ces lésions infrapoplitées, les performances du CO2 sont moindres que sur les segments artériels proximaux et cela est bien documenté dans la littérature avec une tendance à surestimer le degré de sténose en utilisant le CO2.
Afin d’optimiser la visualisation des segments infrapoplités, il est recommandé de faire des injections sélectives le plus proche possible de la lésion permettant d’éviter la « fragmentation » de la colonne de CO2 et d’administrer des dérivés nitrés. Enfin, dans les cas restants douteux, il est légitime d’effectuer des injections de petites quantités de PCI. En dehors des lésions infrapoplitées. L’artère iliaque interne est également moins bien visualisée (évaluation correcte que dans 59,3 %(16)). Ceci est dû à son origine anatomique qui est postérieure ainsi qu’à l’interposition des gaz digestifs. La figure 10 illustre la comparaison d’images de segments artériels obtenues successivement au CO2 et aux PCI.
Figure 10. Comparaison d’images obtenues par CO2 et PCI. A : sténose à l’entrée du stent de la fémorale superficielle. B : sténose de la partie proximale de la tibiale antérieure et occlusion de la tibiale postérieure. C : sténose de la fémorale superficielle avec présence d’un stent sur sa partie distale.
Palena et al.(17) dans une étude menée sur 36 patients atteints d’ischémie critique des membres traités par angioplastie au CO2 (Système Angiodroid), n’ont rapporté aucune différence statistique significative dans la précision du diagnostic qualitatif entre les deux contrastes(6). De plus, Mascoli et al. ont montré sur 31 procédures de réparation endovasculaire d’anévrisme (EVAR) qu’une procédure standardisée peut être efficacement réalisée grâce à un dispositif automatisé(18).
B. Woerly et al. rapportent les résultats de 785 gestes endovasculaires sur les artères des membres inférieurs effectués entre juillet 2020 à juin 2021, dont 564 sur les 785 ont été réalisées utilisant le CO2 comme agent de contraste de première intention à l’aide de l’injecteur automatique Angiodroid(19). Aucun événement indésirable ou complication résultant de l’utilisation de CO2 n’a été signalé. Après 1 an d’utilisation de ce système, la consommation de PCI a été réduite de plus de 85 % à l’origine d’une économie substantielle.
Liens d’intérêts : les auteurs déclarent n’avoir aucun lien d’intérêt en rapport avec l’article.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


