Mise au point
Publié le 30 nov 2015Lecture 6 min
TAVI - Les résultats avec les valves de dernière génération Edwards SAPIEN 3 et Medtronic Evolut™ R
N. BETTINGER, E. DURAND, C. TRON, H. ELTCHANINOFF, service de cardiologie, CHU de Rouen
La prise en charge du rétrécissement aortique a considérablement évolué au cours de la dernière décennie avec l’avènement des valves aortiques implantées par voie percutanée. Alors que les premières implantations ont été effectuées chez des patients compassionnels(1,2), le traitement par voie percutanée a désormais sa place dans les recommandations des sociétés européenne et américaine(4) de cardiologie. Il est indiqué chez les patients porteurs d’un rétrécissement aortique serré symptomatique, récusés pour une prise en charge chirurgicale conventionnelle et dont l’espérance de vie est supérieure à 1 an. Il s’agit donc de patients à haut risque chirurgical (Euroscore logistique ≥ 20 %, score STS > 10 %), ou inopérables du fait de leurs comorbidités (aorte porcelaine, irradiation thoracique, antécédent de pontage aortocoronaire) ou de leur « fragilité »(5). La décision de traiter ces patients par TAVI plutôt que par chirurgie doit être le résultat d’une discussion pluridisciplinaire au sein de la Heart Team.
L’évolution des indications passe par une amélioration des prothèses implantées. Ces améliorations ont notamment pour objectif de limiter les principaux risques liés aux TAVI (transcatheter aortic valve implantation), comprenant essentiellement l’insuffisance aortique paravalvulaire, les complications vasculaires et le risque d’accident vasculaire cérébral (AVC). C’est dans ce sens que les deux valves dominant actuel lement le marché, la valve SAPIEN 3 (Edwards Lifesciences) et la CoreValve® (Medtronic), évoluent, avec une diminution de taille du désilet et l’apparition de systèmes permettant la limitation des fuites aortiques. Les résultats à 1 an des registres en cours avec ces deux prothèses ont été présentés lors du congrès Transcatheter Cardiovascular Therapeutics (TCT) à San Francisco au mois d’octobre.
Valve Edwards Sapien 3
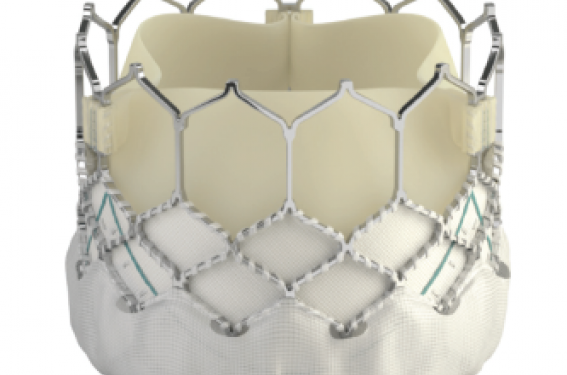
La valve SAPIEN 3 est disponible en France depuis le mois de septembre 2014, en trois diamètres : 23, 26 et 29 mm (figure 1 et tableau 1). Comparativement à la valve SAPIEN XT, elle a été modifiée avec l’ajout d’une jupe externe en tissu de polyéthylène téréphtalate entourant le stent, afin d’améliorer l’étanchéité et de limiter le risque de régurgitation aortique paravalvulaire. La forme du stent a été modifiée permettant une augmentation de la force radiale. Enfin, le diamètre de l’introducteur a été diminué, désormais de 14 F pour les valves de 23 et 26 mm, et de 16 F pour la 29 mm autorisant la voie transfémorale pour un calibre d’artère ≥ 5,5 mm pour les valves de 23 et 26 mm et ≥ 6 mm pour la valve de 29 mm. L’étude PARTNER II S3 (NCT- 01314313) est un registre, évaluant la sécurité et l’efficacité des valves SAPIEN 3 et leur système de délivrance. Les patients sont divisés en deux groupes selon leur risque chirurgical : intermédiaire (PII S3i ; n = 1 076) et haut risque ou patients inopérables (PII S3HR ; n = 583). Chaque groupe est ensuite subdivisé en deux bras selon la voie d'abord (transfémorale et transapicale/transaortique).
Les résultats à 30 jours dans les deux cohortes ont été présentés par Susheel Kodali (Colombia, New York) à l'ACC en mars 2014 et les résultats à 1 an dans la cohorte PII S3HR ont été présentés par Howard Herrman (Philadelphie, Pennsylvanie) au TCT en octobre 2014 (tableau 2).
Figure 1. Valve Edwards SAPIEN 3.
Résultats exprimés en pourcentage (%).
La cohorte S3HR
Elle a inclus 583 patients d'un âge moyen de 82,6 années avec un score STS moyen de 8,6 %, dont 84 % ont été implantés par voie fémorale, 10 % par voie transapicale et 6 % par voie transaortique. À 30 jours, la survie était de 97,8 %. On a noté de très faibles taux de complications avec 1,4 % d’AVC ; 2,5 % de régurgitations aortiques paravalvulaires significatives (modérées, absence de fuite sévère) et 13,3 % d’implantation de stimulateur cardiaque. La survie à 1 an a été de 85,6 % (82,3 % chez les patients inopérables et 87,3 % chez les patients à haut risque ; p = NS). Elle a été significativement meilleure chez les patients implantés par voie fémorale que chez ceux implantés par voie transapicale ou transaortique (87,7 % vs 74,7 % ; p = 0,0006). À titre de comparaison, dans l’étude PARTNER I, la survie à 1 an était de 75,8 % dans la cohorte A (patients à haut risque chirurgical)(6) et de 69,3 % dans la cohorte B (patients inopérables)(7).
En ce qui concerne les complications, le taux d’AVC à 1 an était de 4,3 %, ceux entraînant une perte d’autonomie (score de Rankin ≥ 2) étant seulement de 2,4 %. Le taux d’implantation de stimulateur cardiaque était de 16,9 % et le taux de régurgitations aortiques ≥ modérée (grade II) était de 2,7 % à 1 an. Alors que dans l’étude PARTNER I, il y a eu une surmortalité significative chez les patients présentant une insuffisance aortique légère ou modérée/sévère(8), dans PARTNER II S3, seuls les patients présentant une insuffisance aortique ≥ modérée ont eu une réduction significative de survie à 1 an, comparativement aux patients avec une insuffisance aortique légère ou inexistante (61,9 %, 85,9 % et 88 % respectivement).
Les données échographiques ont montré une réduction du gradient aortique moyen de 45,5 à 11,3 mmHg et une augmentation de la surface valvulaire de 0,67 à 1,67 cm2. Sur le plan fonctionnel, les patients en stade III/IV de la NYHA sont passés de 90,1 % à l’état basal à 7,7 % à 1 an.
La cohorte S3i
Elle a inclus 1 076 patients d'âge moyen de 81,9 années avec un score STS moyen de 5,3 % dont 89 % ont été implantés par voie transfémorale, 7 % par voie transapicale et 4 % par voie transaortique. À 30 jours, la mortalité totale était très faible (1,1 %). La mortalité à 30 jours était la plus faible par voie transfémorale (1,1 %) en comparaison avec la voie transapicale (5,4 %) et transaortique (1,6 %). Les taux de complications étaient également très prometteurs puisque 2,6 % des patients ont présenté un AVC (dont 1 % avec des séquelles importantes) ; 5,6 % ont présenté une complication vasculaire majeure ; 10,1 % ont nécessité la pose d'un pacemaker. Les données du suivi à 1 an n'ont pas encore été présentées.
Valve Medtronic Evolut™ R
Cette valve est disponible en 3 diamètres : 23, 26 et 29 mm (figure 2). Par rapport à la CoreValve®, la valve Medtronic Evolut™ R a une portion aortique réduite en hauteur, un oversizing optimisé, une force radiale plus importante et une extension de la jupe à sa portion ventriculaire. Ces modifications permettent d’optimiser le positionnement de la valve, une diminution des troubles conductifs et une réduction des fuites aortiques paravalvulaires. Elle est également implantée à l’aide d’un cathéter de diamètre inférieur, de 14 F permettant un abord transfémoral pour un diamètre artériel ≥ 5 mm. Cette valve est recapturable, repositionnable et récupérable si nécessaire, permettant un déploiement optimal et précis. Enfin, l’une des particularités de cette valve autoexpansible en nitinol est de pouvoir adapter sa forme dans des anneaux non circulaires ou étant le siège de volumineuses calcifications.
G. Manoharan et al. ont publié les résultats de l’Evolut™ R à 30 jours dans une étude pilote(9) (tableau 3). L’étude a inclus 60 patients avec un score STS moyen à 7,0 %. Parmi eux, 98,3 % ont été implantés par voie fémorale. Concernant les complications, la survie a été de 100 % à 30 jours, et il y a eu 11,7 % d’implantations de stimulateur cardiaque, 8,3 % de complications vasculaires, 3,4 % de régurgitation aortique paravalvulaire (≥ modérée) et aucun AVC. Il n’y a pas eu d’échec de recapture de la valve pour la repositionner sur les 22 tentatives répertoriées.
Résultats exprimés en pourcentage (%).
Jeffrey J. Popma (Boston, Massachussetts) a présenté les résultats de cette étude à 1 an (tableau 3). Le taux de survie était de 93,3 % et il y a eu 3,4 % d’AVC (entraînant un handicap) ; 15,2 % d’implantations de stimulateurs cardiaques ; 8,3 % de complications vasculaires et 4,3 % de régurgitation aortique paravalvulaire (≥ modérée). De facon intéressante, les auteurs ont retrouvé une profondeur d’implantation majorée chez les patients implantés d’un pacemaker en postprocédure (3,3 ± 2,5 mm vs 8,1 ± 3,5 mm ; p < 0,001). Les données écho-graphiques montraient une réduction du gradient aortique moyen de 49,1 à 7,5 mmHg et une augmentation de la surface valvulaire de 0,6 à 1,9 cm2.
Sur le plan fonctionnel, les patients en stade III/IV de la NYHA sont passés de 91,7 % à l’état basal à 6,1 % à 1 an (49 patients).
Figure 2. Valve Medtronic Evolut™ R.
Conclusion
Ces dernières générations de valve présentent donc des taux d’événements à 1 an plus faibles que celles des générations précédentes et un taux de survie excellent.
Les régurgitations aortiques paravalvulaires significatives et ayant un impact sur la survie à moyen et long termes tendent à disparaître. Le taux d’AVC diminue, probablement en lien avec la diminution de diamètre du système de délivrance de la valve.
Enfin, le taux d’implantation de stimulateurs reste non négligeable et semble comparable pour les deux types de prothèse.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


