Focus
Publié le 29 juin 2021Lecture 25 min
Usage de cannabis récréatif : marqueur de risque ou facteur causal d’infarctus du myocarde ?
Jean-Marc PERNÈSa, Guillaume DURAND-VIELb, Pôle cardiovasculaire interventionnel(a) (PCVI 92) et Unité de soins intensifs cardiologie(b), Hôpital Privé d’Antony
M. G. est un homme de 29 ans adressé directement en salle de cathétérisme dans un contexte de syndrome coronaire aigu (SCA) et d’un sus-décalage du segment ST dans les dérivations antérieures sur l’ECG effectué à H5 d’une douleur thoracique constrictive persistante, l’ensemble signant le diagnostic d’infarctus ST+ (STEMI). Cet épisode douloureux persistant succédait à une phase de douleurs identiques et intermittentes survenues dans les 3 jours précédents.
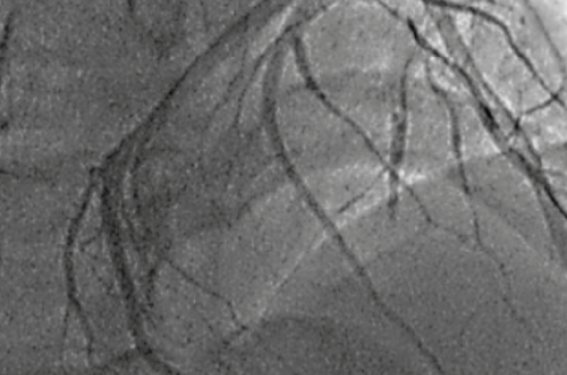
L'interrogatoire révèle une consommation ancienne et importante de cannabis, majorée ces derniers jours avec une dernière prise 3 heures avant l’installation de la dou- leur permanente ; M. G. consommait jusqu’à 30 « joints » par jour depuis l’âge de 15 ans, mais avait réduit ces dernières années, à 5 joints par jour. Un tabagisme chronique (15 paquets années) est associé, sans prise reconnue de cocaïne, ancienne ou récente. La coronarographie met en évidence une occlusion de l’IVA moyenne et la présence de thrombus « frais » s’étendant également dans une importante collatérale diagonale (figure 1). Le reste du réseau coronaire épicardique est strictement sain (figure 2).
Figure 1. Thrombus dans la diagonale et l’IVA moyenne, occluse.
Figure 2. Réseau coronaire sain.
La mise en place directe et sans prédilatation de deux stents, respectivement dans l’IVA et la diagonale, permet de rétablir un flux normal, TIMI 3, dans ces deux artères (figures 3 à 5). L’évolution immédiate est simple avec un taux de troponine US à 31 000 ng/l, une akinésie apicale et une fraction d’éjection à 45 %. Le cannabis est la drogue illicite la plus consommée dans le monde, en Europe et en France(1) . Son principal composé psychoactif est le delta-9 tétrahydrocannabinol (THC), classé comme stupéfiant. Il est souvent considéré par les usagers comme sans danger pour la santé et si les effets psychiatriques et neuropsychiques du cannabis sont depuis longtemps largement décrits(2), les effets somatiques du cannabis fumé, notamment cardiovasculaires et neurovasculaires ne sont rapportés que depuis peu. Les premiers cas de complications touchant la sphère cardiovasculaire ont été décrits dans les années 1960 et les publications se sont multipliées depuis les années 2000, essentiellement sous forme de cas cliniques et de revues de littérature, alors que peu d’études épidémiologiques ont été réalisées. Au vu du développement de la littérature scientifique sur le sujet et à l’occasion d’un cas clinique symbolique d’infarctus chez un jeune consommateur, il est judicieux de dresser un état des lieux des connaissances sur les risques de survenue d’infarctus du myocarde (IDM) potentiellement engendrés par la consommation du cannabis et ses dérivés synthétiques, posant ainsi la question de la réalité d’un lien de causalité entre son usage et le déclenchement d’IDM qui, s’il n’est pas démontré, est fortement suggéré par l’existence d’une relation temporelle entre la survenue de cet événement et la prise de cannabis.
Figure 3. Guides, alternativement dans la diagonale et l’IVA.
Figure 4. Mise en place des stents IVA et diagonale.
Figure 5. Résultat final.
Cannabis : de quoi parle-t-on ?
Papier, textile, corde, huile, protéines, isolant, biocarburant, parpaings, etc., le chanvre est une plante d’une polyvalence unique dans le règne végétal, mais le chanvre industriel ne se fume pas ! En effet, le Cannabis sativa contient à l’état naturel trop peu de THC, la substance psychoactive euphorisante, pour produire un quelconque effet. Le cannabis, nom latin du chanvre, ou chanvre récréatif, est en fait du Cannabis sativa sélectionné sur des générations pour concentrer le THC à des valeurs supérieures à 1,5 % (< 0,2 % en moyenne pour le chanvre industriel). Les feuilles, fleurs et tiges du cannabis produisent plus de 500 composés distincts répartis en 18 classes chimiques différentes et hébergent plus de 100 différents phytocannabinoïdes. Les principaux phyto-cannabinoïdes semblent être le delta-9-tétrahydrocannabinol (Δ9-THC, THC), le cannabinol (CBN) et le cannabidiol (CBD), bien que l’abondance relative de ceux-ci et d’autres phyto-cannabinoïdes varient en fonction des hybridations entre les 3 variétés connues de Cannabis (sativa, indica et ruderalis). Le Δ9-THC est de loin le cannabinoïde le plus étudié et est à l’origine de nombreux, si ce n’est de la plupart des effets physiques et psychotropiques du cannabis. D’autres phytocannabinoïdes (tels que le CBD, le CBC et le CBG) sont présents en moindre quantité dans la plante et ont peu de propriétés psychotropiques, voire aucune(3).
Le cannabis fait l’objet d’utilisations très diverses : sous forme de chanvre, il est cultivé pour des usages industriels (textile, papeterie, isolation, alimentation animale, etc.), principalement en Chine, en Europe et au Canada. Il peut également être produit de façon légale pour des usages médicaux, usages remontant à plusieurs millénaires (il était alors utilisé pour ses qualités antalgiques, antispasmodiques et anti-inflammatoires en Chine, en Inde et au Moyen-Orient), qui s’étaient perdus au fil du temps avant de connaître un regain d’intérêt à partir des années 1990. Enfin, il fait l’objet d’usages non médicaux dits « récréatifs » — légaux ou plus souvent illégaux—, pour ses propriétés psychoactives : il est alors le plus souvent fumé, sous forme d’herbe (marijuana) ou de résine (haschich) avec du tabac.
Le cannabis a été utilisé comme substance euphorisante depuis au moins 4 000 ans et demeure aujourd’hui la drogue illicite la plus populaire au monde. Selon le World Drug Report de 2020(4), on estime que 192 millions de personnes ont consommé du cannabis en 2018, soit environ 5 % de la population mondiale, cette proportion étant encore plus élevée en Amérique du Nord, avec 43 % des petits américains de moins 12 ans avouant une utilisation dans l’année 2019. Depuis 2012, deux pays (Uruguay et le Canada) et 33 états américains sur 50 ont dépénalisé, légalisé et régulé la culture, la vente, la détention et la consommation de cannabis pour les adultes, à des fins récréatives, après en avoir autorisé l’usage à des fins médicales. Ainsi, en 2021, dans le troisième pays le plus peuplé du monde, plus d’un quart des habitants expérimentent un régime légal autorisant la consommation de cannabis à titre non médical pour les adultes (soit 92 millions de citoyens)(5).
En 2014, 17 millions de personnes âgées de 11 à 75 ans ont expérimenté, forcément illégalement, le cannabis au cours de leur vie, en France métropolitaine, dont 4,6 millions en ont consommé dans l’année, 1,4 million en font un usage régulier (au moins 10 fois dans le mois) et 700 000 en consomment tous les jours(6). L’usage au cours des 12 derniers mois concernait surtout les plus jeunes : 38 % chez les jeunes de 17 ans, 28 % chez les 18-25 ans et 11 % chez les 18-64 ans. Les premiers sont 9 % à en faire un usage régulier(7). Parmi les usagers au cours des 12 derniers mois, 21 % présentaient un risque élevé d’usage problématique de cannabis.
En 20 ans, le marché des drogues en France a connu des mutations considérables. La première consiste en la diversification importante des produits proposés sur fond de fortes progressions des consommations. Entre 2000 et 2017, chez les 18-64 ans, les usages dans l’année de cannabis ont fortement augmenté, passant de 8 à 11 %, ceux de cocaïne étant multipliés par plus de cinq, passant de 0,3 à 1,6 %, tandis que ceux d’ecstasy sur la même période étaient multipliés par cinq (de 0,2 à 1 %). Apparus en France aux alentours de 2008, les nouveaux produits de synthèse (NPS) constituent un ensemble hétérogène de substances, potentiellement infini. Les cannabinoïdes de synthèse (CS) constituent la famille de NPS dont la cible potentielle, les usagers de cannabis, apparaît la plus large. L’expérimentation des CS concernait en 2014 jusqu’à 4 % des 18-34 ans(6).
À partir du milieu des années 2000, le dispositif TREND commence à faire état du développement de pratiques, notamment chez les usagers intensifs de cannabis, tendant à privilégier l’herbe ( jugée plus naturelle) au détriment de la résine considérée comme un produit « bas de gamme » de qualité médiocre(8). Si la fin des années 2000 a marqué en France la fin du cycle hégémonique de la résine, la production marocaine s’est adaptée en fabriquant des produits plus puissants grâce à l’introduction de variétés hybrides à teneur élevée en THC(9). Ainsi, entre 2010 et 2019, le taux moyen en THC de la résine saisie en France a presque triplé, passant de 10,5 à 28,2 %(10). Cette forte hausse des taux de THC pose question quant aux risques induits.
Effets physiologiques du cannabis récréatif sur le système cardiovasculaire
Pour bien comprendre l’impact du cannabis sur le système cardiovasculaire, il est impératif d’intégrer le fonctionnement du système endocannabinoïde (SEC).
Le SEC est un ancien système de signalisation lipidique ubiquiste, conservé au cours de l’évolution, que l’on retrouve chez tous les vertébrés, lequel semble jouer un très grand rôle de régulation dans tout le corps humain(11). Le SEC participe à la régulation d’un nombre très vaste de processus physiologiques et physiopathologiques, dont le développement du système nerveux, la fonction immunitaire et cardiovasculaire, l’inflammation, l’appétit, le métabolisme et l’homéostasie énergétique, la digestion, le développement osseux, la densité osseuse, la plasticité synaptique et l’apprentissage, la douleur, la reproduction, la maladie psychiatrique, le comportement psychomoteur, la mémoire, les cycles de veille et de sommeil ainsi que la régulation du stress, de l’état émotionnel et de l’humeur(12). En outre, tout porte à croire que le dérèglement du SEC contribue à de nombreuses maladies chez l'humain et engendre notamment de la douleur, de l'inflammation, des troubles psychiatriques.
Le SEC est principalement composé des récepteurs de cannabinoïdes 1 et 2 (CB1 et CB2), des endocannabinoïdes (dérivés d’acide arachidonique, synthétisés « sur demande », en réponse à un potentiel d'action dans les neurones ou en réponse à un autre type de stimulus biologique), des enzymes de synthèse et de dégradation des endocannabinoïdes.
Les endocannabinoïdes tels que l’anandamide et le 2-AG, de même que les phytocannabinoïdes du cannabis (THC, CBN et bien d’autres), se lient, avec affinité et efficacité variantes, aux récepteurs CB1 et CB2.
La plupart des tissus sont dotés d’un SEC fonctionnel, les récepteurs CB1 et CB2 disposant de schémas distincts d’expression tissulaire. Le récepteur CB1 est l’un des récepteurs couplés aux protéines G les plus abondants dans les systèmes nerveux central et périphérique. Le récepteur CB1 s’exprime également dans plusieurs autres organes et tissus, dont le cœur, la paroi vasculaire, les poumons, l’appareil gastro-intestinal, les reins, la vessie, etc. Les récepteurs CB2 sont plus fortement concentrés dans les tissus et les cellules du système immunitaire tels que les leucocytes et la rate (figure 6).
Figure 6. Les récepteurs à endocannabinoïde CB1 et CB2.
CB1 est le principal récepteur qui médie les effets du THC et impliqué comme le « coupable » potentiel dans bon nombre des effets cardiaques alors que le rôle du récepteur CB2 dans les effets cardiovasculaires reste encore mal connu.
Les effets physiologiques du cannabis sur le système cardiovasculaire s’exercent en premier lieu sur le système nerveux autonome (SNA), mais également sur la demande myocardique en oxygène (O2), les plaquettes et l’endothélium vasculaire(13).
Dysfonction du SNA
La mise en jeu du SEC affecte à la fois les systèmes nerveux sympathique et parasympathique. Fumer de la marijuana entraîne une tachycardie immédiate et une pression artérielle en position couchée élevée. Dans une étude réalisée par P. Baconsfirld et al.(14), un effet immédiat de l’inhalation de marijuana, survenant dans les 10 minutes, est une augmentation de 20 à 100 % de la fréquence cardiaque, pouvant durer entre 2 et 3 h. L’augmentation de la fréquence cardiaque est principalement médiée par l’activation du récepteur CB1. Dans une étude où un antagoniste des récepteurs sélectifs CB1 a été utilisé, l’augmentation moyenne de la fréquence cardiaque maximale a été diminuée de 59 % chez les volontaires en bonne santé qui fumaient de la marijuana 2 h avant le contrôle(15). D’autre part, la marijuana peut inhiber l’innervation parasympathique cardiaque, comme en témoigne le fait que la marijuana réduit la bradycardie vagale pendant la manœuvre de Valsalva(16). L’effet biphasique des cannabinoïdes semble dose dépendant comme l’indiquent certaines études, où des doses plus faibles ont causé une stimulation sympathique et la libération de noradrénaline tandis que des doses plus élevées ont entraîné une stimulation parasympathique(17,18). Les principaux effets physiologiques de la marijuana peuvent être résumés comme une augmentation de la fréquence cardiaque, un tonus sympathique accentué, des niveaux accrus de catécholamines à des doses faibles, et la bradycardie/hypotension à des doses plus élevées. Ces effets sur le système nerveux autonome contribuent en grande partie aux mécanismes pathophysiologiques sous-tendant les événements cardiovasculaires potentiellement délétères liés à la consommation de marijuana (figure 7).
Figure 7. L’impact de la marijuana sur le système cardiovasculaire. Effets cardiovasculaires les plus communs associés à l’usage de marijuana (d’après Latif et al.(13)).
La consommation de marijuana modifie l’équilibre entre l’offre et la demande myocardique en oxygène
Il a ainsi été noté que la consommation de cannabis entraîne une augmentation de l’exposition au monoxyde de carbone. R.T. Jones et al.(19) ont notamment constaté une augmentation de près de 5 fois des niveaux de carboxyhémoglobine après le tabagisme de marijuana comparé au tabagisme classique. La combinaison d’une demande accrue d’oxygène myocardique en raison de la tachycardie et d’une diminution de l’approvisionnement en oxygène liée à des niveaux élevés de carboxyhémoglobine, en rapport avec la combustion, explique ce déséquilibre qui peut avoir comme conséquence une ischémie myocardique transitoire(19).
Action procoagulante du cannabis
E. Deusch et al.(20) ont démontré la présence de récepteurs CB1 et CB2 sur les membranes cellulaires plaquettaires. En outre, il a également été démontré que l’expression de la glycoprotéine IIb-IIIa et de la P-sélectine sur les membranes plaquettaires augmente lors de l’activation des récepteurs CB1 d’une manière dépendante de la dose(21). Ces résultats suggèrent que le THC puisse agir directement sur les plaquettes et activer la cascade de coagulation initiant la formation d’un thrombus. L’activation des récepteurs CB1 et CB2 a été impliquée dans la survenue d’un dysfonctionnement endothélial, via la libération de radicaux libres (NO), dont l’interaction avec le SEC qui a été démontrée par C. Lipina et al.(22). Combinés, ces effets conduisent à un état procoagulant. Un antagoniste des récepteurs CB1 a atténué et presque inversé ces effets négatifs selon certaines études(23,24).
Vasospasme et altérations du flux coronaire
Il a été démontré que le cannabis provoque principalement des réactions de vasodilatation par l’activation transitoire des canaux cationiques dits TRPA (transient receptor potential- Ankyrin). Cependant, la vasoconstriction a pu être constatée dans les circulations coronaires, cérébrales et périphériques(25), ces effets hétérogènes étant liés à des mécanismes d’action différents du THC sur l’endothélium des territoires tissulaires sus- cités. Ainsi, A. Quercioli et al.(26) ont constaté la corrélation entre des niveaux élevés d’endocannabinoïdes dans le plasma et la réduction du flux sanguin coronaire : un vasospasme coronaire réversible induit par le cannabis est susceptible de conduire à une ischémie myocardique.
Inflammation, athérogenèse et cannabis
Les récepteurs CB1 et CB2 (RCB1 et RCB2) qui se trouvent dans les myocytes cardiaques agissent par l’intermédiaire des cellules immunitaires pour limiter l’inflammation et activer les mécanismes cardioprotecteurs. Les RCB1 et CB2 peuvent jouer des rôles antagonistes les uns par rapport aux autres dans l’athérogenèse. CB1 a des effets pro-inflammatoires sur les macrophages et les monocytes et une relation pro-athérogénique avec l’endothélium. Les RCB2 démontrent des capacités anti-inflammatoires et antiathérogéniques ainsi que la conservation de l’homéostasie lipidique(16). En raison de la nature pro-inflammatoire reconnue du RCB1, il a été supposé que les antagonistes de ces récepteurs pourraient aider à améliorer le pronostic cardiovasculaire en réduisant l’inflammation et en améliorant le profil métabolique global.
Cette hypothèse a été examinée par l’étude randomisée CRES-CENDO (Comprehensive Rimonabant Evaluation Study of Cardiovascular Endpoints and Outcomes), publiée en 2010(27), comparant le rimonabant, un antagoniste de RCB1, au placebo chez plus de 18 000 participants à haut risque cardiovasculaire (le rimonabant est un inhibiteur sélectif des récepteurs cannabinoïdes 1 qui a démontré des effets bénéfiques et significatifs sur le poids, le périmètre abdominal et les anomalies biologiques retrouvées dans le syndrome métabolique). Malheureusement, l’étude prévue sur 33 mois a été interrompue prématurément (à 1 an), sans différences significatives sur le critère des MACE, en raison de l’augmentation des effets neuropsychiatriques graves dans le groupe rimonabant (risque accru de suicide).
Deux ans auparavant, l’étude STRADIVARIUS(28) avait randomisé 800 sujets et évalué l’effet du rimonabant sur l'athérosclérose coronarienne (étude par ultrasons endocoronaires) chez les patients porteurs d'un syndrome métabolique. Au terme de l’étude, il n’avait pas eu de différence dans la survenue d’événements cardiovasculaire mais beaucoup plus d’effets secondaires délétères psychiatriques sous rimonabant ; l'effet sur l'athérosclérose apparaissait modeste, négatif sur le critère primaire (PAV = % de volume athéromateux) et positif sur le secondaire (TAV = moyenne de la surface d'athérome par coupe). L’attention nouvelle prêtée aux effets de la marijuana sur les récepteurs CB2 a conduit à quelques études ciblées au cours des dernières années. Le RCB2 est exprimé dans les tissus immunitaires et les cellules hématopoïétiques. Ces récepteurs sont régulés en réponse à l’inflammation et aux lésions tissulaires, pour une finalité anti-inflammatoire(29). Des études sur les cellules endothéliales de l’artère coronaire humaine ont montré que les agonistes RCB2 atténuent les processus pro- inflammatoires déclenchés par l’activation RCB1(30). L’utilisation d’un agoniste RCB2 a réduit l’accumulation oxydée de LDL dans les macrophages avec d’autres marqueurs inflammatoires impliqués dans l’athérosclérose, suggérant que l’activation de RCB2 atténue l’athérosclérose. Ainsi, il y aurait un intérêt significatif à développer un agoniste sélectif de RCB2 pour le traitement de l’athérosclérose(31).
À ce stade, Il n'existe donc pas d'étude convaincante prouvant l'action à long terme de prévention des événements cardiovasculaires de cette famille de médicaments, les antagonistes des récepteurs CB1 et agonistes des CB2, ni a contrario d’arguments scientifiques pour incriminer le THC des phyto-cannabinoïdes dans le développement de l’athérome coronaire.
Revue de la littérature des cas d'IDM rapportés au cannabis
Une revue systématique de la littérature en langue anglaise sur la période 2000-2018 a été publiée en 2020(32) faisant état à ce jour de 62 cas d’IDM induits par cannabis. Il s’agissait essentiellement d’hommes (94 %), âgés de 27 ans (± 10) en moyenne, dont les symptômes avaient débuté pour 80 % d’entre eux dans les 5 heures après la dernière prise de cannabis ; 75 % de ces patients n’avaient aucun des facteurs de risque vasculaire classiques de maladie coronaire. Le SCA correspondait pour 71 % des cas à un STEMI, alors que deux tiers des sujets ont été revascularisés, essentiellement par angioplastie, devant un aspect fréquent à la coronarographie d’une charge thrombotique importante en regard de l’occlusion artérielle proximale qui concernait l’IVA dans la moitié des cas. La non-revascularisation pour l’autre tiers des sujets était liée à l’absence de lésion obstructive retrouvée au moment de l’opacification coronaire, le STEMI étant alors considéré comme secondaire à un spasme épicardique ou une dysfonction de la microcirculation transitoire sur des coronaires normales par ailleurs ; 22 % des victimes d’IDM ont présenté un tableau initial d’arrêt cardiorespiratoire avec une mortalité de 50 % dans ce sous-groupe.
La majorité d’entre eux (69 %) étaient des fumeurs réguliers de cannabis et 31 % des fumeurs occasionnels, voire des primo-consommateurs (IDM après la première et unique prise de cannabis) et fumaient également du tabac (69 %). Quelques cas d’IDM étaient secondaires à la prise de cannabis comestible et/ou à celle de cannabis de synthèse.
Une étude des cas déclarés entre 2006 et 2010 au système national d’addictovigilance en France décrivait 20 cas d’usagers de cannabis ayant développé un SCA, représentant 1,8 % des déclarations d’événements indésirables en rapport avec le cannabis. La majorité d’entre eux étaient des hommes, âgés en moyenne de 34 ans, et huit ont été traités par angioplastie. Neuf complications cardiaques ont conduit au décès(33). Par rapport au nombre d’usagers réguliers de cannabis en France (1,2 million en 2010), ces 20 cas semblent très peu nombreux, mais il existe une importante sous-déclaration dans les réseaux de pharmacovigilance (95 % des cas ne seraient pas rapportés)(33).
Études épidémiologiques sur l'association entre cannabis et IDM
À partir de cette analyse de la littérature faisant du cannabis un marqueur de risque d’IDM, quelques études d’épidémiologie étiologique se sont attachées à établir un lien causal, visant à établir la responsabilité du cannabis comme réel facteur de risque d’IDM.
L’étude observationnelle publiée par M.A. Mittleman et al. en 2001(34) a été la première et demeure la référence en la matière : il s’agit d’une étude fondée sur la méthode cas-croisés, basée sur le modèle cas-témoin où chacun est son propre témoin et dont le principe est de comparer l’exposition d’un sujet à un facteur dans un délai proche de la survenue de la maladie (période cas) à l’exposition de ce même sujet au cours d’une (ou plusieurs) période(s) à distance de la maladie (période(s) témoin(s). L’étude a porté sur 3 882 cas d’infarctus du myocarde issus de 64 hôpitaux américains entre 1989 et 1996. Ces patients ont été interrogés sur leur consommation d’herbe de cannabis et sur d’autres potentiels facteurs déclenchants d’infarctus. Cent vingt-quatre personnes rapportaient avoir fumé de l’herbe de cannabis dans l’année précédant l’infarctus dont 37 personnes dans les 24 h et 9 dans l’heure. Elles déclaraient consommer au moins une fois par mois et au moins une fois par semaine pour respectivement 68 % et 41 % d’entre elles. Une heure après avoir fumé de l’herbe de cannabis, le risque estimé de déclencher un infarctus du myocarde était multiplié par 4,8, tandis qu’il diminuait rapidement et devenait non significatif au-delà de la première heure. Malgré un faible niveau de preuve (peu de cas), cette étude épidémiologique a été la première à faire du cannabis un facteur potentiel de déclenchement d’infarctus du myocarde.
Dans une base de données multicentriques de plus de 10 millions de patients aux États-Unis, A.T. Chami et C. Kim(35) ont montré que l’incidence à 5 ans de l’IDM était nettement plus élevée chez les consommateurs de cannabis, comparés au groupe témoin (210 000 / 11 millions) avec un risque relatif global (RR) de 1,44. Ce résultat a été constaté même lorsque les ana-yses ont été ajustées en fonction de l’âge, de l’hypertension, du tabagisme, du diabète, de la consommation d’alcool et de de cocaïne. Le risque relatif le plus élevé (4,4) a été observé chez les jeunes adultes âgés de 25 à 34 ans. R. Desai et al.(36) ont montré des résultats similaires en évaluant entre 2010 et 2014 la base de données nationale d’hospitalisation (SNI) d’IDM (plus de 2 millions de patients, avec 37 000 patients fumant de la marijuana). L’analyse multivariée a montré que la consommation de marijuana était un facteur de risque significatif pour le développement d’IDM une fois ajustée pour l’âge, le sexe, la race (Odds Ratio 1,079). M. Afshar et al.(37) ont examiné tous les patients âgés de moins de 55 ans qui ont été admis dans un hôpital de New York entre 2012 et 2014 (15 000) et chez qui une analyse toxicologique urinaire avait été faite : chez ceux avec un diagnostic primaire de SCA (254), ils n’ont trouvé aucune différence dans l’incidence d’IDM entre les utilisateurs de mari- juana (59) et les non-utilisateurs (195). Cependant, quand ils ont stratifié des groupes selon l’âge, ils ont constaté chez les utilisateurs âgés 18-36 ans, un risque sensiblement accru pour le SCA comparé aux non-utilisateurs, avec un OR > 5.
Une métaanalyse publiée en 2011 par T.S. Nawrot et al.(38) enquêtant sur les facteurs déclenchants de l’IDM (consommation de cocaïne, repas lourd, marijuana, émotions négatives, effort physique, émotions positives, colère, activité sexuelle, exposition au trafic, infections respiratoires, consommation de café, pollution atmosphérique) a révélé que l’usage du cannabis était la troisième variable associée la plus élevée, avec un OR de 4,8. En tenant compte des divers OR et des prévalences des diverses expositions, la part des infarctus dont il pourrait être responsable est évaluée dans ce travail à 0,8 %.
Le lien de causalité entre les complications cardiovasculaires et l’usage de cannabis n’est pas démontré à ce jour, bien que la relation temporelle entre leur survenue et l’exposition au cannabis suggère une relation causale. Un certain nombre de biais existe et limite la portée des études réalisées sur le sujet. Si l’effet des cannabinoïdes sur le système cardiovasculaire est connu depuis longtemps (THC essentiellement), d’autres substances peuvent constituer des facteurs de confusion ou aggravants, en premier lieu le tabac, ainsi que potentiellement les produits de combustion du cannabis fumé. En effet, les effets biologiques de celui-ci sont complexes, impliquant à la fois le THC et d’autres cannabinoïdes mais aussi les produits de combustion et les produits de coupe qui pourraient également être concernés. Une association statistique valide entre un facteur d’exposition et une maladie ne permet pas en soi de garantir l’existence d’un lien de causalité entre ce facteur et cette maladie et seule l’expérimentation pourrait permettre de façon formelle d’établir la causalité entre un marqueur de risque et une maladie(39). De nombreux schémas d’études sont théoriquement envisageables pour rechercher la cause d’une maladie, mais seule une étude dans laquelle l’exposition à un facteur potentiellement causal serait tirée au sort permettrait d’établir un lien de causalité entre le facteur et la maladie observée, ce qui dans le cadre du cannabis paraît difficile à réaliser et éthiquement discutable. Les études étiologiques étant principalement des études observationnelles de cohortes exposés/non exposés ou cas/témoins, ne permettant pas l’attribution d’un fort niveau de preuve, il faudrait disposer d’un faisceau d’arguments avant de conclure à une probable causalité. Une liste de ces arguments a été établie par A. Bradford Hill dès 1965(40) et constitue encore la référence dans le domaine.
Quid du cannabis "médical" ?
L’utilisation du cannabis à des fins thérapeutiques n’est pas neuve. Le chanvre est l’une des premières plantes domestiquées par l’homme, dont l’usage est attesté dans le Shennong bencao jing, grande encyclopédie des herbes aromatiques du mythique empereur chinois Shennong (datée communément de 2700 ou 2800 avant notre ère), pour la prise en charge des douleurs rhumatismales, de la constipation, de la malaria et des troubles gynécologiques. En Inde, son usage médicinal (et religieux) remonte au Ier siècle avant notre ère, comme analgésique, anticonvulsif, tranquillisant, anesthésique, antibiotique, anti-inflammatoire, antispasmodique, digestif, diurétique, stimulant pour l’appétit et même aphrodisiaque.
Le cannabis médical, légal dans deux tiers des états américains (pour autant non reconnu par la loi fédérale), autorisé en Europe dans plus de 20 pays, est conçu à partir de dosages précis entre les deux molécules principales de la plante : le THC dont le taux doit être strictement inférieur à 0,20 % et le CBD. La concentration du CBD dans la plante Cannabis sativa représente 0,1 à 2,9 % de la matière sèche. La molécule est particulièrement présente dans les graines de cannabis, en outre pauvres en THC (surtout présent dans les fleurs). Cela permet de tirer, à partir de ces mêmes graines mais aussi des fibres et des tiges, de l’huile de CBD commercialisée dans de nombreux pays, dont la France. Une grande partie des renseignements pharmacodynamiques sur le cannabis renvoie aux effets du principal constituant, le Δ9-THC, qui a un effet agoniste partiel sur les deux récepteurs CB, agit aussi au niveau des récepteurs non CB et d’autres cibles, et est responsable des effets psychoactifs du cannabis, ainsi que des effets sur le système cardiovasculaire par l’entremise de ses actions sur le récepteur CB1. Le CBD n’a pas d’effet psychoactif décelable, et ne semble pas se lier aux récepteurs CB1 ou CB2 à des concentrations physiologiques.
Il existe aussi une quantité importante de données suggérant que le CBD touche aussi à l’activité de bon nombre d’autres cibles, y compris les canaux ioniques, les récepteurs et les enzymes. Les effets du CBD sur ces cibles et sur d'autres cibles moléculaires sont associés à des effets anti-inflammatoires, analgésiques, antiémétiques, anti-psychotiques, anti-ischémiques, anxiolytiques et antiépilepti-formes. Une grande partie de ce que l’on sait sur les propriétés bénéfiques de ces cannabinoïdes non psychotropiques provient d’études in vitro et in vivo et il existe peu d’études cliniques rigoureuses et bien menées sur ces substances. Toutefois, les résultats issus de ces études pré-cliniques laissent entrevoir de potentielles indications thérapeutiques telles que la psychose, l’épilepsie, l’anxiété, les troubles du sommeil, la neurodégénération, l’ischémie cérébrale et myocardique, l’inflammation, la douleur et les réactions immunitaires, les vomissements, la prise d’aliments, le diabète de type 1, la maladie hépatique, l’ostéogenèse et le cancer. Cependant, une analyse systématique et une métaanalyse plus récentes d'essais cliniques à répartition aléatoire portant sur des cannabinoïdes (cannabis fumé, nabiximols, nabilone, dronabinol, CBD, THC, lévonontradol, acide ajulémique), révèlent que la plupart des essais montrent un soulagement des symptômes associés à l'utilisation de cannabinoïdes, mais aucune association statistiquement significative n’émerge de l’ensemble des essais(41). À ce jour, aucun des effets cardiovasculaires délétères potentiels liés au THC du cannabis « récréatif » n’a été rapporté au CBD ou au cannabis « thérapeutique ».
L’usage du cannabis à visée médicale est jugé pertinent par l’ANSM pour les patients dans certaines situations cliniques et en cas de soulagement insuffisant ou d’une mauvaise tolérance des thérapeutiques accessibles, qu’elles soient ou non médicamenteuses.
Les situations thérapeutiques pour lesquelles un usage de cannabis à des fins médicales est pertinent sont les suivantes : dans les douleurs réfractaires aux thérapies médicamenteuses ou non, dans certaines formes d’épilepsie sévère et pharmacorésistante, dans le cadre des soins de support en oncologie, dans les situations palliatives, dans la spasticité douloureuse de la sclérose en plaques.
Afin de tester dans des conditions réelles ce nouvel usage, l’ANSM a décidé de mettre en place une expérimentation permettant d’évaluer la faisabilité du circuit de mise à disposition du cannabis pour les patients. À noter que, considérant les risques pour la santé, l’ANSM a exclu la voie d’administration fumée pour le cannabis à visée médicale. L'expérimentation de cannabis thérapeutique en France va débuter sur FOCUS au moins 3 000 patients courant 2021 au plus tard. Les futurs produits seront délivrés sous forme de gélules, de fleurs séchées à vaporiser ou d'huiles contenant du cannabis médical et prescrits uniquement « en cas de soulagement insuffisant ou d'une mauvaise tolérance » avec les traitements déjà existants, précise le décret. Les 33 États américains ayant légalisé l’usage « thérapeutique » du cannabis, selon des règles très variables, ont en commun d’autoriser l’usage médical a minima pour des patients atteints de cancer, du Sida ou de la sclérose enplaques. En 2020, on compte une cinquantaine d’indications thérapeutiques différentes pour le cannabis à travers les États-Unis.
Conclusion
▹ Si les cas d’infarctus en relation avec le cannabis récréatif sont de plus en plus décrits dans la littérature, le nombre rapporté reste très faible comparé au nombre de consommateurs (quelques centaines dans la littérature internationale face à plus d’1 million de consommateurs réguliers en France et de près de 200 millions dans le monde), et en termes de mortalité directe, il est prématuré de comparer les risques du cannabis, qui font encore l’objet de discussions scientifiques, à ceux de l’alcool ou du tabac, depuis longtemps établis et d’ampleur épidémiologique majeure. Cependant, il existe probablement une sous-estimation des effets indésirables, par méconnaissance des professionnels de santé (qui de ce fait ne rechercheraient pas systématiquement la consommation de cannabis dans ce contexte) et/ou sous déclaration aux réseaux d’addictovigilance. Les mécanismes impliqués dans la survenue des IDM restent hypothétiques, associant dysfonctionnement du système nerveux autonome, altération de la fonction plaquettaire, induction d’un vasospasme et effets toxiques directs des constituants de la fumée et des produits adultérins. Il est toutefois probable que la véritable pathogenèse soit multifactorielle.
▹ La relation causale entre la consommation de cannabis et la survenue d’IDM reste sujette à débat. Mais parce qu’il s’agit de complications graves, touchant très majoritairement des hommes jeunes, voire très jeunes, pouvant entraîner le décès et que l’existence d’une relation temporelle entre leur survenue et la prise de cannabis suggère fortement un lien de causalité, il serait prudent, malgré les limites des études mentionnées, d’informer les professionnels et les usagers sur l’existence possible de ce type de complication, notamment lors d’un usage chronique et en quantité importante, ce d’autant que l’on fait face à l’augmentation du nombre de consommateurs et aussi à la teneur en THC des produits consommés. Il serait également souhaitable dans les cas d’infarctus du myocarde ou de mort subite du sujet jeune, de rechercher systématiquement une consommation de drogues, en particulier la cocaïne et le cannabis et leur association à l’alcool et au tabac.
▹ Ces résultats offrent également des pistes pour la prévention. En effet, face à une population de consommateurs qui considèrent que le cannabis est sans danger et qui sont peu sensibles aux risques sanitaires à long terme, une information reflétant les connaissances actuelles sur les possibles complications cardiovasculaires (et neurovasculaires) à court terme de la consommation de cannabis serait sans doute plus efficace.
Références sur demande à biblio@axis-sante.com
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


