Focus
Publié le 18 déc 2024Lecture 11 min
Stimulateur double chambre sans sondes : ça arrive
Les premiers stimulateurs ventriculaires sans sonde ont été implantés en 2012-2013, il y a une douzaine d’années. À l’époque, deux systèmes ont été introduits simultanément : le Micra™ de Medtronic et le Nanostim™ d’Abbott. La principale différence entre ces deux dispositifs résidait dans leur système de fixation : passif avec des ancres pour le Micra™, et actif avec une vis pour le Nanostim™. Cependant, en raison de dysfonctionnements majeurs du Nanostim™ (usure prématurée de la batterie et rupture du bouton proximal), seul le Micra™ a finalement été commercialisé. Son profil de sécurité a démontré une réduction des complications de 30 à 50 % par rapport à la stimulation conventionnelle, ce qui représente un progrès considérable, notamment pour la population âgée nécessitant une stimulation cardiaque définitive.
Le succès du Micra™ a été retentissant, avec plus de 150 000 dispositifs implantés dans le monde. Dans notre centre, la stimulation sans sonde VVI a progressivement remplacé la stimulation conventionnelle VVI, représentant aujourd’hui environ 30 % des implantations de stimulateurs cardiaques (avec plus de 170 stimulateurs sans sonde implantés en 2023).
Malgré ses avantages significatifs en termes de réduction de la morbimortalité, la stimulation sans sonde ne peut pas encore totalement remplacer la stimulation conventionnelle. Certaines limitations et questions subsistent, notamment concernant leur durée de vie et leur remplacement en fin de vie : faut-il implanter un nouveau stimulateur en « série » ou retirer l’ancien ? Cette discussion reste ouverte, bien que les pannes du Nanostim™ aient montré que ces dispositifs pouvaient être retirés sans complication jusqu’à 7 ans après leur implantation.
Un autre frein au développement est l’existence, jusqu’à aujourd’hui, de stimulateurs sans sonde uniquement ventriculaires, avec les limites du Micra AV™. Ces stimulateurs sont donc principalement réservés aux patients âgés, pour lesquels une stimulation VVI est souvent suffisante, ou dans des cas spécifiques chez des patients plus jeunes, pour préserver le capital veineux, notamment dans des situations comme le bloc atrioventriculaire congénital nécessitant des implantations répétées, des risques pour les sondes et pour le capital veineux.
C’est pourquoi l’arrivée, à l’automne 2024, du stimulateur Aveir DR sur les marchés européen et français est accueillie avec beaucoup d’enthousiasme. Il s’agit du premier système de stimulation sans sonde double chambre, permettant une stimulation synchrone de l’oreillette et du ventricule. Ce dispositif utilise le stimulateur ventriculaire Aveir™ VR, ainsi qu’un nouveau stimulateur atrial à fixation active, l’Aveir™ AR. Ces deux systèmes communiquent grâce à une technologie innovante, le système de communication implant à implant (i2i), utilisant des signaux électriques de faible énergie conduits à travers le sang et le tissu myocardique. Cela permet une communication sans connexion physique entre les deux dispositifs.
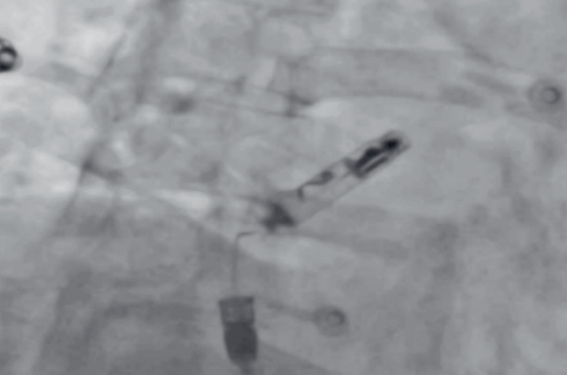
Le bon fonctionnement du système dépend d’un alignement adéquat des deux dispositifs, avec entre eux une distance maximale théorique de 7 cm (figure 1). Le stimulateur atrial est généralement implanté à la base de l’auricule droit, tandis que le stimulateur ventriculaire doit être orienté de manière à ce que son bouton proximal soit dirigé vers le haut, en direction de l’implant atrial. Idéalement, les deux dispositifs doivent être positionnés parallèlement pour maximiser l’efficacité de la communication i2i, contrairement à un positionnement perpendiculaire.
Figure 1. Le premier Avier DR implanté en France en mars 2022.
Validation de l’efficacité et de la sécurité
L’étude de validation de l’efficacité et de la sécurité de cet appareil a été publiée en 2024 dans le New England Journal of Medicine, étude à laquelle nous avons participé. Au total, 300 patients ont été recrutés, dont 190 (63,3 %) implantés pour une dysfonction sinusale et 100 (33,3 %) pour un bloc atrioventriculaire comme indication principale de stimulation.
La procédure d’implantation a été un succès dans 98,3 % des cas, avec 90,3 % des patients ne présentant aucune complication majeure. Les critères d’efficacité, notamment en ce qui concerne les seuils de capture et de détection, ont été atteints chez 90,2 % des patients. Une synchronisation atrioventriculaire d’au moins 70 % a été obtenue chez 97,3 % des patients. Le taux de complications dans les 90 jours suivant l’implantation a été de seulement 9,7 %. Un déplacement du stimulateur a été observé dans 6 cas, principalement dû à une fixation inadéquate, dont cinq concernaient le dispositif atrial, avec deux migrations distales. Après la procédure, cinq autres déplacements du stimulateur atrial ont été constatés, dont quatre avec migration distale. Quatre décès ont été signalés au cours du suivi, mais aucun n’a été jugé lié à la procédure. Le positionnement d’un stimulateur sans sonde à fixation active dans l’oreillette droite s’est avéré complexe, en raison des caractéristiques anatomiques de cette cavité, telles que la finesse de la paroi myocardique, sa petite taille et une géométrie plus complexe. Ces éléments augmentent le risque de perforation et de migration par rapport aux stimulateurs conventionnels et à d’autres systèmes sans sonde. Toute fois, dans cette étude, le risque de perforation s’est révélé plus faible que prévu (0,7 % des patients), comparativement à 1,5 % pour la première série de stimulateurs Aveir VR.
Ces résultats ont conduit à l’approbation par la FDA du stimulateur Aveir DR en 2023, suivie de son marquage CE à l’été 2024, permettant ainsi son implantation en France, en attendant le remboursement de la capsule atriale, prévu probablement pour 2025.
L’évaluation de l’efficacité « en conditions réelles » de la communication i2i, le risque de perforation, notamment atriale, ainsi que la stabilité de ce dispositif nécessiteront des registres complémentaires, notamment avec l’étude France Leadless, qui se poursuivra avec le système double chambre. Il sera également important de déterminer, dans des cohortes plus larges, si la complexité accrue de la procédure, liée à l’orientation spécifique du dispositif ventriculaire pour une synchronisation optimale, constitue un facteur déterminant.
Particularités de la « capsule » atriale
Le système se compose d’un stimulateur atrial (aLP) et d’un stimulateur ventriculaire (vLP), ainsi que d’une gaine introductrice, d’un outil de chargement, d’un cathéter de délivrance et d’un cathéter de récupération pour permettre l’extraction du dispositif si nécessaire (tableau). L’ajout du nouveau stimulateur atrial (aLP) distingue le système Aveir DR double chambre de l’Aveir VR simple chambre.
L’hélice interne de l’aLP améliore à la fois la continuité électrique et la fixation dans l’oreillette droite (figure 2). La longueur du dispositif atrial a été réduite à 32,2 mm (contre 38 pour le vLP), afin de mieux s’adapter à l’anatomie plus restreinte de l’oreillette droite et de l’auricule. En outre, le système est modulaire : l’un ou l’autre des stimulateurs sans sonde peut être implanté de manière autonome pour une stimulation AAI(R) ou VVI(R), avec la possibilité d’ajouter le second stimulateur sans sonde ultérieurement afin de passer à une stimulation double chambre. Bien que théoriquement, les deux stimulateurs puissent être implantés dans n’importe quel ordre, il est recommandé, lors d’une implantation simultanée des deux dispositifs, de poser le vLP avant l’aLP.
Figure 2. Différences entre les vis de fixation des stimulateurs sans sonde atrial et ventriculaire.
Les stimulateurs vLP et aLP sont équipés d’un asservissement basé sur une thermistance, capable de détecter les variations de la température veineuse centrale au début d’un effort physique. Cela permet d’accélérer le rythme du stimulateur en réponse à l’effort. De plus, la courbe d’accélération peut être optimisée automatiquement en fonction des besoins de chaque patient.
Le « renouveau potentiel » de la stimulation AAI
Le concept de stimulation sans sonde double chambre modulable, avec la possibilité d’implanter indépendamment un stimulateur dans l’oreillette droite ou le ventricule droit, marque une véritable évolution dans la gestion de la stimulation double chambre. Contrairement aux implantations conventionnelles de stimulateurs avec sondes, où l’on privilégiait souvent un stimulateur double chambre même pour les dysfonctions sinusales pures, afin d’éviter une réintervention complexe pour « upgrading », le système sans sonde introduit un nouveau paradigme.
D’une part, la communication i2i (implant-to-implant) consomme de l’énergie, ce qui réduit la durée de vie de la batterie. D’autre part, le stimulateur atrial sans sonde, plus compact, dispose d’une batterie de plus petite taille, ce qui affecte également sa longévité, la rendant inférieure à celle du stimulateur ventriculaire sans sonde. Ces facteurs tendent à proposer l’implantation d’un stimulateur atrial sans sonde simple aux patients présentant une dysfonction sinusale pure pour stimuler en AAI (R).
De plus, l’ajout d’un stimulateur sans sonde complémentaire (atrial ou ventriculaire) n’implique qu’une ponction fémorale supplémentaire, ce qui entraîne une morbidité extrêmement faible.
En cas de dysfonction sinusale ou de maladie de l’oreillette, nous implanterons probablement uniquement un dispositif atrial. À l’inverse, en présence d’un trouble de conduction atrioventriculaire paroxystique avec taux de stimulation évalué comme faible, un stimulateur ventriculaire sera implanté en première intention. La possibilité de passer à une stimulation double chambre ultérieurement, en ajoutant un stimulateur sans sonde atrial ou ventriculaire, se fera de manière simple et peu invasive.
Cela représente un véritable renouveau dans la pratique de la stimulation AAI (R), avec une flexibilité accrue et une réduction des contraintes liées aux réinterventions.
Où l’implanter dans l’oreillette droite ?
Le site préféré d’implantation est la base/ostium de l’auricule droit, parce que cette zone est plus épaisse (4,2 ± 1,4 mm) que la paroi latérale de l’oreillette droite (2,6 ± 0,9 mm) et que la partie médiane et distale de l’auricule (antérolatéral 1 ± 0,5 mm, latéral 0,8 ± 0,4 mm, postérieur 0,9 ± 0,6 mm).
L’implantation à la base postérieure de l’auricule minimise la distance et l’angle entre les deux stimulateurs, et l’implantation est plus directe, minimisant la courbure du cathéter de délivrance et l’alignement du stimulateur sans sonde atrial (figures 3 à 5).
Figure 3. Positionnement de l’aLP au niveau de la base postérieure de l’auricule droit et vissage (un tour et demi).
Figure 4. Passage en « tether » mode et vérification de la stabilité.
Figure 5. Libération du stimulateur atrial aLP et angle avec le vLP selon recommandation.
Si les constantes électriques sont inacceptables, la paroi latérale haute de l’oreillette droite peut être une alternative et, en 3e intention, l’auricule droit plus profond. Il faut quand même éviter les positions moyennes ou profondes de l’auricule, car la paroi y est très fine avec un risque de perforation et déplacement. L’utilisation d’incidences OAD 30°, OAG 30° et face en fluoroscopie sont très utiles pour finaliser le placement.
Particularités de la communication implant à implant
Pour assurer une stimulation atrioventriculaire (AV) continue, les stimulateurs Aveir utilisent une communication bidirectionnelle i2i, reliant le stimulateur ventriculaire (vLP) au stimulateur atrial (aLP) et vice-versa, à chaque battement cardiaque. L’importance de chaque direction de communication (du vLP vers l’aLP, dite V2A, et de l’aLP vers le vLP, dite A2V) pour maintenir le synchronisme AV dépend de l’indication clinique de la stimulation.
Les performances de la communication i2i sont évaluées en fonction du pourcentage de transmissions réussies (le débit) et de l’amplitude du signal i2i reçu (la force du signal). Ces performances dépendent fortement de la distance et de l’orientation entre les deux stimulateurs, et elles sont optimales lorsque ceux-ci sont implantés à proximité l’un de l’autre, c’est-à-dire lorsque la distance entre les boutons d’amarrage de l’aLP et du vLP en projection RAO 30° est inférieure à 70 mm (environ deux fois la longueur du vLP), et que les deux dispositifs sont coaxiaux, avec un angle aLP-vLP inférieur à 45° (figure 6). Ainsi, les sites d’implantation doivent être choisis pour minimiser la distance et l’angle entre l’aLP et le vLP. Le positionnement du stimulateur atrial sans sonde sur la partie latérale de la base de l’auricule droit optimise à la fois la distance et l’orientation. De la même manière, l’implantation du vLP dans la région médio-apicale du septum VD contribue à améliorer les performances de la communication i2i.
Figure 6. Système double chambre sans sonde Aveir AR et DR et communication ; positions relatives entre les deux stimulateurs sans sonde. La distance entre les deux boutons proximaux (docking buttons) est idéalement < 70 mm (approx. 2 fois la longueur des stimulateurs). L’angle aigu entre les deux stimulateurs sans sonde (angle aLP-vLP) est idéalement < 45° (aLP : stimulateur sans sonde atrial ; vLP : stimulateur sans sonde ventriculaire).
Possibilités d’extraction de l’Aveir DR
L’Aveir DR est à la fois implantable et récupérable. Comme le système VR, le système DR et donc AR inclut un cathéter de récupération (figure 7).
Figure 7. Cathéter de récupération de l’Aveir atrial et ventriculaire.
Ce dispositif consiste en un triple lasso connecté à un cathéter, dont le design est très similaire à celui du cathéter de délivrance. Ce système a déjà été testé et validé pour l’extraction du stimulateur Nanostim, en raison des pannes survenues avec ce dernier. Pour l’instant, l’extraction du stimulateur Aveir atrial n’a pas encore été testée in vivo. Cependant, on peut supposer que cette procédure ne sera pas très complexe, car le positionnement à la base de l’auricule permet une approche relativement directe pour le capturer et le dévisser. Cela devra toutefois être confirmé dans le futur.
Conclusion
Le lancement du système sans sonde Aveir DR, véritable stimulateur double chambre, représente une avancée majeure en stimulation cardiaque, marquant une nouvelle rupture technologique 12 ans après l’introduction des stimulateurs sans sonde VVI. Cette innovation élargit les indications de la stimulation sans sonde au bloc atrioventriculaire (BAV) complet, nécessitant le maintien d’un synchronisme atrioventriculaire. Elle constitue également un renouveau pour la stimulation AAI, car ces deux systèmes sont « upgradables », c’est-à-dire qu’il sera possible de les transformer en double chambre, en cas d’apparition de troubles de conduction atrioventriculaire pour le stimulateur sans sonde atrial, ou de mauvaise tolérance de la stimulation ventriculaire seule pour le stimulateur sans sonde ventriculaire. De plus, la communication i2i entre les deux prothèses s’est avérée très efficace, assurant un synchronisme optimal.
Cependant, toutes les questions ne sont pas encore résolues. Lorsqu’un patient est implanté avec un stimulateur sans sonde double chambre, les deux dispositifs auront probablement des longévités différentes, ce qui signifie que leur remplacement ne sera pas synchrone. Cela pourrait compliquer la gestion de la fin de vie de ces dispositifs. En outre, la fiabilité et la sécurité de l’extraction du stimulateur atrial reste à évaluer à travers des registres exhaustifs.
Enfin, à l’ère de la stimulation physiologique et notamment de la stimulation de l’aire de la branche gauche en stimulation conventionnelle, il faudra trouver la place de la stimulation sans sonde double chambre, quitte à sans doute développer le concept de stimulation de l’aire de la branche gauche avec un stimulateur sans sonde. Les années qui viennent vont être passionnantes en stimulation cardiaque.
Pour en savoir plus
• Knops RE et al. A Dual-chamber leadless pacemaker. N Engl J Med 2023 ; 388 :2360-70.
• Banker RS et al. Retrieval of chronically implanted dual-chamber leadless pacemakers in an ovine model. Circ Arrhythm Electrophysiol 2023 ;16 : e012232.
• Ip JE. Advanced helix-fixation leadless cardiac pacemaker implantation techniques to improve success and reduce complications. J Cardiovasc Electrophysiol 2023 ; 34 ; 1268-76.
• Laczay B et al. Leadless cardiac ventricular pacing using helix fixation: Step-by-step guide to implantation. J Cardiovasc Electrophysiol 2023 ; 34 :748-59.
• Cantillon DJ et al. Wireless communication between paired leadless pacemakers for dual-chamber synchrony. Circ Arrhythm Electrophysiol 2022 ; 15 : e010909.
• Reddy VY et al. Dual-chamber leadless pacing: Atrioventricular synchrony in preclinical models of normal or blocked atrioventricular conduction. Heart Rhythm 2023 ; 20 : 1146-55.
• Kaptein YE, Mortada ME. Implant-to-implant diagnostics and programming of dual-chamber leadless pacemaker in an orthotopic heart transplant recipient. HeartRhythm Case Rep 2023 ; 9(11) : 811-4.
• Roelke M, Bernstein AD, Parsonnet V. Serial lead impedance measurements confirm fixation of helical screw electrodes during pacemaker implantation. Pacing Clin Electrophysiol 2000 ; 23 : 488-92.
• Rashtian M et al. Preclinical safety and electrical performance of novel atrial leadless pacemaker with dual-helix fixation. Heart Rhythm 2022 ; 19(5) : 776-81.
• O’Connor M et al. Anatomic, histologic, and mechanical features of the right atrium: implications for leadless atrial pacemaker implantation. EP Europace 202 3; 25 : euad235.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


