Trucs et Astuces
Publié le 06 déc 2024Lecture 9 min
Angioplastie carotidienne
Nicolas VALERIO, service chirurgie vasculaire et endovasculaire, hôpital Saint-Joseph, Marseille
Les recommandations récentes sur le traitement des sténoses carotidiennes tant européennes que nord-américaines ont confirmé que la chirurgie restait le traitement de référence et que l’angioplastie carotidienne pouvait s’envisager dans certaines situations comme une alternative(1,2). Cependant, elle doit être réalisée par des opérateurs formés effectuant au moins 12 procédures par an. Cet article présente notre workflow standardisé, ainsi que nos trucs et astuces aux cours des différentes étapes de la prise en charge des sténoses carotidiennes.
En France et dans beaucoup de pays, on observe une augmentation du nombre de cas par an en lien avec la publication d’études montrant des résultats équivalents entre la chirurgie et le stenting, particulièrement pour les sténoses asymptomatiques(3,4). Néanmoins pour être une alternative crédible à la chirurgie, la procédure d’angioplastie carotidienne doit être sûre, c’est-à-dire être réalisée avec un taux cumulé de morbimortalité (TCMM) au moins équivalent sinon inférieur à celui de la chirurgie, et efficace, c’est-à-dire disposer de résultats qui se maintiennent à moyen et surtout à long terme comme l’endartériectomie.
Sélection des patients
Une fois l’indication opératoire posée, le choix de la technique chirurgicale ou endovasculaire doit respecter une rigueur dans la sélection des patients. Ainsi, il faut impérativement reconnaître les critères anatomiques qui rendent plus à risque telle ou telle technique. Le tableau résume les situations à risque qui, pour chaque technique, peuvent compromettre le degré de sécurité de l’acte en augmentant le TCMM. Si l’âge constitue un facteur de risque bien identifié pour l’angioplastie carotidienne, la limite de 75 ans dans les recommandations nord-américaines et 70 ans dans les recommandations européennes ne nous semble pas être un critère indiscutable. Il est plutôt un signal pour attirer l’attention sur le degré de calcifications des vaisseaux. Nous pensons en effet qu’il faut surtout s’attacher à analyser les caractéristiques anatomiques de la crosse et des troncs supra-aortiques pour identifier les situations à risque de l’angioplastie.
Il en est de même du risque chirurgical, dit élevé, en lien avec l’état général qui figure dans les recommandations. Lorsqu’une indication chirurgicale existe, ce critère est exceptionnellement, pour ne pas dire jamais, rencontré.
Pour la chirurgie, la notion de « cou hostile » au sens large doit être recherchée par un examen clinique minutieux. En effet, les situations anatomiques qui diminuent la sécurité de l’endartériectomie, comme l’obésité associée à une bifurcation haute de la carotide, ne sont pas si rares et ont tendance à être sous-estimées. Pour le stenting, l’analyse de la crosse et de la carotide commune sont des éléments déterminants du choix de la technique. L’angioscanner est à ce titre un examen indispensable, car il permet d’analyser précisément les obstacles athérothrombotiques sur le trajet de navigation jusqu’à la lésion, qui peut également être le siège de thrombus rendant l’angioplastie moins sûre.
Choix de la voie d’abord
Il doit se porter sur la voie d’abord qui va permettre d’accéder le plus facilement à la lésion carotidienne en procurant un bon support et suffisamment de stabilité. Bien que la voie fémorale soit le plus souvent utilisée, elle peut s’avérer inefficace, voire dangereuse dans certaines situations anatomiques. Il faut donc toujours envisager les voies d’abords alternatives (brachiales, radiales ou carotidiennes) pour choisir la plus efficace et la plus sûre.
Nous pensons que l’analyse du scanner en 3D est primordiale. Le mode rendu volumique permet de bien visualiser les angles et les contraintes que le matériel, notamment le cathéter ou l’introducteur, devra supporter. L’origine des troncs supra-aortiques sur la crosse qui peut être plus ou moins verticale et les nombreuses variations anatomiques sont autant de difficultés que permet d’anticiper l’analyse 3D.
Ainsi, la présence d’angles aigus et de changement de directions multiples rendent le cathétérisme plus difficile et diminuent la stabilité.
Reconnaître ces pièges permet de les éviter comme dans la figure 1 où l’accès à la bifurcation carotidienne gauche est réalisé non pas par voie fémorale (angle aigu), mais par voie radiale droite (angle ouvert).
Figure 1. Analyse du scanner 3D et choix de la voie d’abord d’une angioplastie carotidienne gauche en fonction des angulations.
L’avantage d’une procédure en salle hybride
Pour être sûre, l’angioplastie carotidienne requiert une excellente qualité d’imagerie à toutes les étapes de la procédure. C’est pourquoi, elle nous semble aujourd’hui de moins en moins compatible avec l’utilisation d’amplificateurs de brillances mobiles sans capteurs plans.
Les salles fixes à capteurs plans offrent une bien meilleure qualité d’images. Le mode fusion d’images permet d’augmenter la précision du geste en intégrant les détails anatomiques du scanner préopératoire. Le repérage des ostia des troncs supra-aortiques, le positionnement de repères sur bifurcation carotidienne et la lésion permettent d’obtenir un masque de fusion très utile pour le bon déroulement de la procédure. La fusion permet également d’utiliser le zoom numérique, afin de minimiser l’irradiation en évitant le recours à un champ plus irradiant, en particulier lors du déploiement du stent.
Navigation et cathétérisme de la carotide commune
Durant la procédure d’angioplastie carotidienne, l’acheminement de l’introducteur de 6 ou 7 French, ou du cathéter guide de 8 French selon les habitudes, est reconnu comme une étape à risque d’embolie et donc d’accident vasculaire cérébral ischémique perprocédure. La prévention de ce risque repose pour nous sur deux points clés : l’utilisation d’une combinaison de matériel « soft » et la règle de rester à distance de la bifurcation carotidienne. Ainsi, pour acheminer l’introducteur dans la carotide commune, nous évitons autant que possible la technique qui consiste à cathétériser l’artère carotide externe avec un guide souple pour ensuite le remplacer par un guide plus rigide afin de monter l’introducteur. Nous préférons utiliser la combinaison d’un guide Stiff 260 cm (Terumo) positionné dans la carotide commune proximale avec une sonde de type VTK (Cook) de 5 French 125 cm. En exerçant une tension adaptée sur le couple guide-sonde, l’introducteur de 6 French 90 cm progressera en coulissant le long de la sonde comme un télescope sans jamais toucher la bifurcation carotidienne.
Lorsque les sinuosités entre le tronc artériel brachiocéphalique (TABC) et la carotide commune droite sont très marquées, nous dissocions les étapes du cathétérisme. Nous positionnons d’abord un guide 0.035 souple puis rigide dans l’artère humérale droite, ce qui permet à l’introducteur d’être avancé dans l’artère sous-clavière droite. Le guide rigide est ensuite remplacé par un guide 0.018 qui permet de stabiliser l’introducteur que l’on recule dans le TABC. La valve de l’introducteur est ensuite piquée en parallèle pour monter une sonde et un guide 0.035 Stiff (Terumo) pour le cathétérisme de la carotide commune. La dernière étape consiste à retirer le guide 0.018 pour faire coulisser l’introducteur dans la carotide commune sans chasser. Dans ces anatomies complexes, l’utilisation du masque de fusion facilite encore la réalisation des différentes étapes du cathétérisme (figure 2).
Figure 2. Anatomie complexe avec sinuosités : cathétérisme par étape sous guidage avec la fusion d’images. Le repérage des ostia des troncs supra-aortiques permet de se positionner avec précision dans la bonne incidence à chaque étape.
Franchissement de la lésion
Le franchissement de la lésion est rarement un problème, mais il doit être délicat et atraumatique. Il faut choisir l’incidence radiologique qui exposera le mieux la sténose et la bifurcation carotidienne. Lors du franchissement, le guide ne doit pas « gratter » la lésion ou pénétrer dans une micro-ulcération. Il est pour cela important d’utiliser un guide 0.014 qui sera préformé en fonction des caractéristiques de la lésion en lui donnant une seule courbure courte ou une double courbure si des changements de direction s’imposent.
Choix du système de protection cérébrale
Les recommandations mentionnent qu’il faut utiliser un système de protection cérébrale autant que possible, mais que la mise en place du dispositif, quel qu’il soit, ne doit pas augmenter le risque de complications. Un des inconvénients reconnus des filtres est le risque de traumatisme de l’artère carotide interne distale lorsque le guide 0,014 se tend sous la pression du cheminement du stent dans les courbures de la crosse. Cette tension et les mouvements du filtre peuvent entraîner un spasme plus ou moins sévère, voire une dissection de l’artère.
Afin d’éviter ce risque, nous préférons utiliser un filtre mobile sur guide de type Emboshield NAV (Abbott) qui a l’avantage de ne pas traumatiser l’endothélium de l’artère, puisque la tension ou les micro-mouvements du guide ne le mobilisent pas.
Nous ne partageons pas l’engouement observé outre-Atlantique pour la technique TCAR, dont nous n’avons pas l’expérience. Cependant, cette intervention comprend un abord chirurgical et la mise en place d’un dispositif filtrant qui complexifie la procédure sans offrir, à nos yeux, de bénéfices par rapport à l’angioplastie avec notre workflow standardisé.
Stenting
Nous ne réalisons pas de prédilatation systématique, sauf en cas de résistance au passage de la gaine hydrophile du filtre au contact de la lésion. Dans ce cas, une prédilatation est réalisée avec un ballon de 2 à 3 mm avant le stenting.
Les recommandations laissent libre l’opérateur dans le choix du stent, de sa taille, de son design (cellules ouvertes, fermées ou double couche), de sa forme conique ou tubulaire. Il est cependant reconnu que pour obtenir un bon résultat immédiat et éviter une resténose à distance, il faut une bonne apposition du stent, ce qui implique de ne pas avoir d’espaces morts entre le stent et la paroi tout en évitant un oversizing excessif.
Le choix du stent est donc un élément essentiel, il se fait au moment du sizing préopératoire sur le scanner. Nous analysons la lésion, son degré de calcification, la forme du bulbe carotidien et la sinuosité de l’artère carotide interne à son origine et immédiatement en aval de la lésion. Nous choisissons ainsi la longueur, le diamètre, la forme et le design du stent.
Nous pensons cependant que cette étape est perfectible car il est souvent difficile de prévoir le comportement du stent au contact de la paroi de l’artère. Nous évaluons actuellement l’intérêt de la simulation numérique et la technique du jumeau numérique de PrediSurge comme outils d’aide à la décision pour le choix des stents des gammes Acculink et Xact (Abbott). En réalisant une étude rétrospective qui comparait les scanners postangioplastie au jumeau numérique de PrediSurge, nous avons pu constater que la simulation numérique pouvait prédire avec précision l’apposition des différents stents de ces deux gammes. Elle permettait aussi de visualiser des défauts d’apposition du stent en fonction de la taille et de la forme choisie (figure 3). Enfin, elle mettait en évidence l’oversizing et les zones où la force radiale du stent était excessive. Finalement, le jumeau numérique pourrait fournir beaucoup d’informations qui ne sont pas visibles à l’artériographie perprocédure. Nous conduisons actuellement une deuxième étude qui vise à évaluer si le jumeau numérique peut aider l’opérateur à mieux choisir le stent. Nous espérons pouvoir présenter nos résultats prochainement.
Segmentation
Xact 6-8-40
Acculink 6-8-40
Acculink 7-10-40
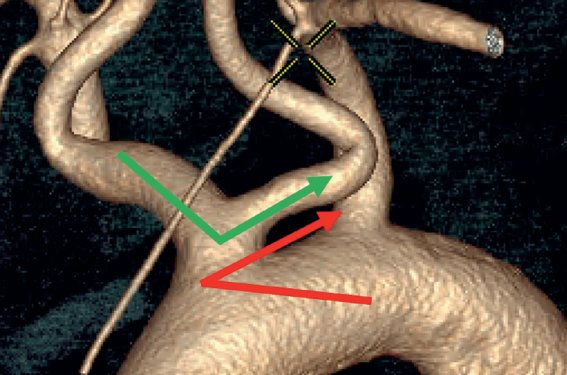
Figure 3. Prédiction par la simulation numérique du résultat anatomique en fonction des stents utilisés. Les flèches montrent les défauts d’appositions lorsque les diamètres du stent sont insuffisants ou la plicature induite par un stent dont la force radiale et la rigidité sont excessives. L’Acculink conique diamètre 7.10 longueur 40 donne pour cette sténose le résultat le plus satisfaisant.
Conclusion
L’angioplastie est aujourd’hui un outil indispensable avec la chirurgie et le traitement médical dans l’arsenal thérapeutique.
Pour être aussi sûre et efficace que la chirurgie, elle doit être réalisée avec une planification précise, un workflow standardisé dans un environnement adapté par des opérateurs formés et expérimentés. Une bonne connaissance du matériel et l’essor de nouvelles technologies comme le jumeau numérique et l’intelligence artificielle devraient encore permettre d’en améliorer les résultats.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


