Publié le 31 aoû 2015Lecture 8 min
Quand et comment évaluer la taille d'un anévrisme de l'aorte abdominale ?
A. LONG, Médecine vasculaire, Hospices Civils de Lyon, Hôpital Édouard Herriot, Lyon ; Université Claude Bernard Lyon 1
L’anévrisme de l’aorte abdominale sous-rénale (AAA) est défini par une augmentation segmentaire de calibre de l’aorte sous-rénale de plus de 50 % par rapport au diamètre attendu, avec perte de parallélisme des parois. Dans la plupart des études de dépistage, la valeur seuil pour retenir le diagnostic est un diamètre de 30 mm.
Actuellement, l’indication à opérer un AAA asymptomatique par chirurgie ouverte ou exclusion endovasculaire par endoprothèse (EVAR) est retenue chez l’homme devant un AAA de 50 mm de diamètre maximal (Dmax) (55 mm dans les recommandations anglosaxonnes), ou à croissance rapide (1 cm en 1 an)(1). Le seuil est plus bas chez la femme (45 mm en France, 50 mm dans les recommandations anglo-saxonnes) car le risque de rupture est à diamètre équivalent 4 fois plus élevé(2).
Enfin, en cas de traitement endovasculaire, l’effet attendu est la rétraction de la coque anévrismale autour de l’endoprothèse et le témoin de l’exclusion est la diminution de son Dmax.
Le Dmax est donc historiquement le paramètre clé du diagnostic d’un AAA et donc du dépistage, de sa surveillance, de la décision opératoire, puis de son suivi après endoprothèse. Les techniques d’imagerie usuelles sont l’écho-Doppler (US) et le scanner (CT).
Or l’AAA est une malade volumique (3D), caractérisée sur un plan de coupe (2D) en US ou CT par une distance (1D). Par ailleurs, le parcours de soins d’un patient l’amène à fréquenter des équipes soignantes différentes et à avoir de façon conjointe ou alternée US et CT.
Une revue récente de la littérature a montré qu’il n’existait pas de consensus dans la méthodologie pour effectuer la mesure du Dmax(3). Avec des conséquences à chaque étape pour le patient :
- diagnostic d’AAA porté par excès ou par défaut dans les campagnes de dépistage privant ainsi un patient porteur d’un AAA d’une prise en charge appropriée notamment sa surveillance, ou inversement instaurant une prise en charge lourde sans raison ;
- évaluation erronée de la croissance d’un AAA ;
- indication opératoire trop précoce exposant inutilement le patient au risque de la chirurgie ou trop tardive l’exposant au risque de rupture(4) ;
- enfin, mauvaise évaluation de la rétraction de l’AAA après traitement endovasculaire.
La mesure du Dmax résulte de 4 étapes. La première est le choix du référentiel de mesure : référentiel anatomique fondé sur les 3 axes orthogonaux X, Y et Z et le référentiel aortique fondé sur la ligne centrale de l’AAA. Ces deux référentiels diffèrent en cas d’AAA sinueux ou à développement asymétrique.
Une fois le référentiel défini, la deuxième étape est le choix du plan de coupe. Selon le référentiel choisi, les plans de coupe diffèrent. Dans le référentiel anatomique, les 3 plans sont : le plan axial (ou transverse), le plan frontal (ou coronal) et le plan sagittal (figure 1a, b, c). Dans le référentiel aortique, les plans sont alignés selon la ligne centrale de l’AAA (figure 1e) ou perpendiculaires à cette dernière.
La troisième étape est le choix de l’axe de mesure sur le plan de coupe retenu. Par exemple, dans le référentiel anatomique, sur une coupe transverse, les axes de mesure habituels permettent de mesurer le diamètre antéropostérieur, le diamètre transverse ou le diamètre maximal quelle que soit la direction. Dans le référentiel aortique, sur une coupe perpendiculaire à la ligne centrale de l’AAA, les diamètres dits antéropostérieur et transverse ne sont plus sur les vrais axes antéropostérieur et transverse si l’AAA est sinueux, ce qui pousse à privilégier la mesure du diamètre maximal quelle que soit la direction.
Enfin la dernière étape est de définir la position des curseurs par rapport à la paroi anévrismale. En CT, les curseurs sont positionnés à l’interface entre la paroi externe de l’AAA et le tissu péri-anévrismal (figure 1d). L’identification de l’interface est aisée en présence de graisse périanévrismale ou en cas de calcifications, mais peut être plus difficile si des structures de même densité collent à la paroi de l’AAA (veine cave inférieure, ganglions périaortiques, veine rénale gauche rétroaortique, anses digestives).
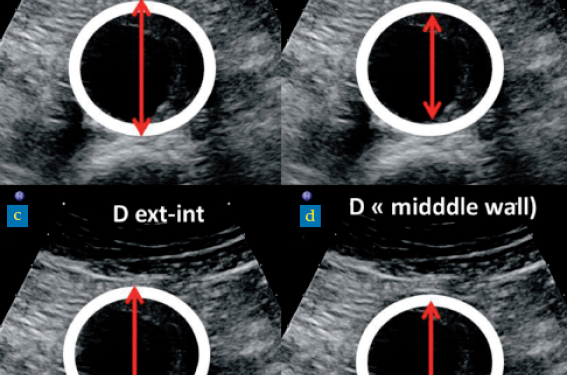
En US, 4 possibilités sont offertes, définissant 4 diamètres (figure 2) :
- diamètre externe avec les curseurs à l’interface tissu périanévrismal et versant externe de la paroi ;
- diamètre interne avec les curseurs à l’interface lumière (ou thrombus en cas de thrombus endosacculaire) et versant interne de la paroi ;
- diamètre externe-interne avec le curseur antérieur positionné à l’interface tissu-versant externe de la paroi et le curseur postérieur à l’interface lumière/thrombus et versant interne de la paroi (figure 3) ;
- diamètre « middle-wall » avec les curseurs positionnés sur la paroi elle-même.
La différence entre diamètre interne et externe est de l’ordre de 5 mm.
Figure 1. Anévrisme fusiforme de l’aorte abdominale en angioscanner, dans le référentiel anatomique. a. Coupe axiale ; b. Coupe sagittale ; c. Coupe coronale ; d. Mesure du diamètre maximal : les curseurs sont positionnés sur le versant externe des parois de l’AAA ; e. Reconstruction MPR coronale.
Figure 2. Les pointes de flèche illustrent le positionnement des curseurs ; le cercle blanc correspond à la paroi de l’AAA (dont l’épaisseur majorée pour les besoins de l’iconographie). a. Diamètre externe : curseur à l’interface tissu-versant externe de la paroi ; b. Diamètre interne : curseurs à l’interface lumière ou thrombus- versant interne de la paroi ; c. Diamètre externe-interne : curseur antérieur positionné à l’interface tissu-versant externe de la paroi et curseur postérieur à l’interface lumière ou thrombus-versant interne de la paroi ; d. Diamètre « middle-wall » : curseurs positionnés sur la paroi elle-même.
Figure 3. AAA en échographie mode B, coupe perpendiculaire à la ligne centrale. L’interface antérieure tissu-versant externe de la paroi et l’interface lumière ou thrombus-versant interne de la paroi (flèches rouges) sont aisément identifiables alors que l’interface postérieure tissuversant externe de la paroi (flèche blanche) est moins facile à identifier.
L’un des critères de choix de la meilleure méthode de mesure pourrait être la reproductibilité du diamètre.
En CT, un travail récent a montré que parmi 10 mesures usuelles possibles, la meilleure reproductibilité était obtenue avec le diamètre maximal quelle que soit la direction sur une coupe perpendiculaire à la ligne centrale de la lumière obtenue après segmentation semi-automatique des parois de l’AAA(5).
En US, la reproductibilité a été essentiellement étudiée en fonction de la position des curseurs et les résultats sont contradictoires. Pour Hartshorne(6), meilleure reproductibilité du diamètre interne comparé au diamètre externe, pour Thapar(7), meilleure reproductibilité du diamètre externe comparé au diamètre interne et plus récemment pour Gürtelschmid(8), meilleure reproductibilité du diamètre externe-interne, comparé au diamètre interne lui-même plus reproductible que le diamètre externe.
Du fait des conséquences dans la prise en charge clinique, il est donc indispensable qu’un consensus soit établi pour effectuer cette mesure.
Y a-t-il une alternative ? L’alternative repose sur une imagerie volumique de l’AAA plus représentative de la réalité anatomique et permettant d’extraire automatiquement le véritable diamètre maximal.
L’imagerie volumique a été développée en CT mais la plupart des logiciels disponibles nécessitent une injection de produit de contraste pour extraire la ligne centrale de la lumière de l’AAA. Peu de logiciels permettent cette reconstruction à partir d’un scanner non injecté. Cette imagerie a essentiellement été évaluée pour le suivi des AAA après endoprothèse. Les modifications de volume étaient plus sensibles que celle du diamètre pour le diagnostic de croissance ou de rétraction(9,10), pour conclure à l’exclusion ou dépister des complications(11).
Une nouvelle génération de sondes permet aujourd’hui une acquisition volumique en US. Il peut s’agir d’une sonde 2D à balayage mécanique, où l’acquisition est faite grâce à un balayage angulaire de l’AAA par le faisceau ultrasonore ou d’une véritable sonde 3D matricielle. Le traitement original des séquences a été développé en collaboration avec Philips Research, France.
Après acquisition, le volume acquis est transféré sur une interface dédiée permettant l’analyse multiplanaire tridimensionnelle de l’AAA, la segmentation semiautomatique des parois, l’extraction du diamètre maximum perpendiculaire à la ligne centrale (Max3D) et le calcul du volume partiel(12) (figure 4). Le choix d’un volume partiel repose sur l’impossibilité dans la majorité des cas d’acquérir dans un même volume les repères anatomiques usuels que sont l’artère rénale la plus basse et la bifurcation aortique.
Nous avons validé cette technique originale chez 42 patients porteurs d’AAA natifs (n = 21) ou après traitement par endoprothèse (n = 21). Les reproductibilités intra- et interobservateur du Max3D et du volume partiel étaient en accord avec les chiffres publiés dans la littérature. Dans ce travail le volume partiel était le volume 30 (Vol 30) défini comme le volume entre 2 plans de coupes séparés par une distance de 30 mm sur la ligne centrale. Les résultats n’étaient pas influencés par l’indice de masse corporelle, la profondeur de l’AAA et la présence de l’endoprothèse. Les valeurs des mesures de Max3D et du volume partiel n’étaient pas influencées par l’orientation de la sonde. Enfin les diamètres Max2D and Max3D étaient fortement corrélés.
Dans une large cohorte des patients porteurs d’AAA traités par endoprothèse, K. Bredahl et coll. ont montré qu’il existait une excellente corrélation entre les volumes obtenus en imagerie volumique CT et US(13) et que le Dmax obtenu en imagerie volumique CT était mieux corrélé au Dmax obtenu en imagerie volumique US qu’au Dmax mesuré en échographie 2D habituelle(14).
Figure 4. Étapes de l’analyse volumique de l’AAA après acquisition avec une sonde mécanique. Illustrations avec l’aimable autorisation de Philips Research. a. Analyse du volume acquis en US après transfert sur l’interface dédiée permettant l’étude de l’AAA selon les différents plans de l’espace (de gauche à droite et de bas en haut : coupes axiales, sagittales, coronales et représentation des différents plans) ; b. Maillage des parois de l’AAA après la segmentation semi-automatique et visualisation par transparence de la ligne centrale de l’AAA ; c. Ligne centrale avec les plans de coupe (cross-section) perpendiculaires à la ligne centrale passant par la paroi de l’AAA. En bleu, plan de coupe contenant le diamètre maximal de l’AAA ; d. Extraction automatique du Dmax ; e. Détermination du volume partiel qui est le volume de l’AAA situé entre 2 plans de coupes séparés par une distance donnée sur la ligne centrale. Ex. : Vol 30 = volume entre 2 plans de coupes séparés d’une distance de 30 mm sur la ligne centrale. Cette distance est choisie par l’examinateur.
Conclusion
À ce jour, le diamètre d’un AAA reste le paramètre utilisé en pratique clinique pour le diagnostic, le suivi et l’indication opératoire, mais il est indispensable d’établir rapidement un consensus pour en faire la mesure.
Le volume d’un AAA est un nouveau paramètre accessible en CT ET en US.
L’indication clinique la plus intéressante de l’imagerie volumique en US d’un AAA est le suivi du sac anévrismal après endoprothèse puisque qu’il a déjà été montré en CT que le devenir du volume de l’AAA était plus sensible que celui du diamètre pour déterminer la rétraction ou la reprise de la croissance de l’AAA.
La confirmation de la robustesse de la technique 3D US par des études multicentriques permettra de diminuer le recours à l’imagerie CT.
La place de l’imagerie volumique pour le suivi des petits AAA reste à évaluer.
Références sur demande à la rédaction : biblio@axis-sante.com
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :