Rythmologie et rythmo interventionnelle
Publié le 16 aoû 2016Lecture 5 min
Aldostérone et troubles rythmiques ventriculaires en période d’ischémie-reperfusion
J. ALEXANDREa,b, L. CHAMP-RIGOTa, D. LEGALLOISa, P. OLLITRAULTa,b, M. CHEQUELa,b, F. BEYGUIa, P. MILLIEZa a : Service de cardiologie, Hôpital universitaire Côte de Nacre, Caen. b : Service de pharmacologie, Hôpital universitaire Côte de Nacre, Caen.
L'aldostérone est une hormone minéralocorticoïde principalement sécrétée par les glandes corticosurrénales ayant un rôle crucial dans le maintien de la volémie et de la tension artérielle, ainsi que de la kaliémie, via son action sur le rein, la réabsorption du sodium urinaire et la sécrétion urinaire de potassium. Longtemps cantonnée à ce rôle de régulation, l’aldostérone est maintenant reconnue comme un élément physiopathologique majeur du système cardiovasculaire.
De nombreuses observations clinicoexpérimentales ont clairement établi l’impact délétère de l’aldostérone dans l’HTA et l’insuffisance cardiaque (IC)(1,2), mais aussi plus récemment au cours d’un syndrome coronarien aigu (SCA)(3,4). Ces effets comprennent, entre autres, la survenue de troubles du rythme ventriculaire.
Les canaux ioniques jouent un rôle essentiel dans la genèse des potentiels d’action (PA) et de l’influx électrique cardiaque. Au cours d’un épisode d’ischémie-reperfusion (I/R) myocardique, ces canaux subissent de profondes modifications pouvant aboutir à la formation de substrats arythmogènes et à la genèse de troubles du rythme.
Le but de cette mise au point est de détailler la littérature sur les relations entre aldostérone et troubles du rythme ventriculaire dans ce contexte, en apportant des éléments physiopathologiques sur les mécanismes supposés, notamment via son action sur les canaux ioniques.
Arythmies ventriculaires observées en cas d’I/R
Normalement, les 3 types de mécanismes habituels sont observés en cas d’I/R : automaticité anormale, activité déclenchée et réentrée. En contexte d’I/R, un déséquilibre entre courants potassiques sortants et courants sodiques et/ou calciques entrants peut survenir (au profit des seconds) et ainsi générer une dépolarisation diastolique spontanée à l’origine d’un automatisme anormal. Dans ce même contexte, il existe une forme particulière d’arythmie par réentrée appelée réentrée de phase 2. Ce type se rencontre principalement dans le syndrome de Brugada, mais aussi au cours d’une I/R ou au sein d’un même territoire myocardique : les cellules ne vont pas toutes subir le même degré d’ischémie engendrant un raccourcissement hétérogène de la durée des PA au sein de ce territoire favorisant ce type de réentrée.
Effets délétères de l’aldostérone et de l’activation de son récepteur en situation d’I/R
Les effets délétères d’une élévation des taux plasmatiques d’aldostérone ont été démontrés en clinique dans un contexte d’HTA avec hyperaldostéronisme primaire(1) ou en cas d’IC chronique(2). Plus récemment, les propriétés délétères d’une élévation d’aldostérone plasmatique en contexte d’ischémie coronarienne aiguë ont été mises en évidence(3).
Une étude a mesuré les taux d’aldostérone plasmatique chez 356 patients présentant un SCA et a mis en évidence que les patients présentant les taux les plus élevés d’aldostérone présentaient significativement plus de décès toutes causes, de décès cardiovasculaires, d’IC, de fibrillation ventriculaire et d’arrêts cardiaques ressuscités après 6 mois.
Plusieurs éléments d’explication ont été avancés sur la présence de taux plasmatiques élevés d’aldostérone lors d’un SCA :
• les changements hémodynamiques survenant au cours d’un SCA et persistant au cours de l’IC entraînent une stimulation du SRAA mais aussi une stimulation sympathique qui augmente la production d’aldostérone ;
• l’existence d’autres stimuli de production d’aldostérone comme les dyskaliémies et la survenue de nécrose myocytaire.
L’aldostérone semble donc élevée lors d’un SCA et est associée à la survenue d’événements cardiovasculaires péjoratifs ; c’est ce qui a motivé la réalisation de l’étude ALBATROSS(4). Cette étude multicentrique randomisée et ouverte a inclus 1 600 patients présentant un SCA avec ou sans sus-ST à haut risque, qui ont été randomisés entre une thérapie standard seule ou associée à 200 mg de soludactone (administrée lors de la coronarographie) suivie par 25 mg/j de spironolactone durant 6 mois. Ce travail n’a pas mis en évidence de réduction de mortalité et de survenue de troubles du rythme ventriculaire dans le groupe spironolactone dans la population globale, mais en revanche dans le sous-groupe de patients avec un sus-ST, il existait une baisse significative de la mortalité (HR = 0,20 [0,06 – 0,69] ; p = 0,0044).
Mode d’action de l’aldostérone dans un contexte d’I/R
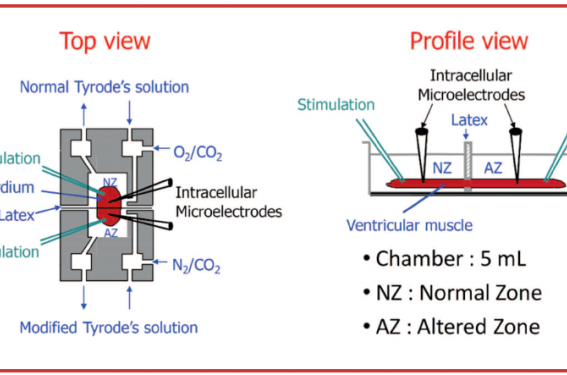
Il existe deux modes d’action de l’aldostérone : une mode rapide non génomique et un mode tardif génomique. Dans un contexte d’ischémie, le mode d’action non génomique rapide (de l’ordre de la seconde ou de la minute) de l’aldostérone semble privilégié avec l’existence de récepteurs membranaires à l’aldostérone ayant des liens directs avec les canaux ioniques membranaires et donc avec le PA(5). Dans un contexte normoxique, il a été démontré que l’aldostérone pouvait modifier l’expression et/ou l’action de canaux ioniques INa, Ito, ICaL , ICaT Ikr et IkATP à l’origine de modifications du PA. En contexte d’I/R, nous avons étudié les effets délétères de l’aldostérone sur un modèle de double cuve permettant d’analyser le PA en condition d’I/R sur un modèle de ventricule droit de lapin (figure). De plus, en utilisant la méthode de patchclamp, nous avons étudié les effets de l’aldostérone sur les différents canaux notamment potassiques et les effets du blocage de l’aldostérone par la soludactone (utilisée dans ALBATROSS).
L’ensemble de nos expérimentations a permis de mettre en évidence qu’en contexte d’I/R la perfusion d’aldostérone a induit une hyperpolarisation et un raccourcissement du PA dans la zone ischémique et une augmentation de la dispersion entre les deux zones ischémique/non ischémique ; et durant la reperfusion, l’aldostérone a augmenté l’incidence de survenue des arythmies ventriculaires spontanées(6). Ces effets délétères engendrés par l’aldostérone ont été prévenus par l’ajout d’antagonistes des canaux IKATP et IK1 (7,8) et seraient donc impliqués dans la survenue des effets délétères de l’aldostérone. L’ensemble de ces effets induits par l’aldostérone ont été prévenus par la soludactone et non par le RU 28318, suggérant que l’aldostérone exercerait ses effets délétères par une voie non génomique(9).
Figure. Modèle expérimental de double cuve (A). Protocole d’I/R sur du ventricule droit de lapin (B). Raccourcissement du PA entre zone ischémique (AZ) et non ischémique (NZ) (C). Troubles du rythme ventriculaire et bloc de conduction en phase d’I/R (D). Technique de patch-clamp sur cellule isolée (E).
Conclusion
Il existe donc un lien entre aldostérone et survenue de troubles du rythme ventriculaire lors d’un SCA, mais aussi pendant la période de reperfusion.
L’aldostérone modifie la durée des PA, la dispersion des durées de PA et majore l’incidence des arythmies spontanées via une modification des courants IKATP et IK1. L’ensemble de ces effets délétères peuvent être prévenus par la soludactone suggérant des mécanismes génomiques.
Nos résultats s’intègrent parfaitement aux données des études cliniques montrant des effets néfastes proarythmiques des taux plasmatiques élevés d’aldostérone à la phase aiguë d’un SCA. Le blocage de l’aldostérone lors d’un SCA pourrait permettre une réduction des troubles du rythme ventriculaire.
"Publié dans RythmologieS"
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :