Publié le 07 fév 2012Lecture 6 min
ASCOT-BPLA : une réponse à la notion de risque résiduel dans l’hypertension ?
E. MILLARA, Suresnes
Lorsqu’au milieu des années 2000, J. Blacher et son équipe mettent en évidence la notion de « risque résiduel » avec les résultats à 5 ans de l’étude PRIME, ils rencontrent un certain scepticisme(1). Cinq ans plus tard, le suivi à 10 ans de PRIME(2), ainsi que d’autres travaux confirment avec une puissance et une robustesse incontestables l’observation suivante : à pression artérielle comparable, les patients hypertendus traités sont davantage exposés au risque cardiovasculaire que des sujets normotendus.
Autrement dit, après ajustement sur tous les facteurs de risque y compris le mode de vie, l’alimentation, et la PA systolique (NB : l’ajustement est une méthode statistique permettant de neutraliser l’impact des facteurs associés), le contrôle des chiffres tensionnels chez l’hypertendu ne permet pas de réduire son risque cardiovasculaire au même niveau que celui d’un normotendu comparable en termes d’âge, de sexe et de cofacteurs de risque. Les hypertendus, dont la pression artérielle est normalisée par traitement antihypertenseur, conservent ainsi un risque cardiovasculaire supérieur à celui de patients normotendus. Ce léger sur-risque persistant malgré un bon contrôle tensionnel est appelé « risque résiduel ». Ainsi, dans l’étude PRIME, la mortalité totale est multipliée par 1,15 chez les patients traités par antihypertenseurs, l’incidence de maladies coronariennes par 1,46, la mortalité CV par 1,62 et les AVC par 1,75.
De même, la cohorte QRISK, ayant inclus plus d’un million de sujets, montre après ajustement sur tous les autres facteurs que le fait de recevoir un traitement antihypertenseur majore le risque CV de 73 % pour les femmes et 84 % pour les hommes(3).
Ce risque résiduel semble spécifique de l’hypertension : en effet, il n’est pas retrouvé pour les hyperlipidémies, pour lesquelles la normalisation du LDL-
cholestérol semble ramener le risque cardiovasculaire au niveau de celui d’une population normolipidémique(2).
Le risque résiduel de l’hypertendu : des explications avec ASCOT-BPLA
Les hypothèses avancées pour expliquer le risque résiduel sont multiples et possiblement associées entre elles : il est possible que le traitement antihypertenseur soit initié tardivement et/ou de façon trop timide, sur des lésions artérielles devenues en partie irréversibles. Il pourrait être en lien avec une mauvaise observance (mais son absence concernant les hypolipémiants ne va pas dans ce sens). Le risque résiduel pourrait enfin être lié au contrôle insuffisant de certaines composantes de l’HTA non intégrées par la mesure brachiale classique, particulièrement la pression centrale et la variabilité tensionnelle.
C’est ce que suggère entre autres l’étude ASCOT(4) qui concernait des patients hypertendus sans antécédents particuliers. Près de 20 000 patients ont été randomisés entre un traitement par amlodipine avec adjonction de périndopril ou par bêtabloquant avec adjonction d’un diurétique thiazidique. Cette étude a été interrompue prématurément, après un suivi moyen de 5,5 ans, en raison d’une mortalité totale très inférieure dans le groupe périndopril/amlodipine et avec une réduction de 24 % de la mortalité cardiovasculaire par comparaison au groupe bêtabloquant/diurétique.
L’exploration mécanistique de cette différence a d’abord montré qu’une PAS légèrement plus basse a été obtenue dans le groupe périndopril/amlodipine (136,1 vs 137,7 mmHg), et que le profil métabolique s’y est révélé plus favorable sur les paramètres tels que poids, HDL, triglycérides, glycémie et créatinine. Toutefois, après ajustement sur ces paramètres, il persistait une différence inexpliquée en termes de mortalité, en faveur du traitement périndopril/amlodipine.
Les études ancillaires ont permis d’en suggérer les mécanismes : d’une part, la PAS nocturne était plus basse en moyenne de 2,2 mmHg dans le groupe périndopril/amlodipine ; en revanche, la PAD était respectée, facteur d’importance, étant établi par une analyse post-hoc d’INVEST, et repris par les dernières recommandations internationales, qu’une PAD < 70 mmHg augmente l’incidence des événements cardiovasculaires majeurs.
D’autre part, la variabilité inter-visite de la PA s’est révélée moindre dans le groupe périndopril/amlodipine. La variabilité tensionnelle inter-visites de la PAS apparaît comme un meilleur prédicteur que la PAS brachiale, vis-à-vis du risque CV et rappelons que la récente méta-analyse de Rothwell(6) conclut que les ICa sont les traitements permettant le meilleur contrôle de la variabilité tensionnelle, suivis par les IEC. En revanche, les ARA2 sont les traitements les moins efficaces pour réduire cette variabilité tensionnelle.
Enfin, l’étude ASCOT CAFE montre également la supériorité IEC/ICa sur l’association bêtabloquant/diurétique, avec une PAS centrale significativement plus basse de 4,3 mmHg, alors que la pression artérielle périphérique était comparable entre les 2 groupes de patients.
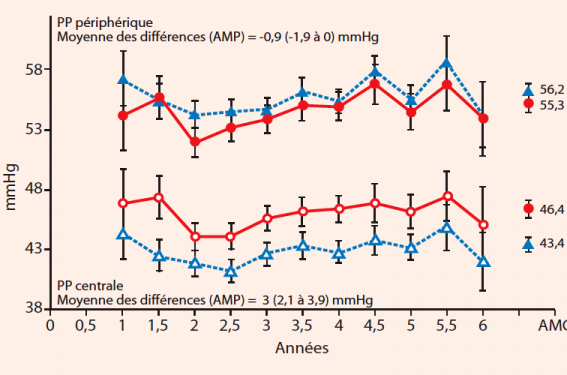
Et de fait, dans l’étude ASCOT, l’intégration de la variabilité tensionnelle inter-visites et de la pression centrale dans les paramètres d’ajustement neutralise la différence entre les deux groupes, permettant d’expliquer en partie la différence de pronostic observée (figures 1 et 2).
Figure 1. Pression artérielle brachiale (signes pleins) et aortique (signes évidés) : la pression périphérique est similaire entre traitement IEC/ICa et BB/Diur, mais la pression centrale est mieux contrôlée par l’association IEC/Ica.
Figure 2. La différence entre pression systolique périphérique et centrale est plus importante pour le traitement IEC/Ica.
Pression centrale : le reflet de la rigidité artérielle
La pression artérielle centrale (PAC) n’est pas corrélée à la pression artérielle périphérique (PAP) : pour la systolique, la différence entre PAC et PAP, qui est de 8 à 10 mmHg(7) peut même atteindre 20 mmHg(8). Sachant qu’une augmentation de 20 mmHg de la systolique correspond à une majoration de 100 % du risque cardiovasculaire, une telle différence est loin d’être négligeable(9).
Cet écart entre PAP et PAC trouve son origine dans les déterminants de la pression aux différents étages de l’arbre artériel : lors de l’éjection ventriculaire, il se produit une première onde de pouls correspondant à la propagation du flux vers les artères périphériques. Cette onde est en partie réfléchie sur les bifurcations artérielles et revient en miroir au niveau de l’aorte pour se surajouter à la première : ce mécanisme rend compte de la majeure partie de la différence entre pression aortique et pression artérielle périphérique. La baisse de la compliance artérielle entraîne une augmentation de la réflexion de l’onde de pouls. Ainsi, l’élévation de la pression artérielle centrale reflète-t-elle la rigidité artérielle, elle-même corrélée à une augmentation du risque cardiovasculaire(10). Plus qu’un marqueur de risque, la rigidité artérielle est un facteur de risque à part entière, et l’hypertension artérielle est le principal facteur favorisant le développement de l’athérosclérose et la rupture de plaque. De fait, la pression artérielle centrale est fortement corrélée à l’athérosclérose carotidienne, à l’épaisseur intima/média, à l’hypertrophie ventriculaire gauche et à la dysfonction ventriculaire gauche diastolique. De même, la pression centrale est associée aux lésions des organes cibles, et notamment à l’atteinte rénale(11,12). Enfin, la pression centrale représente un meilleur facteur prédictif de la survie que la pression artérielle périphérique, comme le montrent l’étude ABPSS(13) et la Strong Heart Study(14). Le risque d’événement cardiovasculaire serait majoré de 13 % en cas de PAC élevée(13,15), de même que la mortalité cardiovasculaire(16).
Les antihypertenseurs ne sont pas égaux vis-à-vis de la pression centrale
Les médicaments antihypertenseurs permettent de réduire l’onde réfléchie et par conséquent la pression aortique. L’étude COMPLIOR montre notamment que la vitesse de l’onde de pouls (corrélée à la rigidité artérielle) est atténuée après un traitement de 6 mois par périndopril(17). Et si l’aténolol exerce un effet antihypertenseur périphérique sensiblement comparable à celui des IEC, il est nettement moins efficace sur la pression centrale(18,19).
Globalement, les antagonistes calciques ont une action hypotensive comparable au niveau central et périphérique, de même que les diurétiques. Les IEC, qui sont d’excellents antihypertenseurs périphériques, le sont plus encore au niveau central.
En pratique
Le contrôle de l’hypertension artérielle mesurée en périphérie laisse persister un risque cardiovasculaire résiduel, qui s’explique notamment par des mécanismes de découverte relativement récente.
L’hypertension est une maladie de l’arbre vasculaire qui induit des altérations artérielles : la prise en charge des patients hypertendus devrait prendre en compte, au-delà du contrôle de la PA brachiale, la pression centrale et la variabilité tensionnelle.
Le choix d’un antihypertenseur apportant un surcroît de protection apparaît essentiel.
L’association périndopril/amlodipine est plus efficace que d’autres pour agir à la fois sur la pression centrale et la variabilité tensionnelle, ce qui pourrait expliquer son efficacité supérieure en termes de réduction des événements cardiovasculaires.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :