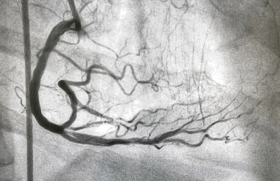
Coronaires
Publié le 09 oct 2012Lecture 8 min
Les acides biliaires dans l’athérogenèse coronaire - Vers une nouvelle cible thérapeutique potentielle ?
O. VARENNE*, H. AELION*, J. ROSENCHER*, H. DUBOC**. *Hôpital Cochin, Université Paris Descartes, Paris. **Hôpital Louis Mourier, Université Pierre et Marie Curie, Paris.
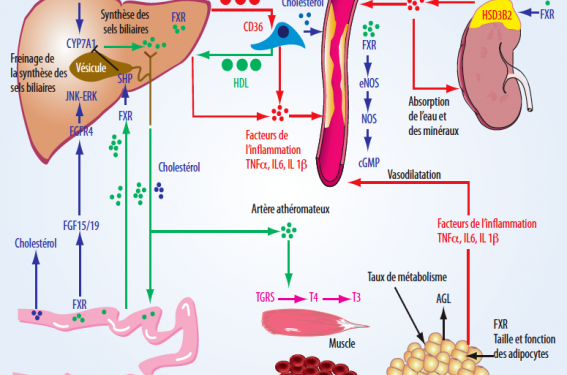
Les maladies cardiovasculaires continuent de représenter l’une des principales causes de morbidité et de mortalité dans le monde. Elles sont dominées par les maladies coronaires, dont l’athérosclérose et sa complication aiguë l’athérothrombose représentent le tournant évolutif. La physiopathologie de l’athérogenèse a fait l’objet, au cours des dernières décennies, de nombreuses recherches et publications, aboutissant à une prise en charge très codifiée et standardisée, bien détaillée dans les différentes recommandations de sociétés savantes telles l’American Heart Association (AHA) et l’European Society of Cardiology (ESC). Ces recommandations font la part belle au traitement par inhibiteurs de l’HMGCoA réductase, ou statines, qui permettent de limiter la survenue d’évènements cardiovasculaires en prévention primaire ou secondaire. Une meilleure compréhension des mécanismes conduisant à la formation des plaques d’athérosclérose et à ses complications athérothrombotiques pourrait permettre de développer de nouveaux traitements spécifiques.
Depuis longtemps il est connu que la formation de plaques d’athérome dans les artères coronaires dépend d’interactions étroites entre les monocytes circulants et l’endothélium des artères coronaires aboutissant à un état pro-inflammatoire local médié en partie par les macrophages. Plus récemment, un lien entre les acides biliaires circulants et l’athérogenèse a été mis en évidence. Il y a dix ans, la description du récepteur nucléaire FXR et du récepteur membranaire TGR5 aux acides biliaires a porté l’attention sur des molécules dont la médecine pensait avoir fait le tour : les acides biliaires.
Les acides biliaires (acides cholique, chénodéoxycholique, déoxycholique et lithocholique) sont des solvants lipidiques, dont l’action physicochimique permet de solubiliser les graisses alimentaires et ainsi de faciliter leur absorption intestinale. Les acides biliaires, en révélant leur mode d’action endocrinien, se sont révélés être des molécules signal impliquées dans de nombreuses voies métaboliques, dont celles impliquées dans l’athérogénèse. Les données scientifiques prometteuses et l’absence de données chez l’homme nous ont conduit à réaliser une étude clinique comparant les profils d’acides biliaires circulants chez les patients avec et sans athérome coronaire en faisant l’hypothèse que certains acides biliaires pourraient être potentiellement « protecteurs » contre l’athérome.
Physiopathologie
La physiopathologie du développement de la plaque d’athérome est très complexe. Quinze années de recherche sur les modèles animaux, telles les souris déficientes en apolipoprotéine E (Apo-/-) ou en récepteur du LDL (LDL-/-), nous ont appris que l’athérome n’est pas qu’une simple maladie dégénérative liée à l’âge mais bien une succession d’évènements physiopathologiques intriqués. En effet, la plaque d’athérome se forme via une succession d’interactions entre l’endothélium artériel, les macrophages de la plaque et leur capacité à évoluer vers des cellules riches en lipides, sous l’influence de la recapture des lipoprotéines oxydées via les récepteurs scavenger aux LDL, tel le récepteur CD36. Sur fond de maladie métabolique, où la sédentarité, le tabagisme et le patrimoine génétique jouent un rôle prépondérant, le processus de formation de la plaque se décrit comme une maladie inflammatoire chronique.
Les acides biliaires, molécules dérivées du cholestérol et dont le but primaire est d’émulsifier les lipides alimentaires lors de la digestion, ont connu un récent regain scientifique avec la découverte de deux récepteurs qui les lient spécifiquement au récepteur nucléaire au farsenoid X (FXR) et au récepteur transmembrannaire TGR5. La découverte de ces deux récepteurs a vu l’explosion du nombre de publications scientifiques liant le métabolisme glucido-lipidique aux acides biliaires, en tant que molécules régulatrices, leur conférant ainsi un véritable rôle endocrinien(1).
In vitro et chez l’animal, les deux récepteurs FXR et TGR5 ont montré un puissant effet contre l’athérogenèse, entre autres par un effet anti-inflammatoire direct sur les macrophages situés à l’intérieur de la plaque d’athérosclérose. Nourries avec un régime riche en graisses et en cholestérol, les souris doublement mutées FXR -/- et ApoE -/- développent des plaques d’athérome aortique 50 % plus larges que les souris simplement mutées ApoE-/-(2). De plus, l’administration d’agonistes de FXR aux souris ApoE-/- réduit de 95 % le développement de la plaque, tout en réduisant l’expression aortique de cytokines pro-inflammatoires (IL-1b et Il-6). Un mode d’action identique à été mis en évidence dans modèle murin LDL-/- : l’activation de TGR5 par un acide biliaire de synthèse induit une réduction importante de l’athérogenèse par plusieurs mécanismes(3) :
- la diminution de la synthèse de cytokines pro-inflammatoires par les macrophages (TNFa), et de l’expression de CD36 ;
- la limitation de la capacité de charge en LDL oxydés réduisant ainsi la transformation des macrophages en cellules spumeuses ;
- une réduction de la surface de la plaque d’athérome, alors que les souris LDL-/- et TGR5-/- ont une augmentation dramatique de la taille des lésions athéromateuses aortiques.
Figure 1. Athérosclérose aortique chez les souris sauvages (Wildtype), déficiente en récepteur nucléaire au farsenoide (FXR-/-), au récepteur à l’apolipoprotéine E (ApoE-/-) ou au deux (FXR-/-ApoE-/-). La surface des plaques d’athérosclérose est significativement plus marquée chez les souris ApoE-/- et encore plus chez celles FXR-/- ApoE-/-.
Le récepteur FXR, principalement exprimé dans le foie et l’intestin, régule négativement la néoglucogenèse hépatique, la synthèse d’acides biliaires et la recapture du cholestérol par le foie. Chez l’animal, son activation peut également diminuer les taux circulants de triglycérides et de cholestérol, dessinant ainsi une boucle physiologique du métabolisme lipidique : depuis l’absorption digestive des lipides permise par l’effet physicochimique des acides biliaires, jusqu’à la recapture cholestérolique par le foie. Le récepteur TGR5, dont l’expression est plus ubiquitaire, augmente la dépense énergétique en agissant sur la iodothyrioninedéiodinase, enzyme qui assure la conversion de l’hormone thyroïdienne inactive T4 en forme active T3. Ainsi, l’activation de TGR5 prévient le développement de l’obésité chez les souris nourries avec un régime riche en lipides, en augmentant leur dépense énergétique.
Notre étude
Nous avons décidé d’étudier l’existence d’un rôle des acides biliaires circulants sur la maladie coronaire chez l’homme en conduisant une étude prospective chez des patients coronariens admis à l’hôpital Cochin pour une coronarographie.
Durant une période de 4 mois, tous les patients hospitalisés pour une coronarographie conventionnelle au cours d’un syndrome coronaire aigu, pour un angor stable, une ischémie silencieuse ou un dépistage de coronaropathie ont été inclus. Le protocole a été approuvé par le comité d’éthique local.
Figure 2. Etude de Cochin. Population de patients adressés pour coronarographie diagnostique. Le principal critère d’exclusion était la prise de statines au moment de la coronarographie.
Les patients ressuscités d’un arrêt cardiaque extrahospitalier, les patients traités par statines, antibiotiques dans les 6 semaines précédents l’hospitalisation, corticoïdes, thérapie antiVIH, ceux présentant une hépatopathie chronique ou ressuscités d’un arrêt cardiaque extrahospitalier ont été exclus de cette étude. Tous les prélèvements étaient réalisés après 8 heures de jeûne et les données cliniques et biologiques ont été collectées prospectivement après la coronarographie chez les patients admis pour syndrome coronarien aigu ou avant en cas d’examen programmé.
Après inclusion, les données cliniques et biologiques ont été prospectivement collectées après 8 heures de jeûne chez les patients en syndrome coronaire aigu ou avant la coronarographie en cas d’examen programmé.
Les patients ont été classés en deux groupes selon la présence (groupe A) ou l’absence (groupe B) d’athérome coronaire visible sur la coronarographie conventionnelle.
Au total, sur près de 400 patients prospectivement screenés, seuls 27 avec athérome coronaire et 17 sans ont été inclus dans l’analyse finale. Le principal motif d’exclusion était la prise régulière de statines. Le critère discriminant a été l’absence ou la présence d’athérome sur les coronarographies, sans toutefois tenir compte de la sévérité des lésions dans la mesure où les acides biliaires ont été liés au développement de l’athérome, et non à la rupture de plaque ou l’angor clinique.
Les groupes ont été ensuite comparés par test statistique de Fischer ou de Wilcoxon.
La concentration de l’acide lithocholique, le plus puissant ligand naturel de TGR5, est significativement diminuée (baisse de 50 %) chez les patients coronariens (médiane = 0,03 μmol/l chez les coronariens et 0,08 μmol/l chez les patients indemnes de lésions coronaires, p = 0,015).
En analyse multivariée, la concentration plasmatique d’acide lithocholique est le seul facteur prédictif d’athérome coronaire indépendamment du sexe (odds ratio 2,41 pour chaque réduction de 0,05 μmol/l ; IC : 1,11 à 5,25, p = 0,027)(4).
Ce travail identifie la baisse de l’acide lithocholique comme un facteur prédictif d’athérome coronaire (détectable en coronarographie), suggérant l’hypothèse que sa diminution s’accompagnerait d’une perte de son effet protecteur. Notre résultat, bien qu’insuffisant pour présenter la baisse de l’acide lithocholique comme un nouveau facteur de risque d’athérome coronaire à usage clinique, ouvre une nouvelle voie dans la physiopathologie de l’athérome et dans sa prévention.
D’autres études réalisées chez l’homme ont montré des résultats similaires. Un travail rétrospectif chez des patients coronariens discriminés selon la sévérité des lésions coronaires, a montré une tendance, à la baisse de l’acide lithocholique(5) bien que non significative statistiquement. Plus surprenant, l’origine de cette baisse plasmatique pourrait être d’origine intestinale : c’est la flore intestinale chez l’homme, qui synthétise exclusivement l’acide lithocholique par la transformation de l’acide chénodéoxycholique. Dans ce même ordre d’idées, une étude israélienne a trouvé une diminution de la concentration fécale d’acide lithocholique chez des patients coronariens(6).
Une étude plus large reste à mettre en place afin de confirmer ces résultats.
L’avenir dira si le bilan de nos patients devra s’enrichir d’un dosage sérique des acides biliaires, et si les agonistes synthétiques des récepteurs TGR5 et FXR rejoindrons l’arsenal thérapeutique standard du patient coronarien.
Une des limites majeures de l’étude vient de la définition de l’athérome lors de la coronarographie conventionnelle. En effet, on sait depuis de nombreuses années, que la formation de plaques d’athérome demeure longtemps sans retentissement sur la lumière artérielle du fait de l’élargissement compensatoire (remodelage positif). Une coronarographie « normale » ne peut exclure la présence de plaque d’athérome, y compris à un stade avancé, dans la paroi artérielle coronaire. Les nouvelles techniques d’imagerie (scanner multicoupes, échographie endocoronaire, OCT) pourraient amener une définition phénotypique plus précise de ces patients dans une étude en cours.
Figure 3. Schéma. Différence de concentration en acide lithocholique entre les patients avec et ceux sans athérome détectable en angiographie coronaire.
Conclusion
La perspective d’une nouvelle voie métabolique comprenant les acides biliaires et leurs récepteurs nucléaires participant à l’athérogenèse suscite de vifs espoirs afin d’identifier de nouvelles cibles thérapeutiques antiathérome.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :