Congrès et symposiums
Publié le 08 jan 2013Lecture 6 min
Prise en charge des extrasystoles ventriculaires
S. ABBEY, Nouvelles Cliniques Nantaises, Nantes
ELECTRA
La prise en charge des extrasystoles ventriculaires (ESV) représente un motif de consultation fréquent. C’est un problème de pratique quotidienne en cardiologie qui est le plus souvent banal, mais qui peut parfois être aussi angoissant. Le contexte de découverte des ESV est très varié, allant de l’examen de dépistage, par exemple lors de la réalisation d’un ECG chez un patient asymptomatique (bilan pour certificat d’aptitude au sport) au bilan de palpitations, voire de syncope ou de mort subite. La prévalence des ESV dépend du mode de dépistage et de la durée d’enregistrement. Elle varie de 10 % sur un ECG à plus de 20 % sur un holter ECG de 24 heures. La prévalence augmente avec l’âge du patient, la présence d’une cardiopathie sous-jacente, le moment d’enregistrement, etc.
Première étape : anamnèse
Lors de la prise en charge, la première étape est de définir l’anamnèse de façon la plus exhaustive possible (antécédents personnels et familiaux) et de dépister les symptômes. Pour la plupart des patients, les ESV sont asymptomatiques, surtout lorsqu’elles sont découvertes à l’occasion d’un examen systématique. En revanche, les symptômes les plus fréquemment décrits sont les palpitations ou la sensation d’irrégularité cardiaque au décubitus, plus rarement des lipothymies ou syncopes. Mais il ne faudra pas ignorer le retentissement hémodynamique en rapport avec la bradysphygmie (ou « fausse » bradycardie) en cas de bigéminisme ventriculaire, qui est responsable d’une asthénie ou une dyspnée d’effort.
Deuxième étape : ECG
C’est une analyse scrupuleuse de l’ECG : la description de l’ESV est ce qui attire le plus souvent l’œil. Le diagnostic est le plus souvent aisé avec l’analyse de la morphologie de l’ESV et surtout de l’activité atriale rétrograde ou dissociée.
• La morphologie de l’ESV a une implication également étiologique : plus les ESV ont une faible amplitude avec un aspect crocheté, polyphasique et élargi, plus il faudra rechercher une cardiopathie sous-jacente et effectuer un bilan le plus exhaustif possible.
• L’analyse de l’aspect ECG du rythme sinusal aura également son importance : la présence d’une onde Q orientera vers une cardiopathie ischémique, mais il faudra également rechercher attentivement des anomalies de la repolarisation (à la recherche d’arguments en faveur d’une canalopathie ou d’une dysplasie arythmogène du ventricule droit [DAVD]).
La répétition des ECG au cours du suivi sera nécessaire puisque l’évolution de l’aspect de l’ECG pourra révéler tardivement une pathologie sous-jacente (négativation des ondes T dans le précordium par exemple pour une DAVD…). Enfin, il conviendra d’essayer de trouver si possible une concordance entre la localisation de l’ESV d’après la morphologie sur l’ECG 12 dérivations et la cardiopathie sous-jacente, notamment en cas de trouble de la cinétique (imputabilité de l’ESV à la cardiopathie).
Troisième étape : enquête étiologique
• Le bilan standard devra comprendre :
- une échographie transthoracique (analyse de la cinétique segmentaire et globale, calcul de la fraction d’éjection, cavités droites, etc.) ;
- une épreuve d’effort pour éliminer une TV catécholergique, rechercher des arguments en faveur d’une cardiopathie ischémique, une DAVD… : la disparition des ESV à l’effort est un élément rassurant en faveur de bénignité, l’apparition ou l’aggravation d’ESV à l’effort ou en récupération étant plus péjorative(1) ;
- un holter ECG pour la mesure quantitative (analyse de la charge en ESV) et qualitative (couplage des ESV, distribution diurne ou nocturne, cathécolergiques ou vagales, etc.).
• Le bilan ultérieur sera orienté selon les résultats de ces examens :
- recherche d’une éventuelle coronorapathie sous-jacente (coronarographie, coroscanner, scintigraphie myocardique… selon les organisations locales) ;
- réalisation d’une IRM cardiaque, en ayant bien précisé au radiologue le motif et l’orientation diagnostique (bilan de CMD, DAVD…). Cet examen pourra parfois nécessiter la prise d’un traitement antiarythmique préalable pour avoir une analyse fiable ;
- recherche des potentiels tardifs : cet examen est très intéressant en cas d’ESV provenant de l’infundibulum pulmonaire car leur absence est un élément important pour écarter le diagnostic de DAVD et ainsi éviter un bilan plus exhaustif. Leur présence est un critère diagnostique pour la DAVD. À noter qu’une nouvelle classification pour le diagnostic des DAVD a été tout récemment proposée avec comme principal objectif d’être plus sensible pour le dépistage(2). Un focus est réalisé sur l’anamnèse et les examens proposés en routine : description plus précise du poids des antécédents familiaux, des anomalies de la repolarisation sur l’ECG (inversion de l’onde T), de l’étude morphologique du ventricule droit observé à l’ETT, et de la morphologie et la quantification des ESV, notamment à l’épreuve d’effort(1). Ainsi, l’analyse de l’axe des ESV à type de retard gauche revêt un caractère important : un axe supérieur représente un critère majeur en faveur d’une DAVD alors qu’un axe inférieur est un critère mineur ;
- recherche d’un syndrome d’apnée du sommeil : elle devra être envisagée en cas d’ESV à prédominance nocturne.
• La place de l’exploration électrophysiologique est moins prépondérante, en dehors de pathologies bien spécifiques (DAVD, tétralogie de fallot, etc.). Le test à l’isoprénaline semble un examen prometteur en cas de suspicion de DAVD.
La présence d’une anomalie de la repolarisation (syndrome de Brugada, QT long, repolarisation précoce…) nécessitera un bilan plus approfondi et un rapprochement auprès d’un centre de compétence concernant les maladies rythmiques ventriculaires et éventuellement une analyse génétique moléculaire.
Si l’ensemble du bilan est normal, on conclura à des ESV bénignes sur cœur sain. Ces ESV s’inscrivent essentiellement dans deux cadres nosologiques bien distincts : soit des ESV répétitives sous la forme de bitrigéminisme, disparaissant à l’effort, et souvent à l’origine d’une bradysphygmie, soit des ESV/TVNS d’effort symptomatiques sous la forme de palpitations.
Quatrième étape : définir la prise en charge thérapeutique (figure 1) et le suivi
Le traitement dépend, d’une part, des symptômes et, d’autre part, de la cardiopathie sous-jacente.
Figure 1. Orientation diagnostique et traitement.
• En présence d’une cardiopathie ischémique ou d’une cardiomyopathie dilatée, la seule FEVG < 35 % suffira à décider de l’implantation prophylactique d’un DAI si le traitement médical est par ailleurs optimal. La prise en charge spécifique des ESV dans ce cadre ne sera justifiée qu’en cas de symptômes reliés à ces ESV ou en cas de suspicion de cardiopathie rythmique associée. En effet, en cas de charge en ESV > 20 % sur le holter ECG, il faudra au préalable évoquer le diagnostic de cardiopathie induite par les ESV et proposer un traitement, même si les ESV sont paucisymptomatiques en termes de palpitations(3). Le traitement est alors limité soit aux antiarythmiques de classe III (amiodarone surtout), soit le plus souvent à l’ablation par radiofréquence.
• Concernant les ESV bénignes, la première étape sera de rassurer le patient. Des mesures hygiéno-diététiques peuvent être prodiguées (diminution des excitants tels que caféine ou alcool) avec malheureusement un effet souvent modeste. Il ne faudra traiter que les ESV symptomatiques et ne pas chercher à « maquiller » les ECG et holter. Il est alors habituel de débuter par des bêtabloquants ou des inhibiteurs calciques bradycardisants avant d’envisager éventuellement un antiarythmique de classe IC.
• Chez les patients qui restent symptomatiques malgré le traitement, ou pour qui la tolérance des traitements est médiocre, ou qui ne souhaitent pas de prise médicamenteuse, l’ablation par radiofréquence (figure 2) est une alternative très efficace avec une indication de classe IIA selon les recommandations internationales(4), et peu dangereuse à condition que l’opérateur soit expérimenté et particulièrement rompu aux différents pièges possibles concernant les localisations des ESV.
Dans tous les cas, un suivi périodique sera nécessaire (ECG et holter ECG).
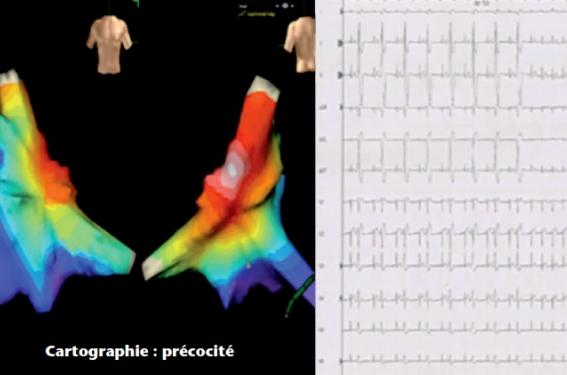
Figure 2. Exemple de cartographie d’ESV infundibulaire bénigne (origine focale) avec disparition dès le début du tir de radiofréquence.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :








