Publié le 26 avr 2005Lecture 9 min
IRM et cœur - Itinéraire d'une enfant gâtée : historique
J.-M. PERNES, hôpital privé d’Antony

Les espoirs placés dans cette nouvelle technique née au milieu du siècle dernier sont concrétisés par une imagerie désormais utilisable en routine. Aujourd’hui, ses différentes séquences d’acquisition ont trouvé de formidables applications en pratique clinique. Ce numéro intégral de Cardiologie Pratique fait un état des lieux de cette technique avec le concours de différents centres experts en la matière.
Le passé recomposé
En 1946, F. Block et E. Purcel de l’université de Stanford et d’Harvard découvrent et décrivent simultanément et indépendamment le phénomène de résonance magnétique nucléaire et partagent à ce titre en 1952 le prix Nobel de physique.
Jusqu’en 1970, la spectroscopie par résonance magnétique représente la seule application de cette découverte, principalement utilisée pour analyser les structures physiques et chimiques moléculaires.
En 1971, R. Damadian, médecin américain, constate que les temps de relaxation des tissus tumoraux diffèrent de ceux des tissus normaux, suggérant pour la première fois que ce phénomène de résonance magnétique pourrait être utilisé dans la détection des cancers. Malgré le scepticisme de la communauté scientifique, il entreprend la réalisation d’un aimant supraconducteur qui devait aboutir en 1977 aux premières images du thorax humain.
Certes, en 1973, P. Lauterbur, chimiste américain et P. Mansfield physicien britannique, ont déjà obtenu des images de petits objets et ce dernier chercheur a, entre-temps, établi les modalités du traitement mathématique et de l’analyse par ordinateur des signaux, permettant de mettre au point une technique d’imagerie utilisable. Pour leurs travaux, ces deux chercheurs se voient attribuer en 2003 le prix Nobel de médecine, décision à l’issue de laquelle R. Damadian se déclare profondément déçu, jugeant même que le comité Nobel a tenté de réécrire l’histoire ! Pour la petite histoire, il vient d’entamer une campagne pour faire valoir sa place de père de l’IRM, suivi dans sa démarche par une grande partie de la communauté scientifique qui juge, comme lui, que les travaux des lauréats arrivent en 2e et 3e positions dans sa mise au point. Une démarche qui restera vraisemblablement sans suite : les décisions du comité Nobel étant sans appel.
Quoiqu’il en soit, en 1975, R. Ernst propose d’utiliser la transformation mathématique de Fourrier pour obtenir une image spatiale à partir du codage de fréquence générée par l’onde radiofréquence au sein du champ magnétique. C’est à cette date que, sans doute pour éviter la confusion avec la médecine nucléaire, la technique se baptise imagerie par résonance magnétique.
En 1977, Damadian rapporte des images du corps entier par la technique. La même année, Jacobus et Garlick publient les premiers spectres par résonance magnétique du phosphore à partir de cœur de rat perfusé, à l’origine de très nombreuses publications sur le métabolisme myocardique des phosphates de haute énergie.
Il faudra attendre 1980 pour que Goldman décrive les premières applications potentielles de l’imagerie cardio-vasculaire, prévisions qui, quelques vingt années plus tard, se sont pratiquement toutes accomplies. Outre l’excellente qualité de l’imagerie anatomique observée dès cette période, de nombreux auteurs notaient déjà la présence des modifications des paramètres de relaxation du myocarde infarci, base du développement futur de la technique d’IRM baptisée rehaussement tardif, et insistaient sur le fait que ces différences entre myocarde sain et nécrosé ou fibrotique pouvaient être accentuées par l’utilisation des produits de contraste de type chélates de gadolinium (figure 1).
Figure 1. Séquence de rehaussement tardif après IDM inférieur : hypersignal dix min après injection de gadolinium.
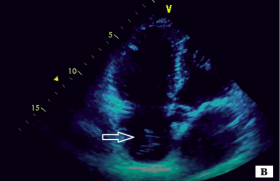
À cette période, les séquences dites de spin écho, synchronisées sur l’ECG, fournissaient un excellent contraste entre le sang circulant dans les cavités cardiaques quittant la zone excitée avant la réception du signal et apparaissant en noir, et les structures tissulaires avoisinantes, certes mobiles, apparaissant plus ou moins blanches selon leurs propres caractéristiques de relaxation. C’est cette propriété qui continue d’être mise à profit pour imager l’œdème apparaissant dans les heures et jours suivant un IDM aigu, particulièrement bien visible sur les séquences dites pondérées en T2, objectivant spontanément l’hypersignal transitoire dans la zone infarcie, à même de distinguer un infarctus récent d’une nécrose ancienne (figure 2).
Figure 2. Contraste spontané lié à l’œdème après infarctus latéral responsable de l’hypersignal.
Malheureusement, la nécessité d’un temps d’acquisition prolongé sur plusieurs minutes rendait cette technique peu rentable pour l’évaluation du cœur.
Le présent : 20 ans ! le bel âge, celui des rêves et des espoirs...
Le grand pas qui a permis de concrétiser les espoirs placés dans la technique à la fin du siècle dernier a été franchi dès lors qu’est apparue une méthode d’acquisition différente, dite en écho de gradient rapide, capable de fournir des images dynamiques des structures cardiaques avec une excellente définition spatiale et temporelle au cours d’une seule apnée, d’une durée de 20 secondes.
Cela est réalisé de manière routinière aujourd’hui grâce à un changement complet de philosophie dans le timing d’administration des ondes radiofréquence. Ces séquences aux acronymes barbares (FISP, FIESTA, FLASH etc.) permettent notamment une différenciation très fine entre myocarde et sang circulant, indépendamment des conditions hémodynamiques, séquences dites en sang blanc (figure 3), représentant à ce jour la méthode de référence d’évaluation de la cinétique cardiaque globale et régionale.
Figure 3. Séquence écho de gradient rapide SSFP pour étude de la cinétique en équivalent coupe petit axe.
Il est même déjà possible aujourd’hui d’obtenir l’acquisition sur un seul cycle cardiaque (35 phases/seconde sur un seul battement cardiaque avec un voxel de 2 mm).
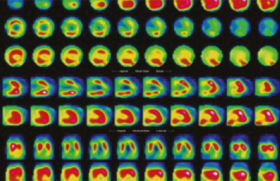
L’un des développements majeurs de ces techniques d’imagerie rapide en IRM concerne l’évaluation de la viabilité myocardique au travers notamment du concept de rehaussement tardif. Celui-ci présente des similitudes avec la redistribution du thallium des méthodes isotopiques, la différence majeure étant qu’en IRM ce rehaussement est observé quelques minutes (10-15) après le premier passage du produit de contraste contre quelques heures (3 à 48 pour la scintigraphie). Autre différence, le chélate de gadolinium utilisé s’accumule dans le myocarde non viable alors que le thallium se distribue dans le myocarde viable. Ainsi, le myocarde qui ne se rehausse pas sur les images tardives est considéré comme viable. Les séquences d’acquisition actuelles, notamment celles dites en inversion-récupération, permettent, en annulant le signal du myocarde normal, une augmentation de l’intensité du signal des régions infarcies de 500 à 1 000 % par rapport aux régions saines, alors que les techniques initiales de spin écho n’autorisaient simplement qu’un gain de 50 à 100 % du myocarde anormal (J.-M. Pernes et coll.)
Ce concept de rehaussement tardif a de formidables applications dans le domaine clinique ; bien que non spécifique, il permet, outre l’évaluation de la viabilité lorsque sa distribution correspond au territoire de perfusion coronaire, de confirmer le diagnostic de myocardite aiguë et de certaines myocardiopathies plus rares, lorsque sa distribution est plus aléatoire et indépendante de la perfusion, comme le détaillent fort bien O. Vigneaux et coll. dans l’article dédié à l’apport de l’IRM au diagnostic des myocardiopathies.
L’étude de la perfusion coronaire en temps réel, au premier passage après injection de gadolinium, après épreuve de stress pharmacologique (injection de persantine ou adénosine) est déjà une méthode potentiellement capable d’évaluer la présence d’une ischémie myocardique. Cette application est particulièrement développée dans l’article de P. Croisille, de l’équipe de Lyon, dont le fer de lance, D. Revel, vécut dès les années 1985, le début de la grande aventure auprès de l’équipe de San Francisco de Higgins, pionnier éclairé de l’IRM cardiaque.
Outre l’aspect morphologique, une approche fonctionnelle de la pathologie valvulaire est rendue possible par l’utilisation de techniques d’acquisition particulières, notamment sensibles à la vélocité, à l’origine d’une quantification possible des flux de régurgitation ou d’évaluation des sténoses.
L’article de D. Didier, autre pionnier émérite de la méthode, fournit un aperçu exhaustif de l’apport de la technique dans le diagnostic et le retentissement des valvulopathies fuyantes et sténosantes.
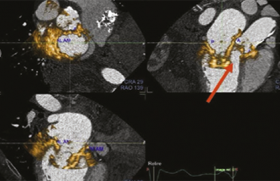
Il est sans doute prématuré d’annoncer que l’ère de l’étude de l’anatomie coronaire par angio-IRM est arrivée. Comme le montre l’article de J.-M. Serfati et coll., toutes les contraintes techniques liées à la cinétique particulière des artères épicardiques n’ont pas encore été levées. Mais contrairement aux autres méthodes d’imagerie utilisant rayons X ou ultrasons par exemple, il n’existe pas pour l’IRM de limitation technologique fondamentalement rédhibitoire aux progrès potentiels. Ceux-ci sont essentiellement liés au talent des chercheurs susceptibles de découvrir la ou les séquences d’acquisition dédiées à une problématique spécifique. Parallèlement à l’étude de la lumière artérielle, de gros espoirs sont placés dans l’étude fine de la paroi et la caractérisation de la plaque vulnérable, qui est un des « Graals » de la cardiologie moderne. Certaines particules superparamagnétiques, les USPIO, petits grains d’oxyde de fer recouverts d’un manteau hydrophile, sont cannibalisées par les macrophages, dont on sait qu’ils colonisent avec avidité la plaque à risque, notamment au niveau de son épaulement.
Des premiers travaux ont montré l’existence d’un hyposignal tardif, traduisant la présence de particules dans les macrophages, sur des imageries réalisées à 24 h et ont ouvert la voie à une recherche fascinante.
L’avenir : les courses à haut champ
Aujourd’hui, l’imagerie cardiaque est obtenue sur des machines dont l’aimant a une puissance de 1,5 Tesla. Encore embryonnaire, la spectroscopie par résonance magnétique devrait trouver des applications cliniques avec les aimants 3 Tesla, la tendance de développement actuelle. Celle-ci nécessite une localisation soigneuse du signal dans la zone d’intérêt du myocarde pour éviter la contamination par des signaux environnants.
Les applications cliniques en spectroscopie du myocarde concernent principalement le métabolisme du phosphore, même si en théorie cette technique est applicable à d’autres noyaux tels que l’hydrogène, le carbone 13, le fluor 19 ou le sodium 23. Bien qu’à relativement faible concentration dans le myocarde, le phosphore 31 est présent au sein de molécules très importantes pour le métabolisme myocardique, tels les phosphates de haute énergie (ATP), la phosphocréatine et les phosphates inorganiques.
La phosphocréatine est labile, sa concentration diminue rapidement en cas d’ischémie alors que celle de l’ATP est beaucoup plus stable et reste longtemps normale, même en présence d’une ischémie prolongée. Le rapport phosphocréatine/ATP a donc été étudié pour l’évaluation de l’ischémie coronaire 1,5 Tesla au repos et à l’effort. À 3 Tesla, le recueil de phosphates inorganiques est possible ; sa valeur ainsi que sa position dans le spectre du phosphore reflètent le Ph intracellulaire. Des études préliminaires ont montré des altérations significatives du spectre dans le fameux syndrome X, cauchemar des cardiologues de plusieurs générations successives, que les auteurs de ces articles princeps attribuent à une altération de la microcirculation responsable d’une ischémie myocardique. Actuellement, avec les systèmes 1,5 Tesla les plus pointus, seul le recueil d’un signal de la paroi antérieure du myocarde est possible, l’utilisation de hauts champs 3 Tesla, le développement d’antenne de surface et l’appoint de nouvelles séquences laissent augurer l’exploration de la totalité du myocarde en spectroscopie au phosphore.
En matière d’imagerie, le passage à 3 Tesla et l’amélioration subséquente du rapport signal/ bruit optimisera la résolution spatiale au prix a priori d’une diminution de la vitesse d’acquisition. Les raffinements techniques issus du compromis entre résolution spatiale et vitesse d’acquisition favoriseront sensiblement les performances de la méthode en matière d’étude de la perfusion et de viabilité. L’amélioration de la résolution temporelle réduira encore les artefacts de mouvement et de flux, autorisant virtuellement l’acquisition et la visualisation en temps réel, d’où une évaluation encore supérieure de la cinétique en une seule apnée, voire un seul cycle cardiaque, avec un excellent rapport signal/bruit. Une visualisation ciné-fluoroscopique en temps réel est déjà d’actualité et l’on peut envisager dans un futur plus ou moins proche la substitution des rayons X par l’IRM pour la navigation vasculaire diagnostique, voire interventionnelle.
« L’avenir est un lieu bien commode pour y mettre les songes ! » (Anatole France)
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :