Rythmologie et rythmo interventionnelle
Publié le 29 juin 2009Lecture 9 min
Le syndrome de Brugada en pratique quotidienne : que doit savoir le clinicien ?
A. BONNY1, 2, W. AMARA3, B. HAMDAOUI4, R. FRANK2. 1Hôpital Saint Camille, Bry sur marne ; 2Pitié-Salpêtrière, Paris ; 3CH Le Raincy-Montfermeil ; 4Hôpital Henri-Mondor, Créteil
Le syndrome de Brugada est une maladie électrique du cœur, responsable de morts subites. Le sus-décalage en dôme de V1 à V3, morphologie de repolarisation pathognomonique de cette canalopathie, est inconstante, puisque lors du suivi, 2/3 des patients modifient ou normalisent leur repolarisation par moments. Ces morts subites se manifestent le plus souvent à l’âge adulte, bien qu’il en existe des formes infantiles, révélant souvent la maladie, parfois découvertes après une syncope, un bilan familial, ou un ECG systématique. Les facteurs prédictifs de mort subite chez les sujets asymptomatiques représentent la grande question non résolue dans ce syndrome. Le DAI reste le seul traitement préventif de la mort subite chez les patients avec syncopes ou arrêt cardiaque ressuscité. Il est cependant greffé d’un taux de complications important. La prévention primaire des sujets asymptomatiques est une question encore non résolue. Ces particularités rendent compte de la difficulté de la prise en charge du syndrome de Brugada.
Points clés
- Le syndrome de Brugada est une canalopathie responsable de mort subite sur cœur « sain ».
- Le sus-décalage en dôme de V1 à V3 (type 1) est la morphologie électrique diagnostique du syndrome et a une valeur pronostique péjorative.
- La mise en évidence spontanée (précordiales droites classiques ou hautes, dérivations inférieures) ou induite (ajmaline ou flécaïne) du type 1 est indispensable pour envisager l’implantation d’un défibrillateur automatique implantable (DAI).
- L’histoire familiale de mort subite et la stimulation ventriculaire programmée prédisent peu du risque rythmique intrinsèque, même en cas de type1 spontané.
- Tout Brugada asymptomatique, même en cas de type 1 à l’ECG et la présence d’autre FDR, ne relève pas de l’implantation d’un DAI. Dès lors, le rapport bénéfice-risque des tests pharmacologiques et la SVP déconseille leur utilisation dans cette population.
- Les symptômes (syncope, mort subite récupérée) posent l’indication d’un DAI.
- La mutation du gène SCN5A n’est présente que dans 20 % des cas. Elle n’a aucune valeur prédictive de mort subite mais peut être utile pour le diagnostic.
Définition
Le syndrome de Brugada (SB), décrit par les frères Brugada en 1992, est caractérisée par une élévation du point J et un sus-décalage du segment ST en « dôme » dans les précordiales droites (V1-V3), associé à des symptômes en rapport avec des troubles du rythme ventriculaire malins : respiration nocturne agonique, syncope inexpliquée ou mort subite.
Historique
Les premiers cas de mort subite nocturne ont été décrits chez des asiatiques jeunes, avec 40 ans d’âge moyen, le plus souvent de sexe masculin. Pokki huirri au Japon, Lai Tai en Thaïlande, Bangungun au Vietnam. Cette pandémie de mort subite nocturne a eu pour conséquence le déguisement nocturne des hommes en femmes, afin d’échapper aux mauvais esprits à la recherche d’hommes valides.
Épidémiologie et Génétique
Il s’agit d’une canalopathie, impliquant probablement plusieurs mutations génétiques, dont la première identifiée est située au niveau du gêne codant pour le canal sodique SCN5A, trouvée chez 15 à 25 % des sujets. On a trouvé d’autres mutations dans d’autres gênes codant pour le canal sodique et le canal calcique lent. La transmission est autosomique dominante avec 40 % de forme familiale.
Chez l’adulte, il touche quatre fois plus d’hommes que de femmes. La prévalence de l’aspect ECG du syndrome de Brugada est plus forte dans la population asiatique par rapport aux caucasiens, respectivement 12-14/10 000 versus 2-5/10 000. L’épidémiologie du SB est mal connue en Afrique mais certains cas ont été récemment rapportés. Le pic de fréquence de mortalité va de 30 à 45 ans. Cette mortalité est souvent nocturne, et peut aussi être favorisée par la fièvre. La prévalence de ces morts subites est difficile à évaluer. Si 4 % des morts subites restent inexpliquées à l’autopsie, on estime que le quart d’entre elles sont dues à des canalopathies, dont une partie peut correspondre au SB.
L’électrocardiogramme du syndrome de Brugada
Morphologies
(figure 1)
Figure 1. Les 3 morphologies évocatrices du SB, le type 1 étant le seul diagnostic du syndrome de Brugada.
La morphologie typique de l’ECG du Brugada, dite type 1, est caractérisée par un sus-décalage en dôme (coved-type) du segment ST au niveau des précordiales droites (V1-V3), une élévation du point J ≥ 2 mm avec portion terminale descendante du segment ST et ondes T négatives. Cet aspect est culminant en V2. Cette morphologie peut se modifier spontanément en des aspects non spécifiques, improprement dénommés type 2 ou type 3. Le type 2 en selle (saddleback-type), signe une élévation du point J ≥ 2 mm avec portion terminale du segment ST ≥ 1 mm associée à une onde T positive ou biphasique. Le type 3 peut invariablement prendre l’aspect du type 1 ou 2 mais avec pour particularité un sus-décalage de la portion terminale du segment ST de moindre importance : < 1 mm.
Le type 1 est le seul aspect ECG diagnostic du SB et fait partie de la définition de ce syndrome.
Les 2 autres types imposent donc de le mettre en évidence, de manière spontanée ou provoquée par des tests pharmacologiques avant d’affirmer le diagnostic du SB.
Comment démasquer l’ECG type 1 du syndrome de Brugada ?
La principale caractéristique de la repolarisation du SB est son caractère fluctuant : d’un instant à un autre, tous les types peuvent se succéder, même la normalisation du segment ST. Dès lors, la mise en évidence du type 1 est essentielle.
a. Dérivations hautes : le positionnement des électrodes V1 et V2 au niveau du 2e espace intercostal (EIC) et V3 au 3e EIC permet souvent de démasquer le type 1 (figure 2).
b. Bien analyser les dérivations inférieures (DII, DIII, aVF) et même latérales car il a été décrit un aspect de type 1 de localisation atypique.
c. Les tests pharmacologiques ont une bonne sensibilité et spécificité : l’ajmaline (1 mg/kg en 5 min) et la flécaïne (2 mg/kg ou max 150 mg en 10 min) majorent ou démasquent l’aspect en dôme (type 1). Le risque de ces tests est de déclencher une fibrillation ventriculaire, et ils ne doivent être fait que dans une unité de surveillance continue. L’ajmaline a l’avantage d’une demi-vie plus courte, réduisant la durée d’observation post-procédure.
Figure 2. Démasquage du type1 en positionnant les électrodes V1, V 2 et V 3 au 3e EIC et majoration du sus-décalage au 2e EIC. EIC- espace intercostal.
Faut-il proposer un test pharmacologique à tous les sujets avec un ECG type 2 ou 3 ?
Oui, s’ils ont des symptômes évoquant un trouble du rythme (palpitations, lipothymies, syncope), ou s’il existe un antécédent familial de mort subite.
Faut-il proposer un test pharmacologique chez un sujet asymptomatique avec ECG normal et histoire familiale de mort subite du syndrome de Brugada ?
La faible valeur prédictive de l’histoire familiale, la bénignité de l’ECG normal et l’absence d’indication du DAI chez les sujets asymptomatiques rendent ce test peu utile, sauf pour savoir si le sujet serait porteur d’une anomalie du canal sodique du fait de la majoration de la pénétrance du phénotype en cas de mutation du gène.
Attention aux faux positifs !
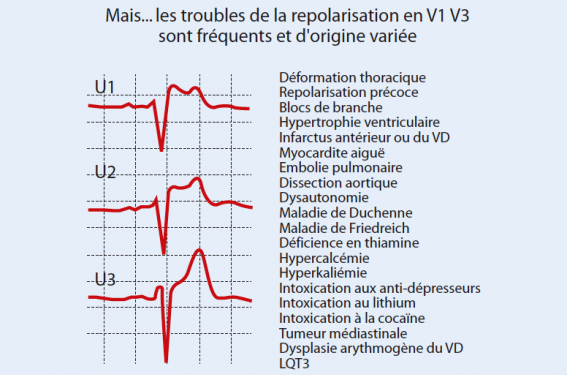
Certaines pathologies (figure 3) modifient l’ECG avec un aspect « Brugada-like ».
Figure 3. Pathologies induisant des troubles de la repolarisation de type « Brugada-like ».
Mécanisme de l’arythmogénèse
L’hétérogénéité des périodes réfractaires des cellules myocardiques (en particulier du ventricule droit) à l’origine des réentrées en phase 2 induisant les arythmies ventriculaires (TV et FV) est la théorie la plus communément admise et développée par C. Antzelevich et al.
Devant un ECG de type 2 ou 3 et un contexte clinique suspect, on tente de révéler l’aspect en dôme en enregistrant les dérivations précordiales hautes (2 espaces intercostaux plus haut) et surtout par un test pharmacologique (ajmaline ou flécaïne).
Les tests pharmacologiques n’ont aucun intérêt en cas de type 1 spontané (dérivations classiques ou hautes).
Affirmer le diagnostic
Le SB répond à des critères précis :
- Sus-décalage du ST en dôme ≥ 2 mm en V1, V2 ou V3 suivit d’une onde T négative.
- Mort subite récupérée, FV, TV polymorphe ou syncope, épisode de respiration nocturne agonique ou antécédent familiaux de mort subite avant 45 ans ou FV inductible lors de la stimulation ventriculaire programmée (SVP) en cas d’ECG typique.
- Absence de cardiopathie (structurale) ou de conditions pouvant reproduire un ECG du SB.
Évaluer le risque de mort subite
Le but ultime de la prise en charge est la prévention de la mort subite. Toute la difficulté consiste à stratifier ce risque pour un rapport bénéfice/risque optimal dans cette population jeune. L’appréciation du risque rythmique de chaque patient est rendu difficile par la disparité des taux d’évènements selon les études : moins de 1 % à 34 ± 52 mois dans la série d’Eckardt et 8 % à 27 ± 29 mois chez les frères Brugada.
Facteurs de risque de mort subite
Les facteurs de risque (FDR) de mort subite du syndrome de Brugada sont, outre une mort subite ressuscitée, une syncope inexpliquée, le type 1 spontané (dérivations classiques ou hautes), l’histoire familiale de mort subite, le déclenchement d’une TV polymorphe ou FV lors de la SVP.
Importance de chaque FDR
– La mort subite ressuscitée a une « chance » sur deux de récidiver dans les 5 ans.
– La syncope inexpliquée chez un sujet avec ECG spontané de type 1 multiplie le risque d’arrêt cardiaque par 6 par rapport à un sujet avec le même ECG mais sans syncope. Ce FDR bascule le sujet dans la catégorie de patient symptomatique avec pour corollaire l’indication d’implanter un DAI (class IIa). La difficulté provient du fait que ces patients font aussi des malaises vagaux dont il faut démêler dans la symptomatologie ce qui est vraiment vagal des syncopes arythmiques.
– L’ECG dit de type 1 est le seul aspect diagnostique et prédictif de mort subite du SB. La forme spontanée (dérivations classiques, hautes ou inférieures) a un pronostic plus péjoratif que le type 1 induit par les tests pharmacologiques.
– L’histoire familiale est un FDR mal codifié. Il n’existe pas de données claires permettant de conclure que l’histoire familiale est prédictive de mort subite chez les autres membres de la famille. Toutefois il est difficile de ne pas en tenir compte. A contrario, chez un sujet avec le type 1 spontané, l’absence de mort subite familiale ne réduit pas son risque intrinsèque.
– Le rôle de la stimulation ventriculaire programmée est très débattu avec deux courants antagonistes : les frères Brugada et coll sont en faveur de cet examen avec des VPP et VPN respectivement à 23 et 93 %. S. Priori et coll opposent le faible taux d’arythmie dans le suivi, que le test soit positif ou non. Les premiers arguent de l’aspect atypique des ECG de certains patients et de la faible durée de suivi des autres études, qui cependant commencent à dépasser 5 ans, et les seconds d’un biais de sélection des patients, les plus graves étant recrutés préférentiellement par l’équipe Brugada. Ce dernier point de vue semble convaincre la plupart des équipes de recherche et les récentes recommandations européennes et nord-américaines ont dès lors relégué la SVP au second plan dans la prise en charge des sujets asymptomatiques dits à haut risque (class IIb). C’est le suivi à plus long terme des tests pratiqués sur des patients avec un aspect typique qui permettront de trancher la controverse.
– La mutation génétique (SCN5A) n’a aucune valeur pronostique. Toutefois, l’analyse génétique apporte un élément diagnostic supplémentaire et donc utile pour le suivi longitudinal des patients asymptomatiques.
Traitement du syndrome de Brugada
Traitement médicamenteux
– La quinidine pourrait être préconisée dans le traitement de l’orage rythmique du SB, et dans la prévention des récidives chez des patients implantés. Ceci doit être confirmé par les études en cours.
– L’isoprotérenol en perfusion est conseillée pour traiter l’orage rythmique.
Défibrillateur automatique implantable (DAI)
Le DAI reste le seul traitement ayant fait ses preuves dans la prévention de la mort subite. Toutefois, le faible taux d’évènements rapporté par l’analyse des mémoires des DAI implantés avec un recul de plus d’une dizaine d’années associé à un taux de chocs inappropriés et de fractures de sondes non négligeables imposent de bien cerner le rapport bénéfice/risque de ce traitement chez des sujets jeunes dont la « qualité de vie » est considérablement altérée en cas de choc inapproprié ou autre complication.
Prévention secondaire
- Le DAI s’impose en cas de mort subite récupérée, quel qu’en soit le mécanisme.
- Il est également conseillé en cas de syncope inexpliquée lorsque l’ECG est typique.
- Si le type 1 est démasqué uniquement après un test pharmacologique, la syncope revêt un caractère pronostique moins péjoratif et les recommandations actuelles conseillent plutôt un suivi (monitoring ECG) à la recherche d’un type 1 spontané.
Prévention primaire
La prévention primaire des sujets sans antécédent de syncope ou mort subite, et donc considérés comme asymptomatiques, est en revanche beaucoup plus difficile à proposer, puisque les facteurs de risques restent flous et controversées.
Quoi qu’il en soit, les sujets asymptomatiques, même à haut risque (type 1 spontané, ATCD familial de mort subite, SVP positive, FA, QRS larges), ne relèvent pas d’un DAI selon les dernières recommandations.
Dès lors, il semble inutile de proposer une SVP (qui ne devrait pas déboucher sur un DAI) à un Brugada asymptomatique, même avec un type 1 spontané.
Syndrome de Brugada et sport
Aucun cas de mort subite à l’effort n’est décrit dans cette affection. Toutefois, conceptuellement l’à-coup vagal post effort physique fait craindre l’apparition du sus-décalage type 1 initiateur de l’arythmie ventriculaire. Il est donc admis de déconseiller le sport en cas de SB documenté et non appareillé. Mais cette précaution ne repose sur aucune certitude scientifique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :