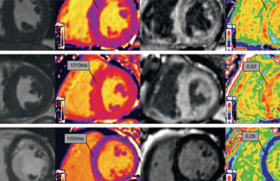
Cardiomyopathies
Publié le 27 oct 2009Lecture 10 min
D. KHATRI, F. EL LOUALI, N.I. ETTALIBI, A. TAMDY, N. ISMAILI, A. ABOURAZZAK, J. ZARZUR, M. ARHARBI, Service de cardiologie B, CHU Ibn Sina, Rabat

Les myxomes cardiaques constituent la forme la plus fréquente des tumeurs cardiopéricardiques. La symptomatologie est souvent polymorphe et non spécifique. Le diagnostic a largement bénéficié de l’apport de l’échocardiographie transthoracique et transœsophagienne. Les progrès de la chirurgie cardiaque permettent une résection plus complète de ces tumeurs. La guérison totale et définitive est possible.
L’analyse de 10 observations ainsi qu’une revue de la littérature permettront de rappeler la fréquence des myxomes cardiaques, d’en discuter les différentes manifestations cliniques, radiologiques et électriques et de souligner l’apport capital des techniques d’imagerie cardiaque non invasives dans l’établissement du diagnostic.
Matériel et méthode
Il s’agit d’une étude rétrospective portant sur une série de 10 patients atteints de myxomes cardiaques colligée au service de cardiologie B du CHU Ibn Sina, sur une période de 12 ans entre 1995 à 2006. Les dossiers médicaux ont été analysés en précisant :
- les données épidémiologiques, cliniques, électriques et radiologiques,
- les caractéristiques tumorales précisées par l’échocardiographie transthoracique ainsi que d’autres examens complémentaires,
- les modalités thérapeutiques et les différents aspects évolutifs.
Résultats
Notre série comporte 10 cas de myxomes, dont 6 femmes (60 %) et 4 hommes (40 %). L’âge moyen était de 40 ± 10 ans, avec des extrêmes allant de 14 à 66 ans. Le délai moyen du diagnostic de la tumeur, par rapport à au début de la symptomatologie, était de 10 mois avec des extrêmes de 15 jours à 5 ans.
Le mode de révélation était variable. La dyspnée d’effort était le symptôme le plus fréquent, rencontré chez 5 patients, suivi par les palpitations chez 4 malades et la douleur thoracique. Deux malades ont présenté des accidents emboliques à type d’accident vasculaire cérébral ischémique (cas n° 1) et une ischémie du membre supérieur gauche (cas n° 5). Un patient (cas n° 10) était asymptomatique sur le plan cardiovasculaire. La découverte a été fortuite au cours d’un bilan pré-anesthésique pour cholécystectomie (figure 1).
L’examen cardiovasculaire était normal chez un patient. Un tableau de rétrécissement mitral a été retrouvé chez 6 patients, une insuffisance mitrale chez un patient et une insuffisance tricuspidienne isolée chez 2 patients. On a noté chez un patient des signes d’épanchement péricardique. Trois patients présentaient des signes d’insuffisance cardiaque droite.
Figure 1. Circonstances de découverte des myxomes.
Par ailleurs, l’examen somatique trouvait : une hémiplégie droite avec aphasie dans un cas (cas n° 1) et une abolition du pouls radial gauche avec hypoesthésie et parésie de ce membre dans un cas (cas n° 5).
Sur le plan électrique, 7 patients étaient en rythme régulier sinusal alors que 3 étaient en arythmie complète par fibrillation auriculaire. Une hypertrophie auriculaire gauche a été notée chez 3 malades et une hypertrophie ventriculaire droite chez un patient. La radiographie pulmonaire a mis en évidence une cardiomégalie chez 9 patients avec un index cardiothoracique moyen de 0,57 ± 0,05.
L’échocardiographie transthoracique a été réalisée chez tous nos patients. Elle a mis en évidence une masse cardiaque dans tout les cas. Le siège de la masse était très variable. Les myxomes étaient localisés dans 8 cas dans l’oreillette gauche et implantés sur le septum interauriculaire, contre un seul cas dans l’oreillette droite et un cas dans le ventricule droit. Les dimensions variaient entre 15 et 80 mm de grand axe (figures 2 et 3). Aucune forme multiple n’a été observée. Des anomalies ont été notées au Doppler couleur, à type d’insuffisance mitrale dans 3 cas (cas n° 2, 4, 6) et d’insuffisance tricuspide avec ou sans HTAP dans 4 cas (cas n° 4, 6, 7, 10). Un rétrécissement mitral organique associé (du à l’interaction de la tumeur avec jeu valvaire) a été relevé dans un cas (cas n° 2).
Figure 2. Image échocardiographique en coupe parasternale grand axe montrnat une masse échogéne occupant l’OG (cas n° 8).
Figure 3. Image échocardiographique en coupe parasternale grand axe montrant le prolapsus de la masse à travers la valve mitrale en systole (cas n°8).
Une échocardiographie transœsophagienne a été réalisée chez un seul malade (cas n° 1). Elle a confirmé, d’une part, la base d’implantation de la tumeur au niveau du septum interauriculaire, à quelques millimètres de l’anneau mitral, et d’autre part, l’intégrité de l’appareil valvulaire mitral.
Le bilan a été complété par un cathétérisme cardiaque chez 2 patients (cas n° 3 et 10). La coronarographie et la mesure des pressions de remplissage étaient normales chez les 2 patients. La ventriculographie a montré une image de soustraction au niveau de l’OD au cours de la systole dans le cas n° 10.
Sur le plan thérapeutique, les 8 myxomes de l’OG ont été réséqués de façon complète sous circulation extracorporelle après atriotomie droite et septotomie. La résection a été complétée par une plastie mitrale chez 4 de ces patients. Le myxome de l’OD (cas n° 9) a été réséqué après atriotomie droite sous CEC. Le geste a été complété par une annuloplastie tricuspide. La résection du myxome du VD (cas n° 10) a été effectuée sous CEC par atriotomie droite complétée par une artériotomie pulmonaire. La tumeur s’implantait au niveau de la partie haute du septum interventriculaire et comportait deux prolongements, l’un à travers l’orifice tricuspide vers l’OD et l’autre à travers l’orifice pulmonaire vers les deux artères pulmonaires. La résection a été incomplète, la tumeur étant inextirpable.
L’évolution à court et à long terme a été favorable sauf pour le cas n° 3 dont les suites opératoires ont été marquées par une septicémie à staphylocoque doré, une insuffisance rénale et un infarctus postéro-inférieur. Le patient a été transféré au service de néphrologie, après stabilisation de son état cardiaque sous traitement médicamenteux optimal.
Le cas n° 10 (myxome du VD) a présenté 4 mois après l’intervention une symptomatologie clinique faite de signes généraux à type d’AEG, fièvre, frissons, amaigrissement avec à l’examen des signes d’ICD. L’échocardiographie a mis en évidence deux masses tumorales pédiculées accolées à la face septale de la chambre de chasse du ventricule droit dilaté, mobiles, se prolabant dans l’oreillette droite, et une tumeur adhérente à la paroi interne de l’artère pulmonaire au-dessus des sigmoïdes. Une relecture des lames de la pièce opératoire a conclu à une biopsie limite entre le myxome et myxosarcome.
Discussion
Le myxome cardiaque est la plus fréquente des tumeurs cardiopéricardiques primitives bénignes. Il représente 52,6 % des cas dans notre série, 63 % dans la série de Meng(1) et 91 % dans la série de Centofanti(2). Nous avons remarqué une légère prédominance féminine (60 %), de même que Denguir (60%)(3) et Yoon (93 %)(4). Nos malades sont plus jeunes, avec un âge moyen de 40 ans (14 à 66 ans). Dans l’étude de Denguir, l’âge moyen était de 49 ans (11 à 70 ans)(3) et l’étude de Yoon âge moyen de 55 ans (25-83 ans)(4).
Sur le plan histologique
Le myxome est une tumeur carcinologiquement bénigne, dérivée de reliquats vestigiaux embryonnaires sous-endocardiques « pluripotents »(5). Dans la littérature, 75 à 90 % des myxomes sont de localisation auriculaire gauche(2,6) (80 % dans notre série). Dans l’immense majorité des cas, la tumeur est implantée sur le septum interauriculaire, au niveau de la fosse ovale ou de ses bords. Lorsque l’insertion n’est pas septale, elle se fait par ordre décroissant sur les faces postérieure et antérieure de l’oreillette gauche ou dans l’auricule gauche(2,6). Nous avons relevé un cas myxome de l’OD (10 % dans notre série). Cette localisation est décrite entre 15 à 20% des cas environ(2,6). La localisation ventriculaire est plus rare (2% des myxomes pour Meng et al(1) et 2 à 4 % pour Reynen et al(7)). Les myxomes à localisations multiples dans une même cavité ou dans plusieurs cavités cardiaques en même temps, sont possibles(3).
Données cliniques
Le délai moyen entre les premiers symptômes et le diagnostic du myxome est de 16 mois en moyenne pour ST John Sutton(8) (12 mois dans notre série). Les données cliniques de notre étude sont comparables à celles de la littérature. Une dyspnée a été constatée dans 50 à 80 % des cas(9), une douleur thoracique chez 10 à 20 % des patients(2). La fréquence des signes généraux varie de 13 à 45,7 %(1) (30 % de nos patients). Lakhdahr rapporte même un cas de myxome de l’oreillette droite révélé par un trouble de l’humeur ayant amené la patiente à consulter en psychiatrie(10).
Les accidents emboliques révèlent le myxome dans 30 à 40 % des cas(7,8,11,12). Il peut s’agir de matériel thrombotique détaché de la surface du myxome, d’une frange du myxome, voire du myxome entier rompu au niveau de son pédicule. Environ la moitié des embolies concernent les artères cérébrales(13), y compris rétiniennes(14). Les accidents emboliques ont été relevés dans 2 cas dans notre série (20 %) et ont concerné l’artère sylvienne gauche (cas n° 1) et l’artère humérale gauche (cas n° 5). Les formes asymptomatiques représentent 10 % dans notre série (1 et 15 % selon les auteurs), et concernent les myxomes de petite taille et/ou siégeant loin des structures valvulaires(2,15).
L’élément sémiologique capital est la variation de l’auscultation dans le temps et surtout en fonction de la position du malade(3). Les myxomes de l’OG peuvent simuler une auscultation de rétrécissement mitral, c’était le cas pour 6 de nos patients. Par ailleurs, un souffle protodiastolique entendu 80 à 150 ms après le deuxième bruit (appelé tumor plop) est retrouvé chez un tiers des patients porteurs de myxomes(7).
Bilan d’imagerie
Selon les données de la littérature, l’ECG et la radiographie pulmonaire ne montrent pas de signes spécifiques. Le diagnostic positif du myxome repose essentiellement sur l’ETT qui constitue l’examen clé avec une sensibilité de 93,3 % et une spécificité de 96,8 %(16). L’ETT a permis le diagnostic chez tous nos patients. Classiquement, l’échocardiographie transthoracique révèle une masse mobile reliée au septum interauriculaire par un fin pédicule(17). Les myxomes ont généralement une échogénicité hétérogène avec parfois des calcifications. L’élément diagnostique le plus important est sa localisation au niveau de l’oreillette gauche et sa naissance à partir de la partie moyenne du septum interauriculaire(18), ce qui permet de le différencier des autres masses intracardiaques (thrombus) ; 90 % des myxomes de notre étude prenaient naissance au niveau du septum interauriculaire, dont 8 au niveau de l’OG et 1 au niveau de l’OD.
L’ETO permet une meilleure analyse de la base d’implantation de la tumeur, de ses rapports avec la valve mitrale, une étude morphologique précise des cavités cardiaques, en particulier de l’OD(19). Dans notre travail, les renseignements fournis par l’ETT étaient suffisants pour poser le diagnostic ; nous n’avons eu recours à l’ETO qu’une seule fois.
L’IRM et CT scan permettent d’identifier des tumeurs de petite taille (entre 0,5 et 1 cm), de déterminer la composition tissulaire tumorale (tissue solide, liquide, hémorragique ou nécrosé)(20-22) et de visualiser la base d’insertion de la tumeur(23).
Traitement
La résection tumorale doit être complète emportant le myxome, son pédicule et sa base d’implantation, le tout avec un minimum de manipulation afin d’éviter toute fragmentation et tout risque de migration embolique(3). Il existe encore des controverses en ce qui concerne l’étendue de la résection nécessaire pour prévenir une récidive du myxome. Bortolotti et al.(24) recommandent de :
– réséquer la base d’implantation avec une large pastille du septum sur toute son épaisseur pour les myxomes implantés autour de la fosse ovale. Le défect septal ainsi créé sera fermé par un patch ;
– réséquer la base d’implantation avec l’endocarde et un peu du myocarde sous-jacent, cela est valable pour toute zone d’attache ou d’adhérence tumorale avec les parois.
Jones et al.(25) considèrent que l’approche chirurgicale biatriale des myxomes de l’oreillette permet une manipulation minimale de la tumeur et assure une exposition adéquate pour une résection complète de la tumeur avec une inspection des quatre cavités cardiaques. D’autres considèrent que l’exposition de la tumeur assurée par l’atriotomie gauche est suffisante pour une résection correcte et avec un faible taux de récurrence(2).
Pour les 8 cas de myxomes de l’OG, une atriotomie droite et une septotomie ont assuré une exposition suffisante et une résection complète. Le myxome de l’OD a été abordé par atriotomie droite.
Les myxomes des ventricules sont exceptionnels, la résection chirurgicale complète est difficile ; elle se fait par atriotomie si le myxome siège près de la valve auriculo-ventriculaire, sinon à travers les gros vaisseaux pour ceux qui siégent dans la chambre de chasse(3). Le myxome du VD de notre série a été réséqué de manière incomplète par atriotomie droite et artériectomie pulmonaire.
Pronostic
La mortalité précoce est inférieure à 5 %(26, 27). Dans notre étude, la mortalité hospitalière est nulle. Le risque de récidive est de 1 à 4 % en cas de myxome sporadique. Il est plus élevé dans les formes familiales, multifocales et le complexe de Carney (syndrome familial associant des lésions cutanées pigmentées, des myxomes cutanées et des tumeurs endocrines)(7,28-29). Plusieurs hypothèses ont été émises pour expliquer la récidive tumorale : la résection chirurgicale incomplète, la dissémination peropératoire de matériel tumoral, la transformation maligne de la tumeur ou encore la multifocalité de la genèse des myxomes(28,30,31). Cependant, pour les formes sporadiques, la résection incomplète est la raison évoquée(28,30,31). La diminution de la fréquence des récurrences, dans les séries récentes, est probablement due aux progrès des techniques et des équipements chirurgicaux ainsi que de l’expérience des chirurgiens(7). Une surveillance échocardiographique semestrielle de tout patient opéré pour myxome cardiaque est recommandée(31).
Le myxome du VD (cas n° 10) a récidivé seulement 4 mois après l’intervention, au niveau du VD et de la paroi interne de l’artère pulmonaire. La relecture des lames a retenu le diagnostic de myxome bénin. Il s’agit, en effet des localisations pour lesquelles la résection chirurgicale était incomplète compte tenu du risque de délabrement.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :