Publié le 12 juin 2007Lecture 6 min
Nouveautés en transplantation cardiaque
S. VARNOUS et I. GANDJBAKHCH, Groupe hospitalier Pitié-Salpêtrière, Paris
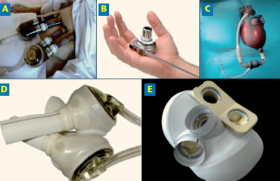
La transplantation cardiaque est actuellement le traitement de référence de l’insuffisance cardiaque terminale. Chaque année en France sont réalisées approximativement 300 greffes cardiaques et 3 500 dans le monde (figure 1). Notre expérience porte sur plus de 1 500 greffes effectuées depuis 1968.
Les nouveautés en transplantation cardiaque concernent le profil des patients, la nouvelle génération des immunosuppresseurs et la meilleure connaissance des complications et du suivi des patients.
Figure 1. Évolution des patients en attente de greffe en France entre 2000 et 2006.
Indication de la transplantation cardiaque
L’indication de transplantation cardiaque est posée quand la survie prévisible est inférieure à 1 an, sous traitement médical le plus approprié comportant les bêtabloquants, la resynchronisation, etc. Ce stade est déterminé par un certain nombre de paramètres classiques d’évaluation d’insuffisance cardiaque (IC) qui sont la fraction d’éjection et le volume télédiastolique du ventricule gauche, le stade fonctionnel NYHA et la capacité cardiopulmonaire à l’effort (VO2 max).
Une fois l’indication de la transplantation cardiaque posée, un bilan exhaustif est réalisé pour :
- éliminer une éventuelle contre-indication à la greffe (pathologie cancéreuse évolutive) ;
- identifier les conditions de la réalisation de la transplantation pour prendre des mesures théra-peutiques nécessaires en per- et postopératoire (résistances pulmonaires, présence d’anticorps lymphocytotoxiques, etc.) ;
- évaluer l’état des autres viscères (poumon, foie, rein, etc.). Ce bilan est nécessairement abrégé chez les patients très gravement atteints.
Une fois inscrits sur la liste nationale de transplantation, les patients sont régulièrement suivis en Centre de transplantation en plus de leur suivi cardiologique habituel.
L’origine de la cardiopathie, dans une étude rétrospective (150 patients transplantés dans notre centre au cours des 2 dernières années), était une cardiomyopathie dilatée à coronaires normales dans 49,3 % des cas et une cardiopathie ischémique dans 32 %. Dans cette même population, le pic de VO2 moyenne était de 9,4 ml/ kg/min. La FEVG moyenne était de 20 %. Vingt pourcent des patients avaient bénéficié de la mise en place d’un défibrillateur et d’un stimulateur multisite ; 13 % des patients étaient sous assistance circulatoire mécanique au moment de la greffe.
L’âge du receveur et du donneur a augmenté de 10 ans en moyenne au cours des 2 dernières décennies. Il est possible de proposer une transplantation cardiaque à 70 ans, voire plus si aucune autre co-morbidité n’est associée.
Traitement immunosuppresseur
À côté des molécules classiques – sérum antilymphocytaire, corticoïdes, ciclosporine et azathioprine — sont apparues de nouvelles générations d’immunosuppresseurs — tacrolimus, mycophénolate mofétil –, et les inhibiteurs de la prolifération du signal qui offrent la possiblilité d’une polychimiothérapie à la carte adaptée à chaque patient en vue d’une efficacité maximale et le minimum d’effets secondaires.
Chez les patients immunisés, porteurs d’anticorps anti-HLA, chez qui la probabilité d’être transplantés était faible, l’utilisation des immunoglobulines et des échanges plasmatiques permet une augmentation significative de la possibilité de la réalisation de la greffe.
Résultats
Après la réalisation de la transplantation, le patient greffé reste hospitalisé en moyenne 15 à 30 jours. Il est ensuite suivi dans le Centre de transplantation à une cadence rapprochée dans les premiers mois. Après la 1re année, une consultation tous les 2 à 3 mois est suffisante, sauf événement intercurrent.
Survie après la greffe
Le taux de survie à 1 an après la greffe cardiaque est de 80 %, selon des résultats des études monocentriques et des registres (figure 2). Ensuite, le taux de mortalité est de l’ordre de 4 % par an après la 1re année. La survie à 5 et 10 ans est respectivement de 70 et 50 %. Les causes de mortalité à long terme sont la maladie coronaire du greffon et/ou la dysfonction tardive du greffon (30 %), les cancers incluant le syndrome lymphoprolifératif post-transplantation (24 %) et les infections (10 %).
Figure 2. Courbe de survie des patients transplantés à la Pitié-Salpêtrière entre 2004 et 2005 (n = 150).
Complications après la greffe cardiaque
Les complications en post-transplantation cardiaque peuvent être réparties en deux groupes :
- liées au greffon : rejet aigu et rejet chronique ;
- liées au traitement immunosuppresseur : infections, cancers, insuffisance rénale, hypertension artérielle, dyslipidémie et complications osseuses.
Rejet aigu
Le rejet est défini par l’ensemble des réactions inflammatoires locales et générales développées par le système immunitaire de l’hôte à l’égard d’un greffon. Cette réaction pourrait aboutir à la destruction complète du greffon en l’absence du traitement adéquat. L’incidence du rejet aigu a diminué au cours des 10 dernières années ; seulement 5 % de rejets de haut grade (> 3A) sont observés au cours de la 1re année. Cette évolution est due au traitement immunosuppresseur à la carte.
La biopsie endomyocardique est l’examen de référence pour confirmer le diagnostic du rejet. La majorité des rejets diagnostiqués au cours de la 1re année postgreffe sont des rejets infracliniques découverts par la réalisation de biopsies systématiques. Les examens non invasifs actuellement utilisés, comme l’écho-Doppler cardiaque avec notamment le Doppler tissulaire et l’IRM cardiaque permettent d’évoquer le diagnostic de rejet sans qu’ils puissent le confirmer. Concernant les marqueurs biologiques comme le NT-proBNP et les peptides natriurétiques, les résultats des différentes études dans le diagnostic de rejet sont controversés.
Rejet chronique ou maladie coronaire du greffon
La maladie coronaire du greffon (MCG) est la 1re cause de morbi-mortalité à moyen et long termes après la transplantation cardiaque. Son incidence est estimée à 40 % à 5 ans. La physiopathologie de la MCG est multifactorielle faisant intervenir des facteurs immunologiques et non immunologiques. Le nombre de rejets aigus, l’infection à CMV, l’âge du donneur, la durée d’ischémie du greffon, la dyslipidémie, l’hypertension artérielle et le tabagisme sont considérés comme des facteurs de risque de MCG.
La majorité des patients ne présentent pas la symptomatologie de l’angine de poitrine en raison de la dénervation cardiaque. Si la coronarographie est l’examen de référence, complétée par l’échographie endocoronaire (IVUS) si nécessaire, la nouveauté est le scanner multibarrette dans le dépistage de MCG avec une sensibilité de 83 % et une spécificité de 95 %. Cet examen non invasif pourrait remplacer, dans un avenir proche, la coronarographie de dépistage itérative, chez le transplanté cardiaque.
La fréquence et la gravité de la MCG exigent des mesures :
- dans la prévention, même partielle, obtenue par la prescription des statines et des inhibiteurs de la prolifération du signal, d’une part, et le meilleur contrôle des facteurs de risque d’autre part ;
- une fois installée, selon la localisation et le type des lésions, on peut proposer une angioplastie coronaire (385 ont été réalisées dans notre série), et plus rarement des pontages coronaires (6 cas dans notre série). La retransplantation cardiaque peut être envisagée chez les patients avec une atteinte coronaire sévère non revascularisable, qui sont symptomatiques.
Complications liées au traitement immunosuppresseur
Les infections, en particulier les infections opportunistes dues ou favorisées par l’immunosuppression, constituent également une cause importante de morbi-mortalité postgreffe. Les infections postopératoires surviennent habituellement dans le 1er mois postgreffe et sont surtout d’origine bactérienne.
Les infections postgreffe tardives regroupent les infections opportunistes (CMV, Pneumocystis carinii, Aspergillus, Toxoplasma, etc.) survenant plutôt pendant les 6 premiers mois. Une meilleure prévention, le diagnostic plus précoce et les progrès dans le domaine thérapeutique ont permis de mieux contrôler ces infections.
L’incidence des cancers est augmentée après la greffe. Le syndrome lymphoprolifératif post-transplantation est souvent EBV-dépendant. Le risque de survenue des cancers d’organes solides est multiplié par trois. L’incidence des cancers de la peau sans gravité vitale est de l’ordre de 10 % dans les 10 premières années.
Les autres complications sont souvent le diabète cortico-induit, l’hypertension artérielle (plus de 60 % des patients sont traités après greffe), la dyslipidémie, l’insuffisance rénale aboutissant à l’hémodialyse dans 10 % des cas à 10 ans et les complications ostéoarticulaires.
Qualité de vie des patients transplantés cardiaques
Plus de 80 % des patients ne se considèrent pas limités dans leur activité ; cependant 35 à 40 % environ seulement reprennent une activité professionnelle. Entre 10 et 15 % des patients transplantés sont retraités d’après l’analyse des registres. Le taux de réhospitalisations est de l’ordre de 30 % au cours de la 1re année et majoritairement pour problèmes infectieux.
En conclusion
La transplantation cardiaque est le seul traitement efficace des patients en insuffisance cardiaque réfractaire au traitement médical.
Les taux de survie postgreffe sont de 80 et 50 % respectivement à 1 et 10 ans avec l’amélioration considérable de la qualité de vie, malgré les contraintes du traitement immunosuppresseur.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :