Rythmologie et rythmo interventionnelle
Publié le 07 avr 2009Lecture 5 min
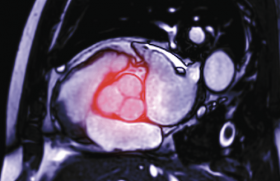
Pourquoi l'oreillette fibrille-t-elle ?
J.-F. LECLERCQ et P. ATTUEL, Paris et Le Chesnay

En fait, pour plusieurs raisons… Car s’il n’y en avait qu’une, ce serait trop simple et enlèverait tout le charme de notre discipline.
Parce qu’elle est trop grosse
C’est la notion de masse critique. L’oreillette du petit mammifère ne fibrille jamais, celle de l’enfant non plus, quelles que soient les méchancetés qu’on puisse lui faire. En revanche, à partir de la taille d’un bon gros chien, il suffit de la stimuler vite et longtemps et elle fibrille. Par ailleurs, on voit beaucoup plus de fibrillation auriculaire (FA) sur cœur sain chez le colosse que chez la petite bonne femme, pour la même raison : plus il y a de tissu atrial, plus il a de chances de fibriller. Ce qui compte c’est donc la taille du thorax et partant du massif auriculaire : plus il sera grand, plus il y aura de possibilité de « vaguelettes » de FA. Par ailleurs, si on laisse un patient en FA, son oreillette grossit tandis que si on le remet en rythme sinusal et qu’il veut bien y rester, elle diminue de taille. Enfin, la taille de l’OG est prédictive de la survenue de FA dans une étude de population.
Parce qu’elle a une structure trop complexe
Il suffit de regarder les deux oreillettes et de les comparer aux deux ventricules pour comprendre que le cheminement de l’influx électrique ne va pas pouvoir se dérouler de façon homogène : d’un côté, de simples sacs avec une entrée et une sortie (les orifices valvulaires), de l’autre des cavités pleines de trous (les veines caves, le sinus coronaire, les orifices valvulaires et les veines pulmonaires) et de recoins (les auricules) dont il faudra faire le tour. Il y a une plus grande complexité des fibres musculaires autour des trous ; elles se groupent en faisceaux préférentiels (le faisceau de Bachmann, la crista terminalis). Comme il n’y a pas de tissu de conduction spécialisé, l’influx a du mal à dépolariser le tissu. Il y a en plus des fibres aberrantes qui s’invaginent dans les veines pulmonaires où elles donnent des extrasystoles, et des résidus embryologiques comme le ligament ou la veine de Marshall, dont l’importance clinique semble grande.
Tout cela est responsable d’une anisotropie de la conduction intra-atriale, et les troubles de conduction font survenir la FA.
Parce qu’elle n’est pas stable électriquement
Le potentiel d’action de la cellule auriculaire est court, avec une plasticité électrophysiologique accrue. Cela explique le phénomène de l’arythmie arythmogène : plus une oreillette fibrille, plus elle aura de facilités à le faire à nouveau. C’est le remodelage électrique : raccourcissement des périodes réfractaires, inadaptation à la fréquence et augmentation des temps de conduction. Ceci fait le lit de la récidive si une extrasystole (le trigger) survient sur ce tissu hypervulnérable (le substrat). Il n’est même pas besoin d’une tachycardie soutenue : la simple irrégularité du bigéminisme suffit pour qu’elle fibrille. C’est cette vulnérabilité, combinaison d’un trouble de la réfractorité et de la propagation de l’influx, que l’on étudie par exemple dans les AVC inexpliqués pour faire le diagnostic de FA paroxystique asymptomatique.
Parce qu’elle est très innervée
Le système nerveux autonome a de très nombreuses terminaisons au niveau atrial avec 4 ganglions parasympathiques au contact des oreillettes. Toute hypertonie vagale va raccourcir les périodes réfractaires et ce, de façon inhomogène, maximale aux alentours de ces 4 ganglions. La coïncidence spatiale entre ces terminaisons nerveuses et les « pivot points » ou les potentiels fragmentés est frappante. Alors on comprend ce que nous avons décrit sous le nom d’arythmie auriculaire vagale, on comprend que la pratique sportive, surtout des sports d’endurance, augmente le risque de FA, on comprend qu’un tonus vagal augmenté augmente le risque de rechute après cardioversion, on comprend qu’un des intérêts de l’ablation de l’OG est la dénervation vagale, on comprend que, peut être, Churchill avait raison…
Parce qu’elle vieillit…
Et donc qu’elle perd des cellules fonctionnelles, en particulier le nœud sinusal. Or, celui-ci a un rôle de « leader » de la dépolarisation du massif atrial. Il protège de la FA car il organise le trajet de l’influx de façon optimale. Dès lors, si le sinus est défaillant, la FA est quasiment inéluctable. D’où les seules indications de stimulation et/ou resynchronisation atriale qui restent pour prévenir la FA dans la maladie rythmique auriculaire. Nous perdons beaucoup de cellules atriales au fil du temps, et il se produit un remodelage tissulaire. Ce n’est rien d’autre que la diminution du nombre de « gap junctions » fonctionnelles qui font passer l’influx d’une cellule à l’autre, grâce aux connexines. Les cellules atriales perdues sont alors remplacées par de la fibrose, ce que montre bien l’excrétion accrue des produits de catabolisme du collagène dans la FA, lorsqu’elle devient persistante ou surtout permanente. Donc, la FA paroxystique fait survenir la FA permanente, et le risque de FA augmente avec l’âge de façon exponentielle, le nombre de patients avec FA va donc en augmentant. Cest notre avenir : si le malade meurt du ventricule, le rythmologue, lui, vit de l’oreillette… D’autant que l’espérance de vie des patients est bonne quand la FA est bien contrôlée et bien anticoagulée.
Parce que le ventricule gauche est trop rigide
En épidémiologie, les deux facteurs échographiques prédictifs de FA au sein d’une population sont, certes, la taille de l’OG, mais aussi l’épaisseur du VG. La PtdVG est augmentée dans la FA paroxystique, les séries importantes de FA retrouvent de l’ordre de 50 %, voire 60 % d’hypertendus comme dans l’EuroHeart Survey, et les études de l’écho dans la FA paroxystique retrouvent un trouble de compliance du VG. Il semble de plus en plus évident que la FA idiopathique est une maladie du VG, plus que de l’oreillette elle-même. C’est lui le responsable du « stretch » exercé sur la paroi atriale : c’est parce que la paroi du VG est trop rigide que l’oreillette gauche souffre, se dilate et que son tissu s’altère plus vite avec l’âge.
Ce phénomène est à son apogée dans la CMH où la FA est fréquente et mal tolérée. On comprend alors l’effet bénéfique des IEC et des sartans qui préviennent davantage l’apparition de la FA que les autres antihypertenseurs, probablement parce qu’ils sont plus efficaces pour diminuer la rigidité ventriculaire. De là à les utiliser dans la FA paroxystique ou persistante idiopathique, il y a un pas que d’aucuns ont déjà franchi, bien sûr en association avec des antiarythmiques classiques.
En pratique
Telles sont les principales raisons pour lesquelles une oreillette présumée normale peut fibriller. On voit les pistes thérapeutiques qui en découlent : prévenir les troubles de compliance ventriculaire, éviter l’hypertonie vagale chronique liée au sport, trouver un antiarythmique qui améliore la stabilité de ce tissu sans altérer celle du ventricule, et peut-être expliquer à la population qu’il y a intérêt à manger moins.
Pour le reste, combler les trous de l’oreillette ou améliorer la conduction, on ne sait pas faire, mais on peut détruire les zones de troubles de conduction localisées qui sont arythmogènes, pour entraver l’évolution de la FA persistante vers la FA chronique.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :