Rythmologie et rythmo interventionnelle
Publié le 04 oct 2011Lecture 12 min
Recommandations : la prise en charge de la fibrillation atriale
F. DELAHAYE, A.-M. ANTCHOUEY, Bron
La Société européenne de cardiologie a récemment publié ses recommandations sur la prise en charge de la fibrillation atriale[1].
La FA est la plus fréquente des arythmies cardiaques soutenues, elle atteint 1 à 2 % de la population générale. Du fait du vieillissement de la population, sa prévalence va être multipliée par au moins 2,5 dans les 50 prochaines années.
La FA a des conséquences fréquentes et sévères (tableau 1). La prévention de ces conséquences est l’objectif thérapeutique principal de la prise en charge de la FA.
De nombreuses situations peuvent causer ou favoriser la progression de la FA, et doivent donc être recherchées et prises en charge : HTA, IC symptomatique (classe NYHA II à IV), y compris la cardiomyopathie due à la tachycardie, valvulopathies, cardiomyopathies, communication interatriale et autres cardiopathies congénitales, maladie coronaire, dysfonction thyroïdienne, obésité, diabète, BPCO et apnée du sommeil, néphropathies chroniques.
Diagnostic et prise en charge initiale
Une anamnèse approfondie doit être obtenue du patient ayant une FA suspectée ou connue :
• La FC pendant l’épisode est-elle régulière ou irrégulière ?
• Y a-t-il des facteurs précipitants tels que effort, émotion, consommation d’alcool ?
• Les symptômes pendant l’épisode sont-ils modérés ou sévères ? On peut utiliser le score de l’EHRA :
- I : « Aucun symptôme » ;
- II : « Symptômes légers » ; les activités quotidiennes normales ne sont pas affectées ;
- III : « Symptômes sévères » ; les activités quotidiennes normales sont affectées ;
- IV : « Symptômes invalidants » ; les activités quotidiennes normales ne sont pas possibles.
• Les épisodes sont-ils fréquents ou rares, leur durée est-elle courte ou longue ?
• Y a-t-il une maladie concomitante telle que HTA, maladie coronaire, insuffisance
cardiaque, maladie vasculaire périphérique, maladie cérébro-vasculaire, AVC, diabète, maladie pulmonaire chronique ?
• Y a-t-il une consommation excessive d’alcool ?
• Y a-t-il des antécédents familiaux de FA ?
La documentation de la FA (par ECG ou à partir d’un dispositif intracardiaque) est nécessaire pour confirmer le diagnostic. La FA est définie comme une arythmie cardiaque avec les caractéristiques suivantes :
• l’ECG de surface montre des intervalles RR « absolument » irréguliers, c’est-à-dire des intervalles RR qui ne suivent pas un motif répétitif ;
• il n’y a pas d’onde P distincte sur l’ECG de surface ; une activité électrique atriale apparemment régulière peut être vue dans certaines dérivations, le plus souvent dans la dérivation V1 ;
• la durée du cycle atrial (quand il est visible), c’est-à-dire l’intervalle entre deux activités atriales, est habituellement variable et < 200 ms (> 300 bpm) ; lorsqu’une FA est suspectée mais non documentée, une surveillance intensive du rythme peut être nécessaire ; le type de FA doit être spécifié ; des épisodes de FA asymptomatiques (« silencieux ») sont fréquents, même chez des patients symptomatiques.
La FA est une maladie progressive. On décrit divers types de FA :
• tout patient qui présente une FA pour la première fois est considéré comme un patient avec une FA diagnostiquée pour la première fois, quelle que soit la durée de l’arythmie ou la présence et la sévérité de symptômes liés à la FA ;
• la FA paroxystique se termine toute seule, habituellement dans les 48 heures. Bien que des paroxysmes de FA puissent durer sept jours et plus, la limite de 48 heures est importante cliniquement. Au-delà de cette durée, la probabilité de retour spontané au RS est basse et une anticoagulation doit être envisagée ;
• on parle de FA persistante quand elle dure plus de huit jours ou bien nécessite une cardioversion ;
• on parle de FA longtemps persistante lorsqu’elle dure depuis plus d’un an, lorsqu’il est décidé d’adopter une stratégie du contrôle du rythme ;
• la FA est dite permanente lorsque la présence de l’arythmie est acceptée par le patient (et par le médecin). Alors, les interventions visant à contrôler le rythme ne sont plus à l’ordre du jour. Si une stratégie de contrôle du rythme est adoptée, l’arythmie est à nouveau dénommée « FA longtemps persistante ».
La prise en charge en aigu doit se concentrer sur l’amélioration des symptômes et l’évaluation des risques associés à la FA. L’évaluation clinique doit inclure la détermination du score symptomatique de l’EHRA. La prise en charge initiale inclut :
– le contrôle de la FC ;
– l’appréciation immédiate de la nécessité d’une anticoagulation ;
– la décision de prescrire un traitement du contrôle du rythme à la prise en charge des symptômes (cela peut être réévalué plus tard) ;
– le traitement de la maladie cardiaque sous-jacente.
Habituellement, la FA progresse d’épisodes courts et rares à des épisodes plus longs et plus fréquents, et les risques liés à la FA peuvent changer au cours du temps (figure 1). Donc, après le diagnostic initial, un plan structuré de suivi doit être fait afin de maintenir un traitement efficace et de prendre en charge les complications potentielles liées à la FA ou au traitement.
Les éléments importants à envisager durant le suivi d’un patient ayant une FA sont les suivants :
– Une anticoagulation est-elle nécessaire maintenant ? De nouveaux facteurs de risque sont-ils apparus ? Ou bien, la nécessité d’une anticoagulation existe-t-elle toujours, par exemple après une cardioversion chez un patient au risque thrombo-embolique bas ?
– Les symptômes ont-ils été améliorés par le traitement ? Si ce n’est pas le cas, ne devrait-on pas envisager un autre traitement ?
– Y a-t-il des signes de proarythmie, ou un risque de proarythmie ? Si c’est le cas, ne devrait-on pas réduire la dose de l’AAR, ou changer le traitement ?
– La FA paroxystique a-t-elle progressé vers une forme persistante ou permanente, malgré l’AAR ? Si c’est le cas, ne devrait-on pas envisager un changement de traitement ?
– La stratégie de contrôle de la FC a-t-elle été efficace, au regard du score de l’EHRA et de la fonction VG ? La FC cible au repos et à l’effort a-t-elle été atteinte ?
Figure 1. Histoire « naturelle » de la FA.
La prise en charge de la FA à long terme nécessite la discussion d’un traitement antithrombotique, le contrôle de la FC, un contrôle additionnel du rythme quand cela est nécessaire, et la prise en charge de la maladie sous-jacente (figure 2).
Figure 2. Cascade de prise en charge des patients avec FA.
Traitement antithrombotique
La FA est un contributeur majeur des AVC et autres ATE. Lorsqu’un AVC survient chez un patient ayant une FA, le risque de décès et d’invalidité, et le risque de récidive d’AVC, sont plus élevés qu’en l’absence de FA. Cependant, le risque d’AVC dans la FA n’est pas homogène, et une partie cruciale de la prise en charge de la FA est l’évaluation du risque d’AVC et l’usage approprié de la thromboprophylaxie.
La catégorisation en risque bas, intermédiaire ou haut a une valeur prédictive faible, et il vaut mieux utiliser une approche basée sur le recensement des facteurs de risque.
Le score le plus simple est le score CHADS2, qui doit être utilisé en 1re intention, car il est rapide à faire et facilement mémorisable (cardiac failure, hypertension, age, diabetes, stroke [doubled] ; 1 point pour : insuffisance cardiaque, HTA, âge, diabète ; 2 points pour : AVC). Lorsque le score CHADS2 est ≥ 2, un ACO (par exemple, AVK) est recommandé, avec un INR cible entre 2,0 et 3,0, sauf contre-indication.
Lorsque le score CHADS2 est à 0 ou 1 ou lorsqu’une évaluation détaillée du risque d’AVC est indiquée, l’utilisation d’une approche basée sur les facteurs de risque complète est recommandée (tableau 2, tableau 3, figure 3).
Figure 3. Algorithme d’utilisation de l’ACO pour la prévention des AVC dans la FA.
Il y a des preuves considérables de l’efficacité de l’ACO pour la prévention des AVC, alors que l’aspirine est moins efficace que l’ACO et peut ne pas être plus sûre, notamment chez le sujet âgé. Le besoin d’une thromboprophylaxie doit faire partie de l’évaluation de la prise en charge, quel que soit le type de FA.
Les patients qui n’ont aucun facteur de risque sont à « vraiment bas risque » et peuvent ne pas avoir de traitement antithrombotique, alors que pour tous les patients avec au moins un facteur de risque, un traitement ACO peut être envisagé.
À côté de l’évaluation du risque d’AVC, il doit y avoir une évaluation du risque hémorragique, par le score HAS-BLED (tableau 4).
L’augmentation du risque thrombo-embolique lors d’une cardioversion est bien connue, et une thromboprophylaxie est recommandée, que ce soit lors d’une approche conventionnelle ou d’une stratégie guidée par l’ETO (figure 4).
Figure 4. Cardioversion d’une FA hémodynamiquement stable, rôle de l’ETO et stratégie de l’anticoagulation subséquente.
La cardioversion de la FA nécessite généralement une anticoagulation effective, précédant la cardioversion de trois semaines et continuée quatre semaines après la cardioversion. L’appréciation du besoin d’une anticoagulation à long terme doit être faite, sur la base du recensement des facteurs de risque (figure 4).
Les stratégies antithrombotiques en cas de mise en place d’un stent coronaire chez les patients ayant une FA et à risque thrombo-embolique modéré ou élevé, chez lesquels une anticoagulation est nécessaire, sont exposées dans le tableau 5.
Contrôle aigu de la FC et du rythme
Contrôle de la FC
Chez les patients stables, le contrôle de la FC peut être fait par l’administration orale de bêtabloquant ou d’inhibiteur calcique non dihydropyridinique. Lorsque l’état hémodynamique est sévère, l’administration IV de vérapamil ou de métoprolol peut rapidement ralentir la conduction AV. En situation aiguë, la FC cible est habituellement de 80 à 100 bpm. L’amiodarone peut être utilisée en aigu en cas de dépression sévère de la fonction systolique VG.
Cardioversion pharmacologique
La FA se termine souvent spontanément en quelques heures ou jours. Le taux de conversion est moindre avec la conversion pharmacologique qu’avec la cardioversion électrique (tableau 6, figure 5). L’administration IV de flécaïnide ou de propafénone en cas de FA récente (< 24 heures) est efficace pour restaurer le RS. L’administration orale de flécaïnide ou de propafénone est efficace aussi (« pilule dans la poche ») après que l’efficacité et la sûreté de ce traitement ont été démontrées à l’hôpital. L’ibutilide et le sotalol sont plus efficaces pour la conversion d’un flutter atrial. Un nouveau médicament, le vernakalant, est efficace aussi et peut être utilisé chez les patients qui ont une cardiopathie structurelle, s’ils ne sont pas en classe NYHA III ou IV.
Figure 5. Cardioversion électrique et pharmacologique d’une FA récente.
Cardioversion électrique
C’est une méthode efficace de conversion de la FA en RS. Les preuves sont en faveur des défibrillateurs externes biphasiques, et le placement antéropostérieur des électrodes est plus efficace que le placement antérolatéral. Les risques et complications de la cardioversion électrique sont surtout les ATE, les arythmies et les risques liés à l’anesthésie générale. Un prétraitement par un AAR augmente la probabilité de restauration du RS.
Prise en charge à long terme
Elle a cinq objectifs :
– prévention des ATE ;
– prise en charge optimale d’une maladie cardio-vasculaire concomitante ;
– amélioration des symptômes ;
– contrôle de la FC ;
– correction du trouble du rythme.
Le contrôle de la FC est nécessaire chez la plupart des patients ayant une FA ; quelquefois, la FC pendant la FA est naturellement lente. Le contrôle du rythme peut être envisagé si le patient est symptomatique malgré le contrôle adéquat de la FC, ou peut être choisi du fait de la sévérité des symptômes, de l’âge plus jeune ou d’un niveau d’activité élevé. En cas de FA permanente, on contrôle la FC. Si les symptômes liés à la FA sont sévères ou s’il y a aggravation de la fonction VG, le choix peut être le contrôle du rythme, on désigne cette catégorie de FA « FA longtemps persistante ». Dans la FA paroxystique, on choisit souvent le contrôle du rythme, notamment si elle est symptomatique et si une cardiopathie sous-jacente est absente ou modérée. La décision de contrôle du rythme est une décision individuelle et doit donc être largement discutée.
Contrôle de la FC
Chez les patients ayant une FA permanente, mais sans symptômes sévères dus à une FC élevée, le contrôle de la FC peut être modéré (FC au repos < 110 bpm). Un contrôle strict de la FC (FC de repos < 80 bpm et augmentation contrôlée de la FC lors d’un exercice modéré) n’est nécessaire que chez les patients qui restent symptomatiques.
Plusieurs médicaments peuvent être utilisés pour le contrôle de la FC, mais ils doivent être soigneusement choisis en fonction de la maladie cardiaque sous-jacente (figure 6). Les doses de ces traitements sont données dans le tableau 7.
Figure 6. Contrôle de la FC.
L’ablation du nœud AV permet un contrôle très efficace de la FC chez les patients ayant une FA. C’est un traitement palliatif mais irréversible, et il n’est donc raisonnable de l’envisager que chez les patients chez lesquels un contrôle du rythme n’est pas indiqué et le contrôle pharmacologique de la FC, incluant une combinaison thérapeutique, a échoué. Donc, l’ablation du nœud AV est une thérapeutique valable mais rarement indiquée.
Contrôle du rythme par les AAR
Les principes du traitement AAR dans le but de maintenir un RS dans la FA sont les suivants :
– la motivation du traitement est de réduire les symptômes liés à la FA ;
– l’efficacité des AAR à maintenir un RS est modeste ;
– un AAR efficace cliniquement peut réduire plutôt qu’éliminer les récurrences de FA ;
– si un AAR n’est pas suffisamment efficace, une réponse cliniquement acceptable peut être obtenue avec un autre AAR ;
– les proarythmies induites par les médicaments et les effets secondaires extracardiaques sont fréquents ;
– la sûreté plutôt que l’efficacité doit être prioritaire pour guider le choix d’un AAR.
Les médicaments et leurs principaux désavantages sont listés dans le tableau 8.
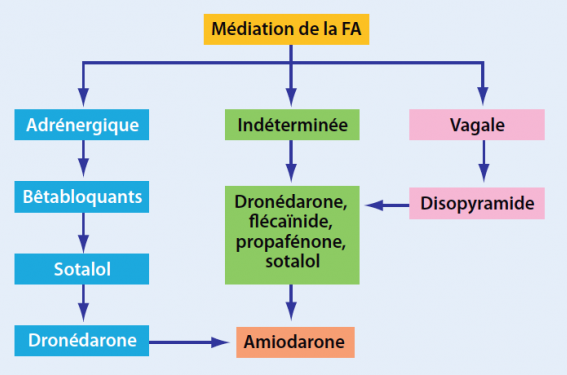
Le choix de l’AAR est illustré dans les figures 7 et 8. Chez les patients sans ou avec minime cardiopathie structurelle, les médicaments sont primairement sélectionnés selon leur sécurité d’emploi, bien que l’allure clinique de la survenue de l’arythmie, FA vagale vs adrénergique, puisse faire suggérer des choix spécifiques. Chez les patients ayant une cardiopathie structurelle, le choix du médicament est déterminé par la maladie cardiaque sous-jacente. La dronédarone n’est pas recommandée chez les patients en IC NYHA III ou IV.
Figure 7. Choix de l’AAR chez le patient avec FA et maladie cardiaque structurelle absente ou minime.
Figure 8. Choix de l’AAR selon la maladie sous-jacente.
Contrôle du rythme par ablation endocavitaire dans l’oreillette gauche
Il est essentiel d’identifier les patients avec un bénéfice potentiel élevé et un risque attendu de complications bas avant de recommander cette stratégie de contrôle du rythme (figure 9). Cette stratégie ne doit pas être envisagée chez les patients asymptomatiques.
Figure 9. Choix entre ablation et AAR.
Contrôle du rythme par ablation chirurgicale
La restauration du RS améliore l’évolution après chirurgie cardiaque. L’ablation chirurgicale est basée sur la création de lésions induisant une cicatrisation de la paroi atriale afin de bloquer la propagation des circuits de réentrée tout en préservant une conduction normale. Cela peut être réalisé par des techniques de coupure-suture, ou avec d’autres sources d’énergie.
Traitement d’amont
Le traitement d’amont, afin de prévenir ou de retarder le remodelage myocardique associé à une HTA, une IC ou une inflammation (par exemple après chirurgie cardiaque) peut prévenir le développement d’une FA nouvelle (prévention primaire) ou, la FA étant présente, son taux de récurrence ou de progression vers une FA permanente (prévention secondaire). Les IEC, les ARA-II, les antagonistes de l’aldostérone, les statines et les acides gras polyinsaturés oméga-3 sont des traitements d’amont de la FA. Malgré des données abondantes sur le potentiel AAR de ces médicaments dans des modèles animaux de FA, les données cliniques restent controversées.
Les preuves les plus abondantes sont en faveur de la prévention primaire de la FA dans l’IC avec les IEC et les ARA-II et dans la FA postopératoire avec les statines. À l’heure actuelle, il n’y a pas de preuve robuste justifiant de recommander l’utilisation des acides gras polyinsaturés oméga-3 pour la prévention, primaire ou secondaire, de la FA.
Les tableaux des recommandations sont à votre disposition en téléchargement sur ce lien.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :