Publié le 04 nov 2008Lecture 8 min
Suivi d’un patient resynchronisé
F. TOURNOUX, Hôpital Lariboisière, Paris
Les Journées françaises de l'insuffisance cardiaque
Le suivi d’un patient resynchronisé pose à l’heure actuelle de nombreuses questions pratiques et en particulier d’organisation. Bien que complexe, il reste primordial pour garantir un bénéfice maximal de la prothèse. Nous verrons donc successivement quels sont les objectifs de ce suivi, qui doit l’effectuer, quels éléments doivent particulièrement être surveillés et à quel rythme doit s’effectuer cette surveillance.
Les objectifs de la surveillance d’un patient resynchronisé
Comme pour toute prothèse, cette surveillance a pour but de prévenir les complications liées à son implantation : complications liées à la procédure bien évidemment (hématome local, déplacement/lésion de sonde, infection, etc.) mais aussi liées aux appareillages eux-mêmes, de plus en plus perfectionnés. Le second objectif est bien évidemment de s’assurer que le patient bénéficie au maximum de la stimulation multisite et, si nécessaire, de savoir ajuster au bon moment la thérapie. Enfin, ces stimulateurs multisites sont souvent associés à un défibrillateur qui par lui-même justifie une surveillance particulière.
Qui doit faire cette surveillance ?
Avant d’être implanté par un stimulateur multisite, le patient était « simplement » un patient insuffisant cardiaque. Il était suivi régulièrement par son cardiologue traitant, éventuellement aidé par un spécialiste de l’insuffisance cardiaque. Grâce aux informations obtenues de l’échocardiographiste, ils ont pu déterminer la gravité du patient et valider pour ce patient les critères actuellement reconnus d’implantation d’un stimulateur multisite (classe III ou IV de la NYHA, fraction d’éjection < 35 %, QRS >120 ms). Ils ont alors proposé le patient à un stimuliste qui a réalisé l’implantation. Le patient a donc bénéficié initialement d’une prise en charge multidisciplinaire (figure 1) qui doit être maintenue après l’implantation, avec des interactions nombreuses et permanentes entre les différents acteurs de la surveillance.
Figure 1. Les différents "acteurs" de la surveillance du patient resynchronisé.
Qui va surveiller quoi ?
Le stimuliste
L’un des premiers acteurs de cette surveillance est bien entendu celui qui a mis en place le dispositif. Il va rechercher des complications liées à la procédure d’implantation et assurer la surveillance technique du stimulateur : contrôle de la batterie, seuils de stimulation/détection, etc. Il va s’assurer que la thérapie est correctement délivrée (idéalement 100 % de capture biventriculaire), en particulier chez les patients en fibrillation auriculaire rapide sans ablation du nœud auriculoventriculaire. Par ailleurs, les prothèses les plus récentes disposent désormais de systèmes de télécardiologie (alertes rythmiques, chocs, etc.) fournissant des informations qu’il faudra analyser et pour lesquelles une prise en charge spécifique pourra s’avérer indispensable. Parmi ces informations, il existe notamment des marqueurs d’insuffisance cardiaque potentiellement informatifs (voir ci-dessous). Enfin, si la thérapie se révèle non efficace voire délétère, le stimuliste prendra bien entendu une part active dans son optimisation.
Le cardiologue traitant
Parallèlement, le cardiologue traitant (plus ou moins aidé du spécialiste de l’insuffisant cardiaque) assurera le suivi général du patient. Suivi clinique tout d’abord (amélioration de la classe NYHA, du score de qualité de vie) mais aussi paraclinique : il peut s’agir de tests très simples comme le test de marche de 6 minutes ou la mesure du pic de VO2max avant (plus objectifs que l’appréciation de la classe NYHA) ou un peu plus complexes comme le BNP (dans une étude de 2006, Pitzalis et coll. ont montré qu’un patient qui n’avait pas normalisé son taux de BNP dans le premier mois suivant la mise en place de la stimulation multisite avait un pronostic significativement plus péjoratif).
Un autre paramètre disponible est la mesure d’impédancemétrie intrathoracique permettant chez un même patient d’identifier les périodes « stables » des véritables poussées congestives. Il n’est pas à l’heure actuelle formellement démontré que l’utilisation de tels marqueurs aient un réel impact sur le suivi des patients et le résultat de plus larges études prospectives (DOT-HF) est nécessaire pour valider ou non définitivement ce type de technologies.
Enfin, la prise en charge du cardiologue traitant reposera pour beaucoup sur les données échocardiographiques obtenues tout au long du suivi.
L’échocardiographiste
Les tâches principales de l’échocardiographiste sont : d’évaluer la sévérité de l’insuffisance cardiaque, d’évaluer la qualité de la resynchronisation ventriculaire gauche et enfin si elle s’avère imparfaite, d’optimiser la thérapie.
La sévérité de l’insuffisance cardiaque
Cela reste une étape indispensable du suivi. En effet, un patient resynchronisé reste un insuffisant cardiaque sévère. On mesurera donc les paramètres de remodelage ventriculaire (fraction d’éjection volumes télédiastolique et télésystolique), le degré d’insuffisance mitrale (dont la réduction par la stimulation peut être majeure), le niveau des pressions de remplissage sur les paramètres usuels (E/A, E/E’, veines pulmonaires, etc.) et enfin la fonction ventriculaire droite dont la réduction grève le pronostic comme chez tout insuffisant cardiaque.
La qualité de la resynchronisation ventriculaire gauche
Elle se mesure à deux moments : en « aigu », c’est-à-dire dans les premiers jours suivants l’implantation, et à « moyen terme » (entre 3 et 6 mois).
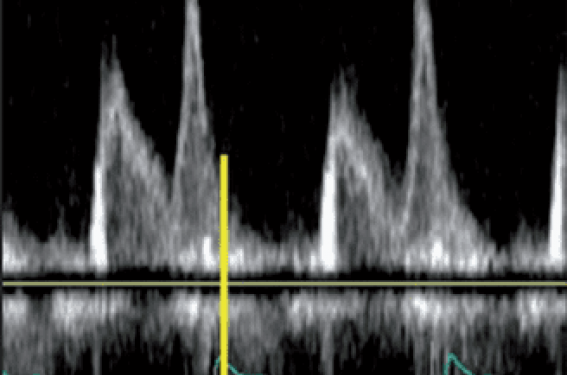
En aigu, il s’agit de rechercher une réduction de l’asynchronisme ventriculaire gauche par la thérapie. En 2007, Bleeker et coll. ont montré qu’une réduction de plus de 20 % de cet asynchronisme juste après l’implantation prédit un degré significatif de remodelage inverse à moyen terme (réduction de plus de 10 % du volume télésystolique). Cependant, compte tenu des résultats récents et décevants de Prospect, la mesure de l’asynchronisme intraventriculaire gauche apparaît difficile et peu reproductible. Une autre évaluation est alors parfois réalisable en aigu : la recherche d’une amélioration de l’hémodynamique. En effet, s’il existe une insuffisance mitrale suffisante, la dP/dt peut être mesurée entre 1 et 3 m/s. Les variations de cette dP/dt du fait de la stimulation biventriculaire peuvent être facilement identifiées comme le montre la figure 2 et ont une valeur pronostique sur le long terme : une augmentation de plus de 25 % de la dP/dt dans les 24 h qui suivent l’implantation est prédictive d’un taux significativement plus faible d’hospitalisations pour insuffisance cardiaque ou de décès (Tournoux et coll., 2007).
Une réduction de plus de 20 % de cet asynchronisme juste après implantation prédit un degré significatif de remodelage inverse à moyen terme.
Figure 2. mesure de la dP/dt chez un patient implanté d'un pacemaker biventriculaire depuis moins de 24h. Avec une stimulation biventriculaire (à droite), la dP/dt est mesurée à 700 mmHg/s versus 400 mmHg/s en position OFF (à gauche). Il s'agit donc d'une augmentation de plus de 25 %, prédictive d'une bonne réponse à long terme.
À moyen terme, on mesurera plutôt le degré de remodelage ventriculaire gauche. En 2005, Yu et coll. ont montré qu’une réduction de plus de 10 % du volume télésystolique est associée à un meilleur pronostic à long terme. Ce marqueur relativement simple à mesurer est depuis utilisé par de nombreux auteurs pour tester la réponse à la stimulation multisite.
L’optimisation
Elle est depuis plusieurs années au centre de nombreux débats. Elle peut se faire à deux étages, auriculoventriculaire et interventriculaire et, jusqu’à cette année, elle ne faisait l’objet d’aucune recommandation claire. La Société américaine d’échocardiographie (ASE) vient d’essayer cette année de faire un résumé de la vaste littérature sur le sujet.
L’optimisation ne doit pas être systématique. Elle peut être longue, parfois difficile et ne semble bénéficier qu’à un groupe limité de patients.
• Pour l’optimisation du délai auriculoventriculaire, les recommandations américaines suggèrent de faire une évaluation du flux mitral en Doppler pulsé avec les réglages « de base » du patient.
Si les ondes E et A apparaissent bien séparées et que l’onde A se termine après le QRS ou que le clic de fermeture mitrale est aligné avec la fin de l’onde A et le complexe QRS, aucune optimisation n’est nécessaire (figure 3).
Figure 3. Arbre décisionnel quant à l'optimisation ou non du délai auriculoventriculaire.
Inversement, une optimisation doit être réalisée. Celle-ci peut se faire via la formule de Ritter ou plus simplement par méthode dite itérative (figure 4).
Figure 4. Exemple d'optimisation du délai auriculoventriculaire : on programme initialement un délai volontairement long (ici 250 ms en haut à gauche). L'onde E apparaît alors comme partiellement fusionnée avec l'onde A, d'où un temps de remplissage ventriculaire gauche court. Plus on diminue le délai auriculoventriculaire, plus l'onde E "sort" progressivement de l'onde A. Cependant, pour un délai court, l'onde A devient alors de plus en plus amputée, témoin d'une diminution du remplissage actif du ventricule (exemple en bas à droite pour 100 ms). Le délai auriculoventriculaire idéal est celui où les ondes E et A sont bien distinctes sans amputation de l'onde A (ici 150 ms en bas à gauche).
• Pour l’optimisation interventriculaire, les petites études disponibles ont montré une augmentation modérée de la fraction d’éjection après optimisation (Sogaard et coll. 2002) avec parfois un bénéfice sur l’insuffisance mitrale (Bordachar et coll., 2000 et 2003). Certains patients semblent réellement en bénéficier de façon aiguë, d’autres non. L’impact sur le long terme reste inconnu et son utilisation doit sans doute être limitée aux non-répondeurs.
En pratique, l’opérateur place son Doppler pulsé sur la chambre de chasse aortique et mesure le VTI sous-aortique (moyenne de 3 valeurs) à la même phase respiratoire pour différents réglages de délai interventriculaire : stimulation simultanée puis pour différentes préactivations du ventricule gauche (-20, -40, -60 ms).
On réalise ensuite la même manœuvre en préactivant le ventricule droit. Une stimulation monoventriculaire gauche peut s’avérer parfois payante et doit être testée. Le VTI sous-aortique le plus important détermine le réglage final. Dans notre laboratoire, l’augmentation du VTI aortique doit être d’au moins 10 % (variabilité interobservateur du laboratoire) par rapport au réglage initial pour être considérée comme significative.
Quand faire cette surveillance ?
(figure 5)
Figure 5. Exemple de suivi d'un patient resynchronisé.
Les premiers jours suivants son implantation
Le patient devra bénéficier d’un contrôle de son pacemaker/défibrillateur, d’un dosage de BNP (valeur de référence) et d’une échocardiographie. Celle-ci pratiquera une première optimisation du délai auriculoventriculaire si nécessaire et cherchera en aigu une réduction de l’asynchronisme ventriculaire et/ou une amélioration de l’hémodynamique pour apprécier la qualité de la resynchronisation.
- À 1 mois : nouvelle évaluation clinique et contrôle de la prothèse. On recherchera une normalisation du dosage de BNP. Si nécessaire, une échocardiographie pour une optimisation complémentaire pourra être réalisée.
- Entre 3 et 6 mois : une échocardiographie devra être réalisée à la recherche d’un remodelage inverse du ventricule gauche (diminution du volume télésystolique > 10 %).
- À 6 mois, une évaluation complète (contrôle de pacemaker, VO2 max, test de marche) sera faîte et débouchera ou non sur la nécessité d’une nouvelle tentative d’optimisation. On pourra aussi se poser la question d’un repositionnement de sonde.
La surveillance suivra ensuite celle des contrôles de la prothèse, à savoir tous les 6 mois.
En pratique
Le suivi d’un patient resynchronisé est un processus complexe nécessitant une évaluation et une prise en charge multidisciplinaire. Une telle surveillance nécessite une organisation parfois lourde mais qui seule peut garantir un suivi optimal. La création dans certains hôpitaux de véritables « cliniques de la resynchronisation » où, régulièrement, au cours d’une même journée, le patient « voit tous ses médecins » qui interagissent entre eux est sans doute une solution idéale vers laquelle il faut tendre.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :