Diabéto-Cardio
Publié le 08 juin 2010Lecture 8 min
Traitement anti-plaquettaire du patient diabétique
O. MOREL, Pôle d’activité medico-chirurgicale cardiovasculaire, Nouvel Hôpital Civil, Strasbourg
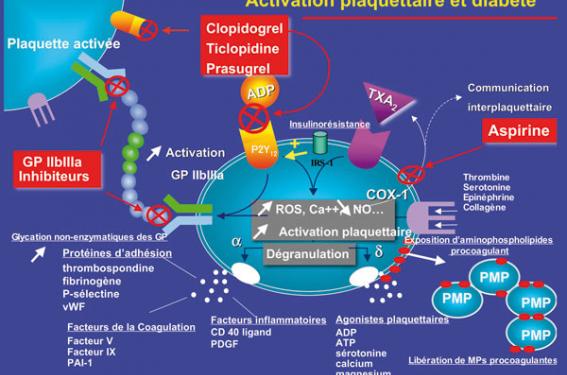
Si la littérature foisonne de papiers démontrant une stimulation plaquettaire intense chez le patient diabétique (figure 1), l’efficacité tout comme le type même des traitements à mettre en œuvre dans cette population à risque athérothrombotique majeur sont beaucoup plus discutés. D’autres mécanismes comme les dommages endothéliaux, une néo-angiogenèse intraplaque importante, des processus inflammatoires ou des phénomènes apoptotiques intenses sont incriminés dans l’athérothrombose accélérée du patient diabétique et pourraient expliquer le bénéfice modeste apporté par la prescription d’antiplaquettaires (figure 2).
Figure 1. Mécanismes de l’activation plaquettaire chez le patient diabétique.
De nombreux facteurs pourraient être impliqués dans l’hyperactivation plaquettaire observée chez le patient diabétique : (i) augmentation du calcium cytosolique, (ii) augmentation de la synthèse des substances radicalaires de l’oxygène, (iii) diminution de la biodisponibilité du NO, (iv) glycation non enzymatique de protéines membranaires, (v) surexpression d’intégrines plaquettaires comme la GPIIb/IIIa, (vi) diminution de l’inhibition plaquettaire par l’insuline. Ces mécanismes contribuent à une augmentation de la synthèse des agonistes plaquettaires comme le thromboxane A2, à la libération de substances procoagulantes ou pro-inflammatoires contenues dans les granules, au remaniement de la membrane plasmique des plaquettes permettant l’externalisation d’aminophospholipides procoagulants comme la phosphatidylsérine et à la libération dans le compartiment vasculaire de microparticules (MPs) procoagulantes plaquettaires.
Figure 2. Mécanismes impliqués dans l’athérothrombose accélérée du patient diabétique.
Chez le patient diabétique, l’activation plaquettaire, la stimulation des monocytes-macrophages, les dommages endothéliaux, l’altération de la fibrinolyse et l’activation de la coagulation sont impliqués dans le développement d’une athérothrombose accélérée. Dans la plaque, une néoangiogenèse intense est observée au cours du diabète, les épisodes d’hémorragies intraplaques constituant un des mécanismes de sa déstabilisation. De plus, les cellules apoptotiques (macrophages, cellules musculaires lisses notamment) libèrent des microparticules (MP) procoagulantes porteuses de facteur tissulaire, responsables de la quasi-totalité de l’activité prothrombotique de la plaque. Au site de la lésion vasculaire, le recrutement précoce des MP circulantes ou séquestrées contribue à la concentration de l’activité facteur tissulaire permettant l’initiation et l’amplification des processus de coagulation.
Prévention primaire
En prévention primaire, plusieurs sociétés savantes recommandent l’utilisation de faibles doses d’aspirine chez le patient à risque cardiovasculaire élevé (tableau 1). Dans la métaanalyse “Antiplatelet trialist”, parmi les 28 000 patients inclus en prévention primaire, indépendamment de l’existence d’un diabète, l’administration d’un antiplaquettaire pendant une durée moyenne de 5 ans permet une réduction modeste de la survenue des infarctus (IDM) non mortels, la réduction des événements vasculaires n’étant pas significative(1).
Chez les patients diabétiques, les données démontant l’efficacité de l’aspirine sont particulièrement ténues. Les recommandations sont basées sur le résultat de trois études principales :
- dans le sous-groupe diabétique de l’étude HOT, de faibles doses d’aspirine (75 mg) ont permis, en association avec un inhibiteur calcique, une réduction du risque de survenue d’un événement cardiovasculaire, au prix d’une majoration de la survenue de saignements non mortels(2) ;
- dans l’US Physician Health Study (USPHS), une diminution prononcée du risque de survenue d’un IDM a été observée à 5 ans chez les diabétiques traités par 325 mg d’aspirine ;
- enfin, dans l’étude ETDRS (Early Treatment of Diabetic Renitopathy Study), un traitement par aspirine a permis une réduction de 28 % du risque relatif de survenue d’un IDM au terme d’un suivi de 5 ans(3).
Néanmoins, plusieurs études comportant des effectifs comparables de patients sont clairement négatives :
- ainsi, dans l’étude PPP, l’intérêt de l’association aspirine et vitamine E a été évalué en prévention primaire. Si cette association permet chez le non-diabétique, une réduction de 41 % des événements cardiovasculaires, la réduction obtenue chez le patient diabétique est moindre (10 %) et n’est pas significative(4). Une tendance à la surmortalité cardiovasculaire a même été observée dans le groupe des diabétiques traités par aspirine et vitamine E ;
- dans l’étude POPADAD (Prevention of progression of arterial disease and diabetes) publiée l’an passé, l’association antioxydants-aspirine n’a pas permis d’obtenir une réduction des événements cardiovasculaires après 8 ans de traitement(5).
Il a rapidement été suggéré que ces résultats déconcertants pouvaient être liés à une inhibition insuffisante des fonctions plaquettaires par l’aspirine seule. Aussi, l’intérêt d’une bithérapie antiplaquettaire par aspirine-clopidogrel a-t-il été évalué dans l’étude CHARISMA. Cette étude comprenait notamment un sous-groupe préspécifié de patients en prévention primaire composé à 80 % de patients diabétiques. Dans ce sous-groupe, une augmentation de 20 % du risque relatif de survenue d’un événement cardiovasculaire a pu être observée chez les patients traités par bithérapie, associée à une surmortalité cardiovasculaire (3,9 % vs 2,2 % ; p = 0,01)(6). Ces données n’ont malheureusement été que très peu commentées.
Si les causes de cette surmortalité cardiovasculaire n’ont pu être clairement établies, un excès d’hémorragie intraplaque pourrait être un mécanisme incriminé.
En effet, plusieurs travaux histologiques ont permis d’établir que la plaque d’athérome du patient diabétique est caractérisée par une intense néoangiogenèse associée à la prolifération des vaso vasorum. La survenue d’un saignement intraplaque est un facteur reconnu de sa déstabilisation, pouvant conduire à sa rupture et à la constitution d’un thrombus surajouté(7).
Prévention secondaire
Pour l’American Diabetes Association, l’administration d’aspirine (81-325 mg) est recommandée chez les patients diabétiques présentant une atteinte athéromateuse. Étant donné l’importance de la voie du P2Y12 chez le patient diabétique, plusieurs travaux ont exploré l’existence d’un bénéfice supplémentaire apporté par les thiénopyridines :
- ainsi, dans une analyse rétrospective de l’étude CAPRIE, Bhatt et coll. ont suggéré une efficacité plus importante du clopidogrel comparativement à l’aspirine dans la réduction du critère combiné (décès cardiovasculaire, AVC, hospitalisation pour ischémie ou saignement : 13,3 % vs 15,6 % ; p = 0,047). Néanmoins, en considérant uniquement les événements ischémiques, la différence entre les deux molécules n’est plus significative(8) ;
- dans l’étude CURE, la bithérapie aspirine-clopidogrel a permis, dans l’ensemble de la population traitée, une réduction du critère primaire ; la réduction de 14,9 % du risque relatif observée chez les 2 840 patients diabétiques inclus (20 % chez les non-diabétiques) n’est pas significative(9) ;
- de même, dans PCI-CURE, la réduction du risque n’est pas significative dans le sous-groupe des diabétiques(10).
Traitement antiplaquettaire au cours de l’angioplastie coronaire
L’angioplastie coronaire représente un modèle de fracture mécanique de la plaque d’athérome conduisant à l’exposition du matériel prothrombotique contenu dans la plaque à l’activation plaquettaire et de la coagulation et à la génération de thrombine. En dépit des progrès techniques et pharmacologiques réalisés ces dernières années, le facteur diabète pris isolément constitue toujours un élément péjoratif du pronostic clinique après la réalisation d’une angioplastie coronaire.
Ainsi, dans l’étude TRITON TIMI 38, le taux de thromboses de stent est deux fois supérieur chez le patient diabétique(11). Au cours des syndromes coronariens aigus (SCA), la charge thrombotique associée à l’intensité de l’activation plaquettaire pourrait expliquer pourquoi la modulation drastique de l’activation plaquettaire est particulièrement bénéfique en termes de réduction des événements (tableau 2). Cette hypothèse est clairement démontrée chez le patient diabétique.
Abciximab
Ainsi, dans une métaanalyse regroupant les premières études consacrées à l’abciximab, l’administration de cette molécule permet une réduction de la mortalité à 1 an chez le patient diabétique(12). De même, au cours des SCA, l’administration d’abciximab permet une réduction de la mortalité cardiovasculaire à 30 jours(13). Ces résultats ne sont pas forcément extrapolables à nos pratiques quotidiennes (dans les études les plus anciennes, absence de bolus de thiénopyridine ou bolus limité à 300 mg de clopidogrel par exemple).
L’intérêt de l’administration d’abciximab chez les patients diabétiques à risque bas ou intermédiaire, bénéficiant d’une angioplastie après administration d’un bolus de 600 mg de clopidogrel, a spécifiquement été exploré dans l’étude ISAR SWEET. À un an, l’incidence du critère combiné décès + récidive d’IDM est comparable dans les deux groupes(14). Néanmoins, une diminution des procédures de revascularisation du vaisseau cible a pu être observée dans le groupe abciximab, ce qui suggère un effet de cette molécule sur la prolifération intimale. Cette hypothèse n’a pas été confirmée dans l’étude ISAR SMART-2 dédiée à l’angioplastie des petits vaisseaux(15). Chez les patients à plus haut risque (SCA ST-) bénéficiant d’une préparation antiplaquettaire « moderne » (clopidogrel 600 mg, aspirine 500 mg), les investigateurs de l’étude ISAR-REACT 2 ont pu mettre en évidence un bénéfice de l’administration d’abciximab, à l’exception notable de la population diabétique(16).
Ce résultat négatif pourrait être attribué à une inhibition insuffisante des fonctions plaquettaires par le clopidogrel.
En effet, de nombreuses études ont établi qu’il existe, chez les patients diabétiques (en particulier insulino-requérants), une proportion plus importante de patients présentant une réponse plaquettaire inadaptée aux doses standard de clopidogrel(17,18).
Des concentrations moindres de métabolites actifs(19), des taux plasmatiques plus importants de fibrinogène(20) ont été avancés comme explications potentielles. Néanmoins, dans cette population, l’impact des polymorphismes des cytochromes impliqués dans le métabolisme hépatique des thiénopyridines (CYP 2C19*) n’est pas connu à ce jour(21).
Les thiénopyridines
Comparativement au clopidogrel, le prasugrel, une thiénopyridine de troisième génération, permet une inhibition plus importante et plus homogène des fonctions plaquettaires. De plus, l’effet du prasugrel ne semble pas affecté par l’existence d’un polymorphisme CYP 2C19*(22). L’intérêt du prasugrel dans l’angioplastie des SCA a récemment été évalué dans l’étude TRITON TIMI 38. Cette étude comprenait notamment 3 146 patients diabétiques(11). En association avec l’aspirine, l’administration de prasugrel a permis une réduction importante du critère combiné, notamment dans le groupe diabétique (décès, récidive d’IDM, AVC, saignement majeur) (12,2 % vs 17 %, HR 0,70 ; p < 0,001). Ce bénéfice est également observé chez les patients traités par anti-GPIIb/IIIa. Le nombre de patients à traiter pour prévenir un événement est de 21 pour les diabétiques de type 2, de 13 pour les diabétiques insulinorequérants et de 711 chez les patients non diabétiques.
Chez les diabétiques, le traitement par prasugrel ne semble pas associé à un surrisque hémorragique.
Les autres voies thérapeutiques
D’autres voies permettant une inhibition plus drastique de l’hyperactivation plaquettaire semblent intéressantes. Ainsi, une trithérapie associant aspirine-clopidogrel à un inhibiteur des phosphodiestérases de type III, le cilostazol pourrait améliorer le pronostic des patients revascularisés par angioplastie sans majorer le risque de saignement(23). Comparativement à la ticlopidine, l’administration du cilostazol pourrait s’accompagner d’une réduction de la prolifération intimale chez le diabétique(24).
Durée du traitement antiplaquettaire chez le patient diabétique
La question de la durée du traitement antiplaquettaire chez le patient diabétique revêt une importance majeure, notamment en cas d’implantation de stents actifs, associés, pour certains d’entre eux, à un retard à la réendothélialisation et à un risque accru de thrombose de stent très tardive (> 1 an). Après un SCA, une bithérapie aspirine-clopidogrel est préconisée pendant 12 mois, suivie d’un traitement au long cours par aspirine.
Chez le patient diabétique, l’arrêt du clopidogrel s’accompagne, au niveau biologique, d’une élévation des taux plasmatiques de la CRP et de la P-sélectine(25). L’impact clinique de ce rebond thrombotique et inflammatoire n’est pas connu à ce jour.
En pratique
Chez le patient diabétique, si les données actuelles sur les bénéfices des antiplaquettaires, notamment en prévention primaire, sont particulièrement modestes, l’angioplastie au cours des SCA constitue une situation où le bénéfice clinique d’une inhibition drastique des fonctions plaquettaires est clairement établi.
Dans cette indication, le prasugrel, qui permet une inhibition plus importante et plus homogène de la voie du P2Y12, pourrait rapidement venir supplanter les autres thiénopyridines.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :