Complication
Publié le 15 oct 2018Lecture 8 min
Prise en charge d’une paralysie diaphragmatique postablation ?
Séverine PHILIBERT, Saint-Joseph, Paris ; Gabriel LAURENT, CHU de Dijon
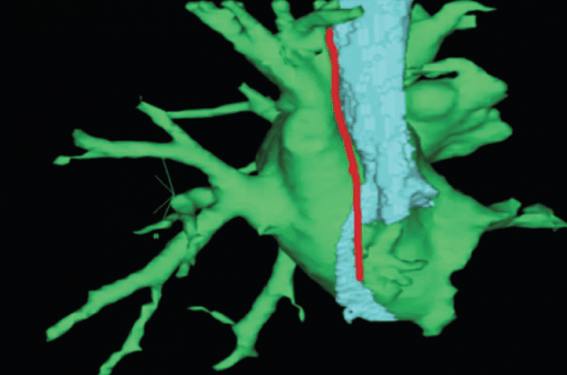
L’isolation « électro-anatomique « des veines pulmonaires (VP) fait partie du quotidien des centres de rythmologie invasive. Qu’elle soit réalisée au moyen d’un cathéter de radiofréquence (RF) ou avec un cryoballon (CB), cette technique d’ablation de la fibrillation atriale (FA), expose malgré tout à des risques dont la paralysie du nerf phrénique droit (PNP). La conséquence peut être une hémiparésie diaphragmatique droite responsable de dyspnée. Ce risque que l’on peut considérer comme un aléa thérapeutique doit être systématiquement expliqué au patient avant la procédure.
Bien qu’en théorie une PNP puisse survenir avec tout type d’énergie, son incidence est plus importante avec l’application du froid. Cette différence est certainement plus liée à la technique qu’à l’énergie elle-même comme nous le rapportons ici à travers les données de la littérature. C’est avant tout la prévention qui doit être au centre de notre attention.
Paralysie du nerf phrénique avec la cryoablation
L’application circonférentielle de froid via un cryoballon placé à l’ostium des VP est une technique de plus en plus utilisée, du fait d’une courbe d’apprentissage courte mais aussi d’une efficacité clinique comparable à long terme à la radiofréquence. La paralysie diaphragmatique droite est décrite comme la complication la plus fréquente avec une incidence d’environ 6 % (3 à 11 %)(1-3).
Sur le plan anatomique, le trajet du nerf phrénique droit (NPD) est relativement proche des VP droites. D. Sanchez-Quintana et al. ont décrit qu’il passait à proximité de la veine cave supérieure (VCS) (distance min : 0,3 ± 0,5 mm) et du bord supérieur de la VP supérieure droite (VPSD) (distance min : 2,1 ± 0,4 mm)(4). La proximité anatomique de ces structures ainsi que la grande surface de distribution du liquide de refroidissement via le ballon favorisent cette complication.
Elle peut également être favorisée par une inadéquation entre la taille du ballon (petit diamètre : 23 mm) et celle de la veine (grand diamètre). Dans cette situation, le ballon risque d’être introduit trop profondément (dans un objectif d’occlusion complète), ce qui expose également au risque de sténose de VP. Il est préférable dans ce cas de prendre un ballon de taille plus importante (28 mm) et de le positionner de la manière la plus antrale possible. En pratique courante, c’est le ballon le plus gros qui est le plus utilisé. Une sonde d’échographie intracardiaque peut également fournir des informations sur le placement antral du ballon, réduisant ainsi la risque de gel profond dans la VP et le risque de PNP(5). Récemment, il a été montré une plus grande efficacité du cryoballon de deuxième génération (CB2) comparé à la première génération de ballons (CB1). Dans une étude allemande publiée en 2015 dans EuroPACE, les 2 générations de CB de 28 mm ont été comparées en termes de sécurité et d’efficacité. Un total de 360 patients atteints de FA a subi une isolation des VP avec le CB1 (106 patients) ou le CB2 (254 patients). L’intégrité du NP droit au cours de l’ablation des VP droites a été surveillée par la palpation de l’intensité du hoquet produit par une stimulation continue du nerf au niveau de la veine sous-clavière. Cette technique est classiquement utilisée dans les centres qui pratiquent cette technique. Une PNP en cours de procédure est survenue dans 8,7 % avec le CB2 versus 5,7 % avec le CB1, différence non significative. Le taux de PNP persistante (jusqu’à 480 jours de suivi) n’était pas non plus significativement différent : 2,8 % et 1,9 % pour CB2 et CB1(6).
Dans une étude belge de 2014 comparant les deux générations de ballons, le taux de PNP était de 4,5 % avec le CB2, potentiellement en lien avec l’utilisation du petit diamètre (23 mm). Une récupération au cours du suivi a été retrouvée dans 78 % des cas. Il faut noter que la majorité des patients étaient asymptomatiques(7).
Il existe donc des résultats contradictoires dans la littérature concernant l’incidence de cette complication lorsque l’on compare les deux générations de ballons(6-9). Actuellement cela a peu d’importance puisque l’utilisation du CB2 s’est généralisée.
Pour résumer, on peut dire que l’incidence d’une PNP aiguë n’est pas négligeable au décours d’une procédure de cryoablation (8 % au maximum), et qu’elle peut persister au long cours dans 1,5 à 4,5 %. Il n’y a pas de données évaluant les conséquences sur la qualité de vie des patients, mais il semble fort heureusement que ceux-ci restent majoritairement asymptomatiques.
Paralysie du nerf phrénique avec la radiofréquence
Dans l’essai randomisé FIRE and ICE examinant les profils d’efficacité et de sécurité en cryoablation et par radiofréquence, l’incidence des lésions du NP était respectivement de 2,7 % et de 0 %(10, 11). Dans Freeze-AF, les résultats sont similaires avec 5,8 % versus 0 , ce qui signifie que l’utilisation de la radio-fréquence présente un meilleur profil de sécurité vis-à-vis de cette complication.
À noter que dans Freeze-AF, le taux plus élevé de PNP avec la cryoablation peut s’expliquer aussi par l’utilisation plus importante de CB1(12). La généralisation des techniques d’isolation antrale des VP par radiofréquence, à l’aide des systèmes de navigation intracardiaque (qui permettent de « taguer » le trajet du nerf si nécessaire), a fait quasiment disparaître cette complication.
Monitoring perprocédure
Pour surveiller le NP, on le stimule au double du seuil de capture à l’aide d’un cathéter proche de la jonction entre la VCS et la veine sous-clavière droite (figure 1). Un monitoring manuel avec palpation de la force d’excursion diaphragmatique pendant la stimulation du NP, sous la marge costale, est la méthode la plus commune de surveillance. Un monitoring peut également être réalisé à l’aide du cathéter ICE placé dans la VCI afin de suivre les mouvements du diaphragme(5).
Figure 1. Position radiologique du cathéter quadripolaire pour monitoring du nerf phrénique. Le ballon de cryothérapie se trouve dans la VPSD.
La réduction de l’amplitude ou la perte de la contraction diaphragmatique imposent la déflation du cryoballon en urgence. En pratique, l’opérateur peut parfois faire face à un déplacement du cathéter placé en regard du NP, simulant une PNP, aussi il est important de s’assurer de la stabilité de ce cathéter avant de débuter le froid. On conseille de rester attentif durant les 4 minutes de la brûlure, même si celles-ci peuvent paraître longues et il est impératif de ne pas utiliser de produit curarisant lors des procédures sous anesthésie générale. Si c’est le cas à l’induction, la néostigmine peut être utilisée comme antagonisant.
En plus de la palpation, la surveillance de l’EGM du diaphragme (PACM) peut augmenter la sensibilité de la détection précoce d’une PNP(13-14). Dans l’étude française de F. Franceschi et al., une réduction de 30 % de ce potentiel a été identifiée comme seuil pour prédire la PNP. Cette valeur a été confirmée par une étude canadienne sur 200 procédures. Cette technique a permis de réduire à 1,5 % l’incidence des PNP persistantes en fin de procédure(15). S’il se produit une PNP, l’opérateur doit immédiatement arrêter l’ablation. Le monitoring du PACM peut aider à évaluer le temps de récupération de la fonction du diaphragme. Si la durée de récupération est courte, l’ablation peut être reprise avec une position plus antrale du ballon. Si la paralysie persiste après l’intervention, une radiographie du thorax de référence doit être réalisée pour suivre ensuite l’évolution.
Bilan morphologique postprocédure
La radiographie thoracique de face est un examen simple, qui doit être répété pour suivre l’évolution d’une ascension de la coupole diaphragmatique droite (figure 2). La TDM ou l’IRM thoraciques permettent une appréciation grossière de l’amyotrophie de la coupole qui se laisse davantage refouler vers la cavité pleurale en position allongée. L’IRM permet également de détecter des mouvements paradoxaux des coupoles paralysées lors du cycle respiratoire.
Figure 2. Paralysie diaphragmatique droite à 24 h d’une ablation par cryothérapie. Noter la surélévation de la coupole. Neuf mois plus tard ce patient a partiellement récupéré alors qu’il présentait initialement une réduction de sa capacité pulmonaire totale de 30 %.
L’élévation d’une coupole diaphragmatique entraîne le plus souvent un syndrome restrictif dont la sévérité est assez proportionnelle à l’importance de cette élévation. Cette restriction est majorée lors du passage de la position assise à la position couchée. Cette aggravation positionnelle est due à l’incapacité de la coupole amincie à lutter contre la pression abdominale qui augmente en position allongée. La réduction de la cavité pleurale qui en résulte entraîne une compression du parenchyme pulmonaire sus-jacent voire des cavités cardiaques. Dans la cadre du bilan, il est donc particulièrement intéressant de faire des EFR en position assise et en position couchée afin d’apporter un élément supplémentaire dans le diagnostic de la faiblesse anormale de la coupole.
Approche thérapeutique
Il n’y a à ce jour aucune recommandation dans la prise en charge des PNP dans les suites d’une ablation de FA. Certains auteurs proposent une perfusion de stéroïdes pour diminuer l’inflammation à la phase aiguë(16).
Dans les séries publiées, il semble que cette complication soit le plus souvent asymptomatique. Il faut essayer d’améliorer les patients qui restent gênés avec l’aide de nos collègues pneumologues qui ont l’habitude de prendre en charge ce type de pathologie.
Il est important de corriger les facteurs aggravant la dyspnée (surpoids, tabagisme, BPCO). La kinésithérapie peut être utile pour accélérer la récupération musculaire. En cas de retentissement important sur la ventilation pendant le sommeil, la dysfonction diaphragmatique peut justifier une assistance ventilatoire nocturne. Ce traitement améliore la qualité de vie des patients.
Il n’y a aucune publication à ce jour qui confirme l’intérêt de cette prise en charge, ni aucune proposition thérapeutique dans les recommandations européennes ou américaines(17,18). L’approche thérapeutique n’est donc pas codifiée et il faut donc tout entreprendre pour réduire l’incidence de cette complication. La gestion de ces patients doit se faire au cas par cas et il faut les rassurer sur les chances de récupération même au-delà de 2 ans.
Conclusion
Une PNP peut survenir au cours d’une procédure d’ablation de FA en particulier lors de l’isolation des VP droites (particulièrement la supérieure) et de la VCS. Il s’agit d’un aléa thérapeutique dont il est impératif de prévenir les patients.
Davantage de précautions sont à prendre en cas de cryoablation, dont une bonne adéquation entre la taille du ballon et celle de la VP, ainsi qu’un positionnement le plus antral possible. Un monitoring du nerf phrénique pendant les brûlures doit être réalisé systématiquement pour détecter précocement cette complication qui a de grandes chances de récupération si les brûlures sont stoppées immédiatement.
L’incidence de la PNP après cryoablation à 1 an est comprise entre 1,5 et 4,5 %, sans données au-delà de 12 mois dans la littérature. Le point le plus rassurant est que les PNP secondaires à l’ablation semblent avoir un pronostic bénin et que dans la plupart des cas, il existe une récupération clinique complète avec le temps.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


