Focus
Publié le 31 mai 2012Lecture 5 min
Recommandations pour la gestion péri-opératoire des prothèses rythmiques
C. GRIMARD, InParys, Saint Cloud
Environ 4,5 millions de personnes dans le monde sont porteuses d’une prothèse cardiaque rythmique (stimulateur ou défibrillateur). Dix pour cent de la population générale subit chaque année une intervention chirurgicale. Malgré une technologie toujours plus sophistiquée des prothèses cardiaques, le risque théorique d’interactions sur le fonctionnement de ces prothèses au cours d’une chirurgie, ablation, anesthésie ou autre radiothérapie n’est pas nul.
Une prise en charge conjointe du patient porteur d’une prothèse cardiaque, impliquant cardiologue, chirurgien et anesthésiste, permet d’établir la conduite à tenir en fonction du type d’intervention prévue, avant, pendant et après celle-ci, afin qu’aucune situation délicate ne mette le patient en danger. Enfin, des recommandations concernant la gestion des prothèses en périopératoire sont éditées chaque année par un consensus d’experts américains (American Society of Anesthesiologists [ASA], Society of Thoracic Surgeons [STS], HRS et AHA)(1).
Quelles sont les interactions rencontrées ?
Ce sont les interférences électromagnétiques qui représentent la majorité des interactions périopératoires.
Interférences liées au bistouri électrique
Les plus fréquentes sont celles liées à l’utilisation du bistouri électrique. Elles découlent de l’utilisation d’un courant de radiofréquence localisé, afin d’obtenir une parfaite dessication tissulaire ou coagulation vasculaire.
Le courant électrique peut être délivré en mode mono ou bipolaire.
En mode bipolaire (chirurgie ophtalmologique ou microchirurgie), la probabilité de survenue d’une interaction est infiniment faible(2).
En mode unipolaire (majorité des chirurgies), le courant est délivré via un stylet sur le site opératoire et traverse le corps du patient sur une large surface avant d’atteindre l’électrode de retour ; le risque d’interférences est donc plus important. Il augmente avec l’étendue de surface corporelle traversée et avec une éventuelle traversée de la prothèse cardiaque. Ainsi, la localisation de la plaque de retour du bistouri est-elle capitale.
Autres interférences
Les autres interférences résultent de l’exposition à de nombreuses sources d’énergie ou radiations, et de l’utilisation d’appareils électriques à proximité ou au contact direct des prothèses cardiaques(3). Ces sources d’interférences sont listées dans le tableau 1, ainsi que les moyens de limiter leur survenue.
Quelles sont les conséquences de ces interactions ?
L’impact clinique des interférences
Il dépend de l’indication d’implantation de la prothèse, de la stimulodépendance du patient, du mode de stimulation programmé, et de la présence dans la prothèse de filtres et autres algorithmes permettant de la protéger contres ces interférences.
L’impact rythmique des interférences
Il peut être de différents types.
Surdétection
Il s’agit de loin de la conséquence la plus fréquente.
Le stimulateur entend à tort des impulsions électriques émanant de la source d’interférence. Il en résulte des inhibitions de stimulation à l’étage auriculaire ou ventriculaire. Ces inhibitions sont d’autant plus graves que le patient est stimulodépendant (risque de pauses cardiaques pouvant déstabiliser l’hémodynamique ou entraîner des syncopes). Sur un défibrillateur, les artefacts peuvent être interprétés à tort comme une tachycardie, pouvant conduire au déclenchement de l’appareil et à la délivrance de chocs électriques.
Lésions myocardiques
L’utilisation d’un bistouri électrique monopolaire dont le circuit traverse la prothèse cardiaque peut entraîner une lésion tissulaire à l’extrémité de la sonde enchâssée dans le myocarde. Cette lésion peut elle-même être responsable d’une élévation du seuil de stimulation de la sonde concernée(4).
Mise en route de l’asservissement de fréquence
Elle se fait via les capteurs intrathoraciques qui sont à l’origine du fonctionnement de cet algorithme et le stimulateur peut analyser les artéfacts induits par un bistouri comme une respiration rapide, et augmenter la fréquence de stimulation à sa fréquence maximale.
Reprogrammation sur un mode de secours
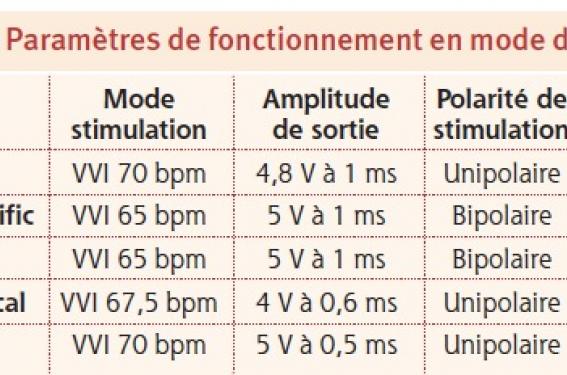
Ce cas est rencontré essentiellement dans le cadre de l’exposition aux radiations ionisantes. La prothèse se trouve alors reprogrammée sur un mode dit « de secours » ventriculaire (tableau 2). Elle ne tient plus compte des paramètres antérieurement programmés. Sur un défibrillateur, une seule zone de thérapie est ouverte avec délivrance de chocs électriques à pleine énergie.
Quelle stratégie adopter afin de limiter la survenue de ces interférences ?
En préopératoire
• Consulter les données récentes du stimulateur/défibrillateur figurant sur le dernier compte rendu : longévité, derniers seuils, alertes récentes.
• Connaître l’indication d’implantation de la prothèse : stimulation, défibrillation, resynchronisation.
• Déterminer la stimulodépendance du patient, son rythme intrinsèque.
• Déterminer l’effet de l’aimant sur la prothèse.
• Déterminer le risque potentiel de survenue d’interférences en fonction du type d’intervention ou examen prévu. Si nécessaire au vu de tous ces paramètres, prévoir un nouveau contrôle du stimulateur avec une éventuelle reprogrammation. En cas de désactivation préférable du défibrillateur, le lieu et la date de l’intervention doivent être choisis pour permettre au rythmologue d’intervenir.
En peropératoire
• Présence d’un chariot d’urgence, d’un équipement de stimulation/défibrillation externe, et d’un aimant.
• Surveiller l’ECG. Le scope doit être réglé sur le mode « stimulation » permettant de compter les spike sans sur-détection.
• Mettre des patches de défibrillation externe en cas de désactivation du défibrillateur.
• S’assurer qu’un contrôle de la prothèse peut être effectué si nécessaire.
En postopératoire
• Reprogrammer le défibrillateur si désactivation préalable.
• Interroger le stimulateur cardiaque en cas de doute sur la survenue d’interférences pendant l’intervention : impédances des sondes, tests de seuil, mise à zéro des mémoires. Le reprogrammer en cas de programmation sur un mode particulier en préopératoire (IRM, désactivation de l’asservissement, etc.).
• Les experts recommandent un contrôle systématique de la prothèse après une séance de radiothérapie ; un contrôle à 1 mois en cas de chirurgie avec utilisation du bistouri, de CEE, d’une ablation par radiofréquence, d’une électro-convulsivothérapie, ou d’une lithotripsie.
Conclusion
Les prothèses cardiaques modernes sont conçues pour supporter une intervention chirurgicale ou autre exposition aux interférences sans entraîner de mauvais fonctionnement ou de modification de leur programmation. Les interférences pouvant perturber ce fonctionnement sont rares, et leurs effets sont très largement mineurs sur la bonne marche de ces prothèses(5). L’amélioration permanente de la technicité des stimulateurs augmente constamment la sécurité de leur environnement.
Cependant, l’amélioration parallèle des techniques d’imagerie, l’utilisation croissante d’appareils électriques et la diffusion des ondes dans notre entourage sont des raisons suffisantes pour rester disponibles afin de traquer de nouvelles interactions potentielles, surveiller, contrôler, et reprogrammer les appareils de nos patients afin de leur en éviter les désagréments.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


