La lettre du GACI
Publié le 30 mar 2021Lecture 8 min
TAVI - Gestion du traitement antithrombotique en 2021
Ashok TIROUVANZIAM, Hôpital Privé du Confluent, Nantes
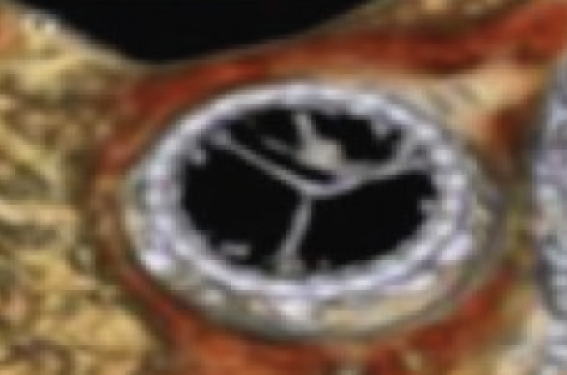
Depuis la première implantation en 2001 par Alain Cribier(1), le TAVI (trans-aortic valve implantation) est devenu le traitement de choix de la sténose aortique serrée symptomatique quel que soit le risque opératoire du patient : inopérable, haut risque, risque intermédiaire. Il est désormais également validé par la Food and Drug Administration (FDA) en cas de bas risque opératoire(2) lorsque la voie transfémorale est réalisable.
Bien que réduites au fil des ans du fait des améliorations technologiques et de l’expérience accumulée des opérateurs, les complications liées au TAVI demeurent toutefois supérieures à celles observées pour l’angioplastie coronaire(3). Elles sont d’ordre essentiellement hémorragique et ischémique – les seules abordées dans cet article – et altèrent le pronostic du patient à long terme après réalisation du TAVI (figure 1).
Figure 1. Saignements tardifs post-TAVI.
La prévention et le traitement de ces complications sont rendus complexes en raison d’une population traitée âgée, présentant de lourdes comorbidités et pour laquelle la balance risque hémorragique sur bénéfice ischémique du traitement antithrombotique est aléatoire.
Les complications cérébrovasculaires du TAVI
Elles sont de 0,6 à 6,4 % à 30 jours (2,2 à 10,4 % à 1 an ; tableau 1), et sont superposables aux taux observés dans le remplacement valvulaire aortique chirurgical.
Leurs causes sont multifactorielles et fonction de la période de survenue en postopératoire.
• Périprocédurales de J0 à J1 : embolisation par interaction guides/cathéters avec l’arbre vasculaire, les sigmoïdes aortiques.
• Postprocédurales de J1 a J30 : survenue de fibrillation atriale/ FA de novo dans 15 % des cas.
• Tardives au-delà du premier mois jusqu’à 1 an : FA chronique dans 30 % des cas et athérosclérose diffuse (figure 2).
Figure 2. Complications tardives post-TAVI.
La réalisation systématique d’une imagerie cérébrale par résonance magnétique (IRM) après TAVI montre la présence de lésions cérébrales silencieuses chez 2/3 de patients sans corrélation anatomoclinique claire avec d’éventuelles dysfonctions neurocognitives postopératoires(4). Le recours aux filtres de protection cérébrale (FPC) a été préconisé pour prévenir ce risque embolique.
Si les résultats préliminaires de registres observationnels concernant l’usage des FPC démontrent leur efficacité en termes de capture de débris emboliques, ceux-ci n’ont aucun effet sur la réduction de la mortalité à 30 jours. Les réponses sur la nécessité de leur usage systématique (patient jeune à faible risque), ou ciblé sur des patients à haut risque (antécédent d’AVC, FA, sténose carotidienne, bicuspidie, etc.) sont attendus.
Dans l’étude PROTECTED-TAVR, 3 000 patients bénéficiant d’un TAVI, avec ou sans protection par le filtre Sentinel (Claret Médical) vont être randomisés jusqu’en juillet 2022. L’objectif primaire est le taux d’AVC intrahospitalier ; la fin des inclusions est prévue en juillet 2022.
La prévention des complications emboliques se joue également durant la procédure sur le plan technique : franchissement prudent de la crosse aortique (système flex cathéter, technique dite du « no touch »), de l’orifice aortique, stenting direct chaque fois que possible, choix judicieux du diamètre du ballon pour la pré- ou postdilatation, détection de thrombi éventuels en préopératoire (débris de la crosse ou du ventricule gauche).
La durée de la procédure doit être optimisée et la plus brève possible.
Infarctus et TAVI
Avec une prévalence de 40 à 70 % de coronaropathies chez les patients bénéficiant d’un TAVI, le taux d’infarctus est de 5,1 % à 30 jours (2 % à 1 an)(5).
En l’absence de données dans la littérature, la gestion de la coronaropathie préopératoire est variable selon les pratiques : elle va de l’absence de coronarographie diagnostique à une revascularisation systématique des lésions détectées. Cette dernière stratégie reste l’objet d’un débat et soulève en outre plusieurs types de questions : tout d’abord le bénéfice réel d’une revascularisation associée au TAVI, le moment de sa réalisation (pré- ou post-TAVI ?), l’accès futur aux coronaires (et donc le choix du type de valve intra ou supra-annulaire à privilégier), et enfin, la gestion périopératoire de la bithérapie antiagrégante, reconnue comme un facteur de risque prédictif indépendant de saignement intrahospitalier(6).
La thrombose de bioprothèse TAVI
La sous-étude d’imagerie de l’étude PARTNER 3 (figure 3), a mis en évidence un degré variable de dysfonction bioprothétique allant du simple HALT asymptomatique (hypo attenuating leaflet thickening, 14 % à 30 jours), à l’obstruction thrombotique valvulaire totale pouvant entraîner une défaillance hémodynamique et clinique sévère.
Figure 3. Les différents stades des thromboses de bioprothèses TAVI (d’après Makkar et al. PARTNER 3 CT, TCT 2019).
Toutefois, le bénéfice d’un usage systématique des anticoagulants (AOC) en prévention du HALT pouvant être contre-balancé par le risque hémorragique non prédictible dans une telle population, n’est validé par aucune donnée actuelle de la littérature. Des facteurs prédictifs indépendants de thrombose valvulaire post-TAVI ont néanmoins été mis en évidence parmi lesquels : le diamètre de prothèse < 23 mm, la procédure de valve in valve, l’index de masse corporel > 30 kg/m² et l’insuffisance rénale chronique (tableau 2).
Une attention particulière doit être portée au suivi clinique et échographique des patients présentant ces facteurs de risque, permettant une prise en charge thérapeutique précoce, le cas échéant, de la thrombose valvulaire.
Quel que soit le stade de la thrombose (dont le mécanisme est préférentiellement thrombine dépendant), le traitement anticoagulant (AVK) s’avère plus efficace qu’une mono- ou une bithérapie antiagrégante, et doit être maintenu jusqu’à normalisation clinique, échographique et scanographique de contrôle (il est discuté au cas par cas au-delà).
Complications hémorragiques du TAVI
La majorité des saignements est précoce et survient dans les 30 premiers jours qui suivent la procédure (10,4 %), avec un taux cumulé de 15,2 % à 1 an (figure 4). Qu’ils soient précoces (liés majoritairement à la voie d’abord ou au péricarde), ou tardifs au-delà du premier mois (d’origine gastro-intestinale, urogénitale ou neurologique), les saignements augmentent significativement la mortalité à 1 an (figure 1).
Figure 4. Taux de saignements à 30 jours et 1 an au décours d’un TAVI.
La réduction de ces complications passe par la connaissance et la maîtrise préalable des facteurs favorisants :
Sexe féminin, insuffisance rénale chronique, artériopathie périphérique, ratio diamètredésilet sur artère > 1, gestion de l’anticoagulation périopératoire, sélection par imagerie de la voie d’abord principale, voie radiale accessoire, ponction sous échographie vasculaire, maîtrise des systèmes de fermeture et enfin diagnostic précoce et gestion des complications vasculaires.
Recommandations actuelles en 2021
(tableau 3)
Dans l’attente des résultats de larges études randomisées, les recommandations concernant le traitement post-TAVI se fondent actuellement sur des études observationnelles et l’avis d’experts et préconisent d’un côté et de l’autre de l’Atlantique :
• L’aspirine au long cours (classe IIA, niveau de preuve B).
• Une bithérapie antiagrégante (aspirine et clopidogrel), pour les 6 premiers mois (classe IIB, niveau de preuve C).
• Les antivitamine K (avec objectif d’INR à 2,5), pendant les 3 premiers mois chez les patients à faible risque de saignements (classe IIB, niveau de preuve B).
• Les anticoagulants oraux directs (AOD), ne sont pas à ce jour recommandés en cas de fibrillation atriale (FA), valvulaire et/ou de prothèse mécanique associée.
• Gestion du traitement antiagrégants plaquettaires
Pour les patients ne nécessitant pas de traitement AOC au long cours, les résultats d’une métaanalyse regroupant 4 études randomisées (dont la cohorte A de l’étude POPular TAVI), comparant 665 patients répartis en 2 groupes (aspirine seule vs aspirine + clopidogrel pendant 3 mois post-TAVI), a démontré une réduction significative des saignements (majeurs et mineurs) sous aspirine seule (HR : 0 ,49 ; IC 95 % : 0,32-0,75), sans majoration des complications ischémiques (infarctus et AVC ) ou de la mortalité globale(7). Ces données devraient faire évoluer les recommandations pour passer de la bithérapie actuelle à une monothérapie par aspirine durant la phase dite « d’endothélialisation » de la prothèse.
• Gestion du traitement anticoagulant
Trente pour cent des patients éligibles au TAVI sont sous traitement AOC au long cours (la FA chronique en étant la principale indication), et 15 % développent une FA de novo dans l’année qui suit l’implantation(8).
Le traitement AOC est un facteur de risque prédictif indépendant de mortalité à 3 ans dans le registre FRANCE-TAVI(9).
Compte tenu par ailleurs du risque hémorragique et de la surmortalité induite par la bithérapie antiagrégante (DAPT) en sus du traitement anticoagulant, l’alternative d’un traitement simplifié par monothérapie antiagrégante (SAPT), a été évaluée dans différentes études. Parmi celles-ci, la 2e cohorte de l’étude randomisée POPular TAVI a inclus 665 patients en deux bras (331 patients traités par AOC seul vs 334 patients traités par AOC + clopidogrel pendant 3 mois).
Elle a démontré une diminution significative à 12 mois de tout type de saignement dans le bras AOC seul (resp. 21,7 % vs 34,6 % ; p < 0,01), sans majoration des événements cardiovasculaires ou ischémiques (resp. 13,4 % vs 17,3 %), critère de non-infériorité atteint (figure 5). Seuls 24 % des patients de cette cohorte étaient traités par AOD, il n’est donc pas possible de tirer des conclusions comparatives avec les AVK.
Figure 5. POPular TAVI : taux de saignements à 1 an selon le groupe(7).
• Place des nouveaux anticoagulants oraux directs
Les AOD apparaissent comme une alternative intéressante aux AVK (meilleure compliance, surveillance biologique simplifiée, interactions médicamenteuses minimisées, etc.) en post-TAVI.
Leur bénéfice sur la réduction des complications hémorragiques (dont celles d’origine intracrânienne), sans effet pour autant sur les événements ischémiques (IDM, AVC) ou sur la mortalité globale, n’a été démontré que dans des registres prospectifs observationnels tels que OCEAN-TAVI(10).
L’étude randomisée GALILEO(11), a comparé le rivaroxaban (Bayer) à faible dose sur 2 groupes recevant rivaroxaban (10 mg) associé à une faible dose d’aspirine pendant 3 mois versus clopidogrel (75 mg) associé à une faible dose d’aspirine pendant 3 mois, chez des patients n’ayant pas d’indication à un traitement anticoagulant.
L’étude a été stoppée prématurément en raison du taux de décès (resp. 7,7 % vs 4,6 %) et de complications thromboemboliques (resp. 12,7 % vs 9,5 %), supérieurs dans le groupe AOD, sans explication valide concernant cette surmortalité.
Dans ces conditions et à la lumière de cette étude, l’usage d’un AOD (même à faible dose) en post-TAVI, en l’absence d’indication pour une anticoagulation orale, ne peut être recommandé et reste purement empirique à ce jour.
Des réponses concernant la place des AOD par rapport aux AVK, chez les patients ayant une indication d’anticoagulation sont en attente des résultats des études suivantes :
– ATLANTIS comparant l’apixaban (Bristol Myers-Squibb) au traitement standard (AVK ou APT) ;
– ENVISAGE TAVI-AF comparant l’édoxaban (Daiichi Sankyo) aux AVK.
– WATCH-TAVR comparera chez les patients en FA à haut risque hémorragique, la fermeture de l’auricule gauche par le système WATCHMAN™ (Boston Scientific) au traitement médical.
Conclusion
Ce que l’on sait en 2021
▹ La population bénéficiant d’un TAVI est à haut risque hémorragique et ischémique.
▹ Les recommandations actuelles concernant le traitement post-TAVI sont limitées, à faible niveau de preuves et basées sur des registres observationnels et sur l’opinion d’experts. Le traitement anticoagulant au long cours est un facteur prédictif de mortalité à long terme, l’adjonction d’un traitement antiplaquettaire (mono ou bithérapie), majore ce risque.
▹ Les AVK sont efficaces dans le traitement curatif des HALT.
▹ La monothérapie antiagrégante par aspirine réduit le risque hémorragique sans effet sur la mortalité ou les complications ischémiques en comparaison d’une bithérapie antiagrégante en post-TAVI.
▹ En l’absence d’indication d’anticoagulant, le traitement par AOD, même à faible dose, n’est pas indiqué à l’heure actuelle. Chez les patients en FA, la place de ces nouvelles molécules reste à définir en comparaison des AVK, dans l’attente des résultats prochains des études randomisées.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


