Grand angle
Publié le 20 juin 2019Lecture 8 min
Création de fistule artérioveineuse d’hémodialyse par voie percutanée
Alexandros MALLIOS*, Thomas LE HOUÉROU, Ghazi HARIKA, Jennifer CANONGE, Romain DE BLIC, Alessandro COSTANZO, Benoît BOURA, Institut Mutualiste Montsouris, Paris *A. Mallios est consultant pour Avenu Médical et BD
Depuis la première publication par Brescia et Cimino en 1966(1), la fistule artérioveineuse (FAV) native reste le meilleur abord vasculaire chez les patients atteints d’insuffisance rénale au stade terminal et nécessitant une épuration extrarénale. Les autres types d’accès employés n’ont jusqu'alors pas obtenu de meilleurs résultats en termes de perméabilité, de complications, de durée d'hospitalisation et de coût malgré le progrès des variables techniques et de produits développés par l’industrie(1-3).
Néanmoins, les résultats sont extrêmement fluctuants avec des taux d’échec de maturation allant de 50 à 60 % et environ 50 % de perméabilité primaire(4-7). La grande variabilité des résultats chez des cas similaires suggère que le bilan préopératoire, les techniques chirurgicales et l’expérience de l’opérateur influencent considérablement la maturation de la fistule, qui peut souvent nécessiter plusieurs interventions d’angioplastie endoluminale pour finalement aboutir à obtenir une FAV opérationnelle(8-11).
Depuis quelques années deux techniques ont été développées pour la confection d’une FAV par voie percutanée.
• Le système ELLIPSYS® (Avenu Medical), qui utilise l’énergie thermique pour créer une anastomose par fusion tissulaire entre l’artère radiale proximale (ARP) et la veine perforante du coude (VPC).
• Le système WavelinQ™ (BD-BARD), qui utilise deux cathéters portants des aimants et une électrode transmettant un courant électrique pour créer une communication entre l’artère radiale ou l’artère cubitale et sa veine profonde satellite(12-15).
Dans cet article, nous décrivons les aspects techniques et la littérature existente à ce jour concernant ces deux techniques.
Présentation des deux systèmes et technique
Le système ELLIPSYS®
Le principe de fonctionnement du cathéter ELLIPSYS® repose sur l’utilisation d’une résistance thermique (TRAD-thermal resistance anastomosis device) permettant ainsi la section puis la fusion en forme d’ellipse des parois artérielles et veineuses afin de créer une communication entre celles-ci (figure 1).
Figure 1 : A : cathéter ELLIPSYS®, extrémité. B : cathéter et poignet du système. C : générateur.
La fusion tissulaire intervient lorsque le collagène de type I est chauffé à plus de 140 °C sous des pressions exercées entre 2 et 23 bars, provoquant ainsi la réticulation des fibres de collagène entre les tissus adjacents(16-17).
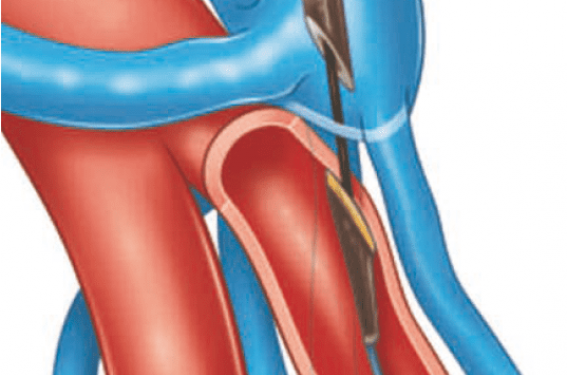
Une ponction est réalisée au niveau de la veine médiane céphalique ou médiane basilique à l’aide d’une aiguille de microponction (COOK© Medical). Sous échographie en coupe axiale, l’aiguille est acheminée depuis le point de ponction jusque dans la VPC où elle transfixe la paroi de l’artère ARP lorsqu’elle croise la VPC (figure 2).
Figure 2 : Ponction de la veine médiane céphalique puis ponction directe de l’artère radiale proximale (ARP) à travers la veine perforante du coude (VPC).
Après avoir ponctionné l’artère depuis la veine, un introducteur 6 F radial Glidesheath Slender® (Terumo Interventional Systems) est introduit sur un guide 0,021’’. Il est ensuite réalisé un échange de guides, pour un Nitrex™ 0,014’’ (ev3©) de 80 cm. Vient ensuite l’introduction du système ELLIPSYS® dont la forme distale du cathéter joue le rôle d’hameçon lorsqu’il est en position ouverte, venant ainsi buter contre la paroi artérielle lors de la traction du dispositif (figure 3).
Figure 3 : Le système ELLIPSYS® en position ouverte qui vient buter contre la paroi artérielle lors de sa traction.
À la fermeture du système, les parties distale artérielle et proximale veineuse se rejoignent, mettant en contact les deux parois. Le générateur donne instantanément l’épaisseur de tissu comprise entre la partie distale et proximale du cathéter qui doit se situer entre 0,2 et 0,9 mm et qui confirme la bonne prise des deux parois. Après activation, une énergie thermique est appliquée pendant trois cycles d’une dizaine de secondes tout en exerçant une légère traction sur le cathéter lors du dernier cycle. Cette légère traction permet ainsi de libérer le système une fois la fusion terminée et l’anastomose est créée (figure 4).
Figure 4 : Après l’activation du générateur, l’application de l’énergie thermique et de la pression de courte durée permettent la création d’une anastomose permanente par thermofusion.
L’hémostase est réalisée par compression du point de ponction veineux pendant 2 à 3 minutes.
Le résultat obtenu est une anastomose calibrée, de forme elliptique de 4 x 2 mm (figure 5). Une dilatation immédiate de l’anastomose par un ballon de 5 x 20 mm permet d’accélérer la maturation de la FAV.
Figure 5 : Vue intérieure de l’anastomose.
Le système WavelinQTM
Il repose sur l’utilisation d’une électrode de radiofréquence mise en place en position latérale sur un cathéter inséré dans la veine qui va venir au contact d’un cathéter artériel. Le bon positionnement des cathéters veineux et artériel repose sur l’utilisation d’aimants disposés de manière régulière le long des cathéters. Une fois correctement alignés, ils apparaissent comme une succession de bandes blanches et noires en fluoroscopie (figure 6).
Figure 6 : Vue fluoroscopique du système WavelinQ™.
Cette technique nécessite donc deux introducteurs : un artériel et un veineux. La première génération du système avait un diamètre de 6 F et nécessitait une ponction de l’artère et la veine humérale. La deuxième génération du système a maintenant un diamètre réduit de 4 F et la ponction peut être réalisée également au niveau de l’artère et la veine radiale si l’anatomie le permet (diamètre de vaisseaux > 2 mm) (figure 7).
Figure 7 : Deuxième génération du système WavelinQTM 4 F.
Une fois le cathéter veineux bien positionné, une électrode de radiofréquence, vient s’appuyer sur une facette en céramique du cathéter artériel délivrant ainsi un courant de radiofréquence pendant 2 secondes (0,7 seconde à la puissance de 60 W pour le WavelinQ™ 4 F EndoAVF) et vaporise ainsi les tissus de part et d’autre (figure 8). L’ablation des guides est nécessaire pendant l’activation de la sonde de radiofréquence. La fistule est ainsi créée. Lors de l’ablation du cathéter veineux, il est recommandé de réaliser une embolisation de la veine humérale afin de recentrer le flux sanguin dans le réseau superficiel. Le cathéter artériel permet lui de réaliser l’angiographie de contrôle.
Figure 8 : Visualisation de l’électrode qui livre le courant électrique pour créer la communication artérioveineuse.
Résultats
Les résultats initiaux de création de FAV par voie percutanée sont très prometteurs mais il s’agit de deux techniques très récentes avec peu d’études. Aucune étude randomisée à ce jour n’a comparé les résultats des FAV percutanées aux FAV chirurgicales.
Pour le système ELLIPSYS®, les études publiées de Hull, Mallios et Hebibi ont montré un succès technique de 95-99 % et une perméabilité secondaire 86 %-96 % à 1 an. Les réinterventions les plus fréquentes sont des angioplasties de l’anastomose pour augmenter le débit et faciliter les ponctions (35 %). Pour quelques patients (7 %), une superficialisation peut être nécessaire si la veine est trop profonde. Une ponction avec un cathéter cathlon (Wallace) au niveau de la veine médiane basilique et/ou basilique permettant l’utilisation de la veine basilique sur sa partie proximale, près du coude là où la veine est sous la peau, peut éviter un geste de superficialisation chez ces patients (figure 9).
Figure 9 : Patient avec une FAV créée par le système ELLIPSYS® et dialysé depuis 1 an en biponcture au niveau de la veine céphalique sans aucun signe de dégénération anévrismale. Une ponction de la veine médiane basilique pourrait aussi être effectuée chez ce patient si sa veine céphalique était difficile à ponctionner ou de longueur insuffisante au niveau de son bras.
Aucune complication importante a été signalée, aucun cas d’hyperdébit ou de vol vasculaire. Les taux de maturation et utilisation de FAV sont supérieurs de 90 % à 1 an avec d’excellents paramètres de dialyse(18-20).
L’étude NEAT qui a évalué la première génération du système WavelinQ™ a démontré un succès technique de 98 % avec 8 % de complications importantes liées à la procédure et 2 % liées au dispositif. Le pourcentage de patients avec une perméabilité fonctionnelle était de 64 % à 12 mois et la perméabilité cumulative à 84 %(21). L’étude EASE a évalué le système de 4 F sur 32 patients avec un succès technique de 100 % avec 3 % de complications importantes. La perméabilité cumulative était de 87 % et la perméabilité fonctionnelle de 74 % à 6 mois.
La seule étude comparative des deux systèmes a été présenté par R. Sharvedyan au congrès SIR 2019 (Austin, États-Unis). Les résultats de 27 patients opérés avec le système WavelinQ™ versus 30 patients opérés par le système ELLIPSYS® ont montré moins de réinterventions pour ELLIPSYS® et une supériorité en ce qui concerne la perméabilité, la maturation et l’utilisation de FAV (figure 10)(23).
Figure 10 : Comparaison des deux systèmes sur 57 patients, présentée par R. Shahverdyan lors du congrès SIR 2019.
Discussion
La création de fistule par voie endovasculaire offre certains avantages et pas seulement d’un point de vue esthétique. Les FAV chirurgicales pourtant bien supérieures aux prothèses et aux cathéters tunnelisés ont souvent des problèmes de maturation ou de complications sévères(24,25).
La création d’une FAV utilisant plusieurs veines de drainage et l’artère radiale pour l’anastomose permet de créer une FAV avec un débit modéré et une pression basse qui semble être un vrai avantage à moyen et probablement à long terme(19,26,27). Les deux systèmes existants permettent la création d’une FAV par voie percutanée. Néanmoins, ils ont certaines différences importantes par rapport à la nature de l’énergie utilisée pour créer la FAV, la localisation anatomique, le besoin d’embolisation de veines profondes et l’utilisation de rayons X. Ces différences techniques semblent également avoir une influence sur les résultats fonctionnels(23).
Conclusion
À ce jour cependant, les études sont encore limitées et le recul encore insuffisant. Il faudrait des études comparatives supplémentaires dans le futur sur les résultats à long terme des créations de FAV percutanées.
Mais il semble évident que la création de FAV par voie endovasculaire va devenir la technique de référence pour les patients ayants une insuffisance rénale terminale. Grâce à l’avancée technologique, au perfectionnement de la technique et à une meilleure expérience des équipes, les résultats continueront à s’améliorer, comme on peut l’observer avec toutes les autres techniques innovantes et mini-invasives.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :


