Rythmologie et rythmo interventionnelle
Publié le 02 nov 2014Lecture 10 min
Faut-il vraiment ablater tous les flutters auriculaires ?
J.-F. LECLERCQ, Paris
Il faut commencer par regarder le tracé ECG, et examiner le patient. Autrement dit, comme toujours en médecine, faire le diagnostic avant le traitement... Cela permettra, même si l’on n’est pas un rythmologue professionnel, de classifier le trouble du rythme dans l’une des catégories définies ci-dessous.
Le flutter commun
C’est de loin le plus fréquent. L’aspect en dents de scie qui remplace la ligne isoélectrique en II, III, F est caractéristique, à tel point que c’est la première arythmie décrite par sir Thomas Lewis juste après la découverte de l’électrocardiogramme. Il traduit une dépolarisation permanente de l’oreillette droite selon un mouvement circulaire antihoraire, descendant rapidement par la paroi latérale grâce à la crista terminalis et remontant plus lentement par le septum (Puech). Il est dû à une macro-réentrée avec une zone de conduction lente dans l’isthme cavo-tricuspide décrit par Cosio. Cet isthme entre la veine cave inférieure, l’ostium du sinus coronaire et la tricuspide est une région où, de façon physiologique, la conduction est plus lente que dans le reste de l’oreillette droite, et c’est un point de passage obligé de l’influx pour boucler le circuit du flutter.
Toute pathologie entraînant une dilatation de l’oreillette droite va ralentir encore la conduction dans l’isthme, permettant que s’y crée le bloc unidirectionnel nécessaire à la réentrée. De fait, les patients ayant un flutter commun ont un isthme plus long avec une poche plus profonde que la normale(1). L’incidence annuelle du flutter commun est de l’ordre de 1 ‰ chez l’adulte, et de 6 ‰ après 80 ans. Les pathologies causales sont l’insuffisance cardiaque et l’insuffisance respiratoire, les causes déclenchantes les plus fréquentes étant la chirurgie thoracique ou cardiaque et les infections respiratoires. Mais même s’il y a souvent une cause aiguë déclenchante, le flutter commun une fois installé n’a en général pas tendance à s’arrêter si le circuit de macro-réentrée n’est pas perturbé par des extrasystoles intercurrentes. La tolérance est variable en fonction de la conduction nodale et de la pathologie sous-jacente, mais souvent mauvaise, en particulier à l’effort.
Dans le flutter commun, l’ablation par radiofréquence de l’isthme cavotricuspide est le traitement de choix. Elle doit représenter le traitement de première intention puisqu’elle permet d’éviter les récidives dans environ 95 % des cas, au prix d’un geste interventionnel simple, bref, quasiment exempt de complications. Celles-ci sont au nombre de deux : complications de l’abord veineux fémoral, et épanchement péricardique réactionnel, les deux bien rares. En effet, se contenter d’arrêter le flutter par stimulation ou par choc n’empêchera pas sa récidive, et les traitements antiarythmiques ne sont que médiocrement efficaces : on le voit bien puisqu’ils s’avèrent en général incapables de stopper un flutter installé (sauf l’ibutilide, utilisable seulement en intraveineux). De nombreuses études contrôlées ont ainsi comparé le taux de récidive de flutter après cardioversion simple ou après ablation par radiofréquence(2-5) : elles sont toutes positives. Pourtant, il n’y a pas de recommandations sur ce sujet.
En pratique donc, tous les flutters communs permanents doivent être ablatés, du moins dès que l’on décide de remettre le patient en rythme sinusal. C’est le cas de l’immense majorité des patients, notamment lorsqu’il y a une fréquence ventriculaire élevée et/ou une altération de la fonction pompe. Seul le flutter à conduction lente chez le grabataire en institution est à respecter...
Mais bien des patients ayant un flutter commun ont (ou auront) aussi de la fibrillation auriculaire (FA). C’est le cas de tous ceux qui ont une grosse oreillette gauche, qui sont hypertendus, ou qui ont une cardiopathie gauche, car si le flutter est une maladie de l’oreillette droite, la fibrillation est une maladie de l’oreillette gauche. Cela représente plus de la moitié des patients ayant un flutter commun. Eh, oui ! les mêmes causes produisant les mêmes effets, et les deux oreillettes étant électriquement reliées, le contraire serait étonnant... En pratique, seuls les patients qui ont du flutter sur une affection respiratoire et quelques patients jeunes n’ayant strictement rien d’autre, chez qui on peut suspecter une anomalie anatomique isolée de l’isthme cavo-tricuspide, n’ont pas de risque de développer de la FA. D’où la discussion après ablation du flutter de l’intérêt de la poursuite des anticoagulants, des antiarythmiques et des antihypertenseurs, notamment les sartans(6,7). Bien sûr, l’attitude sera différente selon qu’il s’agit d’un premier accès clairement favorisé par une cause aiguë (postopératoire de chirurgie pulmonaire) chez un patient à cœur gauche normal, ou d’un flutter sous antiarythmique chez un patient traité de longue date pour FA paroxystique...
La question de l’intérêt de l’ablation de l’isthme cavo-tricuspide chez les patients ayant à la fois de la FA et du flutter documentés n’est pas actuellement tranchée. Pourtant les liens entre les deux affections sont dans ce cas évidents, l’une entraînant l’autre, et ce réciproquement(8). On peut donc espérer diminuer l’incidence des accès de FA en supprimant la possibilité de faire du flutter par ablation de l’isthme. C’est ce qu’ont noté divers auteurs(2-4). Mais il n’est pas question de supprimer le risque de FA simplement en traitant le flutter. Donc chez ces patients, la place de l’ablation de l’isthme est à discuter selon le contexte : si le flutter est permanent et médiocrement toléré, il est logique d’en faire l’ablation. En revanche, si le patient alterne FA, flutter et rythme sinusal, ce n’est probablement pas l’ablation de l’isthme qui va résoudre son problème. Il est à signaler que la seule recommandation disponible sur l’ablation de flutter concerne les patients candidats à l’ablation de la FA : ceux qui ont du flutter associé doivent alors avoir une ablation de l’isthme, recommandation de classe I B(9).
Le flutter inverse
Plus difficile à reconnaître sur le tracé de surface, il a un « air de famille » avec le flutter commun. Mais les dents de scie sont inversées : dans le commun, dans les dérivations inférieures, la descente est lente et la remontée rapide alors que dans l’inverse, c’est... l’inverse ! (figure 1). Pourquoi ? Parce que c’est le même circuit de macro-réentrée, mais tournant dans l’autre sens.
Figure 1.
Dans le flutter commun, l’influx tourne dans le sens antihoraire, descendant par la crista terminalis et remontant par le septum, et dans le flutter inverse le circuit est horaire, descendant par le septum et remontant par la crista. En somme, c’est la même chose, sauf que c’est le contraire... On le voit bien sur la figure 2 où est présentée la cartographie faite rapidement avec deux cathéters dans les deux cas.
Figure 2. Dans le flutter commun, au centre, le sinus coronaire est dépolarisé de l’électrode proximale vers la distale, et la crista terminalis de haut en bas avec la proximale de la sonde d’ablation avant la distale (circuit antihoraire). Dans le flutter inverse, à droite, le sinus coronaire est dépolarisé de la même façon alors que la crista terminalis se dépolarise de bas en haut, avec l’électrode distale de la sonde d’ablation précédant la proximale (circuit horaire).
L’ablation de l’isthme est donc aussi efficace dans le flutter inverse que dans le flutter commun, puisque le point critique est le même. Ainsi les indications sont les mêmes. Mais vous vous demandez peut-être pourquoi on voit plus de 90 % des flutters sous la forme « commune » antihoraire, et pou quoi le rapport entre les deux formes n’est pas 50-50... ? C’est parce que vous n’avez pas compris quelle est la genèse du flutter. Pour boucler le circuit de réentrée, l’influx doit être bloqué dans une zone de bloc unidirectionnel (ici l’isthme). Si le flutter commun est de loin le plus... commun, c’est qu’il est lancé par des extrasystoles auriculaires gauches : bloqué dans l’isthme, l’influx parcourra l’oreillette droite dans le sens antihoraire et pourra alors traverser l’isthme dans ce sens puisqu’il sera sorti de sa période réfractaire. C’est ce que constatent les électrophysiologistes qui veulent déclencher un flutter commun chez un patient en rythme sinusal : on y arrive en envoyant des extrastimulations dans le sinus coronaire, mais si l’on fait la même chose sur l’oreillette droite latérale, on ne déclenche rien, ou un flutter inverse car dans ce cas l’influx tournera dans le sens horaire après le blocage dans l’isthme. Effectivement en clinique la majorité des patients qui ont du flutter ont beaucoup plus de raisons d’avoir des extrasystoles initiatrices venant de l’oreillette gauche que de la droite.
Les flutters incisionnels
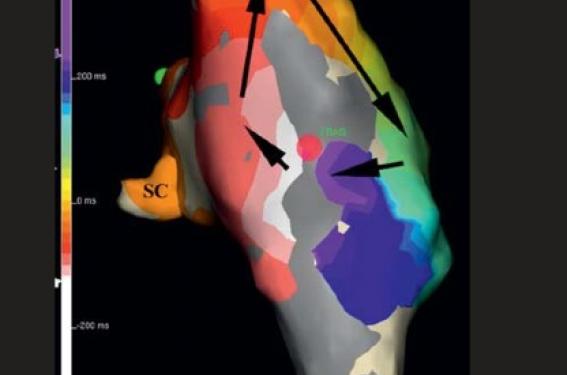
Ce sont ceux aimablement fournis par les chirurgiens cardiaques, grâce aux incisions qu’ils pratiquent dans l’oreillette droite pour réparer une cardiopathie congénitale, cyanogène ou non. Le prototype est la réparation de la communication interauriculaire. Dans la majorité des cas, le chirurgien a pratiqué une atriotomie droite verticale en avant de la crista terminalis. Ces patients, surtout ceux opérés tardivement, ont alors de quoi développer un circuit de flutter commun avec la dilatation auriculaire droite consécutive au shunt gauche-droit, mais ils peuvent également constituer un circuit de réentrée autour de la cicatrice d’atriotomie. Ils peuvent aussi avoir les deux, soit séparément, soit ensemble (circuit en 8 avec deux bras différents en avant et un bras commun en arrière, comme sur la figure 3). Dans ce cas, l’ablation de l’isthme seul est inefficace, et il faut compléter le geste par une autre ligne d’ablation joignant la partie basse de l’atriotomie à la veine cave inférieure. D’une façon générale, il est difficile de prévoir à l’avance le ou les circuits en cause, et ces gestes d’ablation bénéficient grandement des techniques de cartographie tridimensionnelle qui sont l’apanage des centres spécialisés en rythmologie interventionnelle. La figure 4 en montre un exemple très parlant : la tachycardie tournait bien autour de l’atriotomie droite, mais la réflexion se faisait en plein dans cette cicatrice où la conduction avait repris, des années après l’acte chirurgical.
Ces flutters incisionnels doivent toujours être ablatés : ils sont particulièrement rebelles aux médicaments antiarythmiques, et la majorité de ces patients ayant une oreillette gauche normale n’ont guère de risque de FA. L’ablation du flutter incisionnel sera donc effectivement un geste curatif.
Figure 3. Si l’on fait l’ablation de l’isthme, on n’interrompt que la moitié du circuit qui continuera à tourner autour de l’atriotomie.
Figure 4. Vue postéro-latérale droite. Le schéma couleur suivant l’arc-en-ciel montre que la totalité du cycle tachycardique est autour de la cicatrice d’atriotomie verticale (en gris foncé). En suivant l’ordre des couleurs, on voit que l’influx descend en avant de la cicatrice et remonte derrière, mais que le passage entre les deux se fait non pas juste au-dessus de la veine cave inférieure, comme c’est le plus souvent le cas : ici le chirurgien, probablement instruit par l’expérience, a bien prolongé son incision jusqu’à la VCI qui est cicatricielle. Le passage du violet au blanc se fait à travers la cicatrice qui a donc repris une conduction lente, 15 ans après l’intervention... En ce point précis, on enregistre un potentiel fragmenté quasi continu, et un seul tir arrête le flutter.
Les flutters gauches
C’est une pathologie bien plus rare que les précédentes, du moins tant qu’un geste d’ablation n’a pas été effectué dans l’oreillette gauche... car il y a actuellement une véritable « épidémie » de flutters gauches iatrogènes tournant autour de lignes d’ablation plus ou moins incomplètes effectuées pour traitement de la fibrillation auriculaire. On peut aboutir ainsi à transformer une FA paroxystique en flutter gauche permanent nettement moins bien toléré... En pratique, la plupart de ces patients doivent être repris pour ablation (sans enthousiasme car le remède s’est avéré pire que le mal !). On essaie en règle générale auparavant de les interrompre par choc et de renforcer le traitement antiarythmique.
Ce que l’on peut voir en dehors des séquelles d’ablation est un flutter périmitral, notamment après chirurgie mitrale (prothèse ou réparation). Le traitement en est difficile : peu sensible aux antiarythmiques, difficile à stopper par stimulation, geste interventionnel risqué à gauche chez un mitral opéré... dont l’oreillette gauche est très pathologique. Ici pas d’indication d’ablation a priori mais bien celle du choc et des médicaments.
Ce qui n’est pas un flutter...
On entend par flutter (au sens large) une macro-réentrée dans une oreillette (droite ou gauche). Mais cela ne résume pas bien sûr tous les troubles du rythme auriculaire à cadence régulière ou pseudo-régulière. Si la FA franchement irrégulière est aisément reconnue, il est des FA à grosses mailles dont l’irrégularité du cycle atrial ne saute pas aux yeux (ce que d’aucuns ont pu appeler « fibrillo-flutter »), et il y a bien des tachycardies atriales organisées, régulières, qui ne sont pas des flutters. Des micro-réentrées auriculaires ou des foyers ectopiques sont alors en cause. Ils peuvent parfois simuler un flutter (figure 5), et sont accessibles aux techniques d’ablation. Mais celle-ci n’est pratiquée qu’en seconde intention. En effet, les réentrées auriculaires sont souvent peu rapides, bien tolérées, occasionnelles et ne posent guère de problèmes thérapeutiques : rien ou pas grand-chose suffira comme traitement... Quant aux foyers, ils sont par nature capricieux, peuvent se manifester et disparaître quand cela leur chante. On conçoit que les indications d’ablation sont ici rares, sans aucun rapport avec ce que l’on entend par flutter dans le langage courant.
Figure 5. L’aspect de l’activité atriale ressemble un peu à celle d’un flutter dans les dérivations inférieures, mais la fréquence (130 bpm) n’a rien à voir, et la négativité de l’oreillette en I,L et V6 signe l’origine auriculaire gauche.
En conclusion
Avant de faire ablater un flutter, regardez bien le tracé ainsi que le contexte et si vous avez des doutes, demandez à un « sachant ». Si l’ablation par radiofréquence de l’isthme cavo-tricuspide est bien le standard international du traitement du flutter, elle ne constitue pas pour autant le traitement adéquat de tous les troubles du rythme auriculaire...
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :