Thérapeutique
Publié le 30 avr 2015Lecture 15 min
Faut-il revasculariser ou non les patients coronariens stables ?
J.-G. DILLINGER, P. HENRY, Hôpital Lariboisière, Paris
Alors que les nouvelles recommandations européennes sur la revascularisation myocardique ont été publiées cette année, nous célébrons le 51e anniversaire des premières interventions de pontages aorto-coronaires réalisées en 1964. Depuis cette période, la revascularisation myocardique des patients coronariens a considérablement progressé, que ce soit par chirurgie cardiaque avec le choix des greffons artériels ou que ce soit par angioplastie avec l’amélioration des « devices ». L’ensemble de ces progrès a abouti à une baisse régulière des événements cardiovasculaires chez nos patients coronariens stables. De la même manière, l’évolution constante de la pharmacopée (aspirine, bêtabloquants, statines, inhibiteurs de l’enzyme de conversion, etc.) a permis d’offrir un traitement médical optimal à nos patients, améliorant leur qualité de vie et leur pronostic. Mais avec un tel éventail de médicaments, faut-il encore revasculariser nos patients coronariens stables en 2015 ? Si oui, lesquels et comment ? Voici quelques éléments de réflexion issus de l’« evidence based medicine » et de notre « experience based medicine ».
Qu’est-ce que l’angor stable ?
La maladie coronaire stable est caractérisée par des épisodes réversibles d’ischémie myocardique qui sont inductibles par l’exercice, l’émotion ou un autre stress et qui sont reproductibles pour un même niveau de stress. Ces épisodes sont couramment associés à un angor mais peuvent être asymptomatiques. La maladie coronaire stable inclut aussi le patient stable, souvent asymptomatique, après un syndrome coronaire aigu et le patient asymptomatique avec une ischémie myocardique silencieuse comme le patient diabétique. Le caractère stable de la maladie est défini par l’absence d’évolutivité dans le temps de cet angor ou de ces lésions. Bien sûr, la première chose sera de s’assurer que le patient ne présente pas un syndrome coronaire aigu (évolutivité de l’angor, signes ECG, élévation de troponine, etc.) auquel cas la conduite thérapeutique sera complètement différente. De plus, nous n’évoquerons pas ici les cas particuliers de l’angor spastique et de l’atteinte microvasculaire.
Quels sont sa fréquence et son pronostic ?
La prévalence de l’angine de poitrine est difficile à définir de façon précise. De façon constante dans la littérature, elle augmente avec l’âge dans les deux sexes (5-7 % chez les hommes et les femmes âgés de 45-64 ans à 10-12 % chez les femmes âgées de 65-84 ans et 12-14 % chez les hommes âgés de 65 à 84)(1). Chez de nombreux patients, les premières manifestations de la maladie coronaire peuvent être une dysfonction endothéliale et/ou une atteinte microvasculaire (ex : impuissance) et ces signes sont associés à un risque augmenté de maladie coronaire. Concernant le pronostic, les études cliniques les plus récentes comme les registres retrouvent des taux de mortalité annuelle d’envi ron 2 % par an(2-5). Toutefois, au sein de cette population avec une maladie coronaire stable, le pronostic individuel peut varier considérablement en fonction des caractéristiques cliniques (sévérité de l’angor), des caractéristiques anatomiques (lésions multiples ou du tronc commun, fraction d’éjection ventriculaire gauche, etc.) et des autres comorbidités (âge, insuffisance rénale, diabète, etc.). Chez les patients à haut risque (diabète, antécédent d’IDM, maladie artérielle périphérique), la mortalité annuelle peut atteindre 4 % comme dans le registre REACH(6).
Quel traitement médical optimal ?
La revascularisation myocardique n’est pas une alternative au traitement médical. Ce dernier est systématique, que l’on envisage ou non une revascularisation. Ce traitement médical a d’abord pour but de soulager les symptômes (et d’améliorer la qualité de vie) mais surtout d’éviter les événements cardiovasculaires aigus (figure 1). Les statines et les antiagrégants plaquettaires (aspirine ou clopidogrel) sont les seuls médicaments qui contribuent à améliorer le pronostic des patients avec les bêtabloquants et les IEC en cas de dysfonction ventriculaire gauche. Le traitement médical s’intègre dans une prise en charge globale des facteurs de risque (LDL < 0,7 g/l, pression artérielle <140/90 mmHg) auquel doit s’associer l’exercice physique (dans le cadre ou non d’une réadaptation cardiaque) et la modification du style de vie (sevrage tabagique, régime alimentaire équilibré, etc.). L’ensemble de cette prise en charge optimale comme dans l’étude COURAGE permet de réduire la mortalité cardiovasculaire à moins de 1 %/an dans cette population(7,8).
Figure 1. Traitement médical du patient coronarien stable d’après les recommandations ESC 2013(9).
Quantifier l’ischémie myocardique ?
La quantification de l’ischémie myocardique ou de la sévérité des lésions est fondamentale pour guider la revascularisation. Le premier examen complémentaire indispensable est l’échographie cardiaque qui permettra de déterminer la fraction d’éjection ventriculaire gauche (FEVG), de mettre en évidence des troubles de cinétique et d’appréhender l’ischémie de façon indirecte. Le registre CASS a bien montré qu’une FEVG altérée était l’élément le plus fort pour prédire un mauvais pronostic. La survie sans mortalité à 12 ans dans ce registre était de 73 % en cas de FEVG ≥ 50 %, de 54 % en cas de dysfonction VG modérée (entre 35 et 50 %) et de 21 % en cas de dysfonction VG sévère (≤ 35 %). L’échographie cardiaque a donc un rôle pronostique déterminant. Pour quantifier l’ischémie de façon plus précise, un examen complémentaire de stress ou une imagerie coronaire est nécessaire, pas tant pour confirmer le diagnostic, mais pour établir le pronostic à moyen et long terme. Le choix de l’examen de dépistage fait souvent l’objet de controverse. Toutes ces techniques ont toutes des avantages mais aussi des limites. Le choix du test doit s’effectuer en fonction du profil du patient notamment son niveau de risque (appelé aussi probabilité prétest), et des possibilités locales. L’accès à plusieurs techniques de quantification d’ischémie ne peut être qu’un avantage pour le cardiologue pour orienter son patient vers l’examen le plus pertinent. Les indications des différentes techniques et leur sensibilité et spécificité respectives sont présentées dans le tableau 1. Une coronarographie devra être proposée chez les patients dont le test de dépistage a mis en évidence une ischémie significative.
L’échographie cardiaque avec analyse de la FEVG est un élément majeur pour le pronostic du coronarien stable et pour guider la revascularisation.
Quel patient angineux stable coronarographier d’emblée ?
La coronarographie est rarement nécessaire en première intention pour établir le diagnostic de maladie coronaire. Elle peut être envisagée chez certains patients où aucun examen non invasif ne sera contributif, ce qui reste assez rare. En revanche, il est justifié de proposer l’examen en première intention pour établir la sévérité des lésions chez les patients avec une altération de la fonction ventriculaire gauche (< 50 %). Les patients avec une dysfonction VG ont une mortalité annuelle ≥ 3 % même sans facteurs de risque associés et il est donc important de ne pas omettre une maladie coronaire sousjacente. Par ailleurs, chez les patients avec une probabilité quasi certaine de maladie coronaire (essentiellement chez les hommes de plus de 60 ans avec un angor typique) ou des symptômes sévères (angor au moindre effort/CCS3), il semble licite de pratiquer directement une coronarographie d’évaluation, ce qui ne veut pas dire forcément revascularisation. Chez ces patients, le but de cet examen sera de dépister les lésions menaçantes telles que des lésions bitronculaires ou tritronculaires ou une lésion significative du tronc commun ou de l’IVA proximale qui laisse préjuger d’une ischémie étendue. Toujours dans le registre CASS, la survie des patients traités médicalement à 12 ans était de 91 % en l’absence d’atteinte coronaire contre 74 % chez le patient monotronculaire, 59 % chez le patient bitronculaire et 50 % chez les patients tritronculaires.
Quel patient angineux stable coronarographier après un test d’ischémie ?
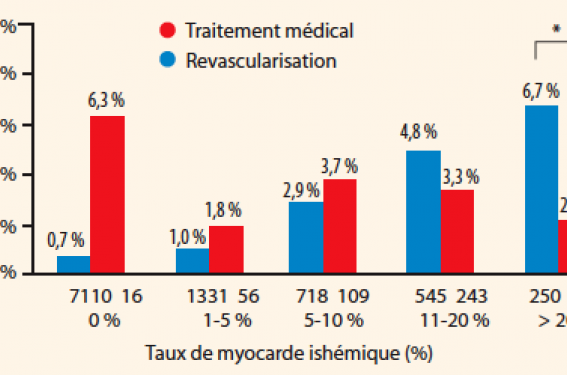
R. Hachamovitch et coll. ont montré que chez les patients avec une ischémie myocardique ≥ 10 %, le traitement médical ne suffisait pas pour prévenir les événements cardiovasculaires (figure 2)(10). L’étude scintigraphique de l’étude COURAGE(11) a aussi démontré que le taux d’événements (décès, infarctus) augmentait de façon significative dès 5 % d’ischémie (23 % vs 0 % en l’absence d’ischémie) et atteignait même 39,3 % chez les patients avec une ischémie étendue (≥ 10 % du myocarde). Il faut donc proposer une coronarographie aux patients avec une ischémie myocardique ≥ 10 % ce qui correspond en fonction des tests de dépistage à :
– une ischémie ≥ 2 segments sur 17 à la scintigraphie myocardique ;
– une anomalie de contraction de ≥ 3 segments sur 17 en échographie de stress ;
– une anomalie de contraction de ≥ 3 segments sur 17 ou une ischémie réversible de ≥ 10 % (soit ≥ 2 segments/17) du myocarde en IRM de stress ;
– un score de Duke (calculé à partir de la durée d’exercice, de la sévérité de l’angor et de l’importance du sous-décalage du segment ST) prédisant un taux de mortalité ≥ 3 % à l’épreuve d’effort.
Figure 2. Différence entre le traitement médical et la revascularisation myocardique chez le patient coronarien stable en fonction de l’importance de l’ischémie (Hachamovitch R, Circulation 2003).
Quels patients coronariens stables revasculariser ?
Le but de la revascularisation peut être double : soulager les symptômes notamment en cas d’échec du traitement médical (ce qui est assez rare) mais surtout modifier le pronostic cardiovasculaire du patient et éviter les événements futurs. Il est important de se rappeler que lorsqu’on prend en charge un patient coronarien en général entre 60-70 ans parfois plus jeune, on raisonne sur un patient qui a une espérance de vie d’au moins 20 ans. Malheureusement, le suivi dans nos études même dans les meilleurs cas est de 5 à 10 ans, ce qui rend difficile les extrapolations à plus long terme.
Ischémie myocardique > 10 %
Nous avons bien vu le caractère pronostique de l’ischémie. Dans l’étude scintigraphique de COURAGE, la réduction de l’ischémie myocardique (d’au moins 5 % du myocarde) améliorait le pronostic des patients par rapport à ceux qui conservaient la même ischémie myocardique. Il faut donc envisager une revascularisation chez les patients avec une ischémie myocardique ≥ 10 % pour réduire l’ischémie myocardique. Cette décision doit prendre en compte les caractéristiques anatomiques des lésions et les comorbidités afin d’évaluer le risque de cette revascularisation. L’étude ISCHEMIA (recrutement en cours, n ≈ 8 000 patients) compare le traitement médical à la revascularisation chez des patients coronariens stables avec une ischémie modérée (5-10 %) et nous donnera des nouvelles données.
Patients avec une dysfonction VG
Les patients avec une dysfonction VG sont des candidats idéaux à une revascularisation. L’étude CASS avait montré que le bénéfice de la revascularisation chirurgicale par rapport au traitement médical était particulièrement intéressant dans le sous-groupe des patients avec une dysfonction VG. Plus récemment, l’étude STICH chez des patients avec une FEVG < 35 % n’a pas démontré de différence sur la survie à 5 ans par rapport au traitement médical avec cependant une réduction sur la mortalité cardiovasculaire et un taux de cross-over important (17 %) dans le groupe traité médicalement(13).
Patients après un syndrome coronarien aigu
Plusieurs études ont montré l’intérêt de la revascularisation dans le sous-groupe des patients pluritronculaires après un syndrome coronaire aigu (revascularisé sur la lésion coupable) : l’étude DANAMI(14) chez les patients avec une ischémie après un IDM thrombolysé, l’étude SWISS II chez les patients stables avec un SCA récent (dans les 3 mois) et une ischémie silencieuse. Plus récemment, l’étude PRAMI(15) et l’étude CULPRIT ont comparé la revascularisation complète pendant la même procédure ou la même hospitalisation par rapport au traitement médical chez les patients avec un STEMI. Ces deux études ont montré un bénéfice de la revascularisation précoce. L’étude internationale multicentrique COMPLETE incluant 3 900 patients est en cours et confirmera peut-être ces résultats.
Patients coronariens pluritronculaires : intérêt de la FFR ?
Une métaanalyse de plusieurs études randomisées publiée par S. Yusuf et coll. en 1994 a montré la supériorité de la revascularisation chirurgicale par rapport au traitement médical chez les patients avec une sténose du TCCG et les patients pluritronculaires(17). L’étude MASS II plus récente (2010) avec un suivi clinique de 10 ans montre une supériorité de la chirurgie par rapport au traitement médical sur l’incidence des infarctus et des revascularisations sans différence sur la mortalité. Chez ces patients pluritronculaires, la revascularisation par angioplastie guidée par la FFR pourrait être très intéressante. L’étude FAME 2 a montré une supériorité de l’angioplastie guidée par FFR (Fractional Flow Reserve) par rapport au traitement médical sur les revascularisations urgentes mais pas sur la mortalité et les infarctus du myocarde chez des patients coronariens stables. L’étude BHF-FAMOUS NSTEMI trial présentée lors de l’ESC 2014 a montré l’intérêt de guider sa revascularisation par FFR par rapport à l’angioplastie conventionnelle chez les patients pluritronculaires avec un NSTEMI. L’étude FAME 3 va comparer l’angioplastie guidée par la FFR à la revascularisation chirurgicale chez les patients pluritronculaires avec comme critère principal la survenue des événements cardiovasculaires à un an.
Patients âgés
Les patients âgés sont également un sous-groupe qui mérite toute notre attention car ils sont de plus en plus fréquents. Les choix thérapeutiques sont bien sûr plus difficiles compte tenu des comorbidités (insuffisance rénale chronique, anémie chronique, saignements plus fréquents, polypathologie, etc.) rendant la revascularisation plus difficile et l’utilisation d’une double antiagrégation plaquettaire plus compliquée, mais ce sont souvent des patients qui bénéficient le plus de la revascularisation (ischémie myocardique importante, diminution des réhospitalisations, etc.). L’étude TIME(18) comparant le traitement médical à la revascularisation chez les patients ≥ 80 ans n’a pas montré de différence sur la mortalité à 3 ans mais il existait dans cette étude une amélioration des événements ischémiques non fatals dans le groupe revascularisé. Nous manquons cependant de données spécifiques et suffisantes dans cette population. Que faire par exemple chez un patient nonagénaire avec une lésion calcifiée du TCCG distal et asymptomatique sous traitement médical ? Personne n’a la réponse et le choix du patient reste déterminant dans la décision finale.
La revascularisation ? Oui, mais pour les coronariens les plus sévères
Ce sont clairement les patients les plus sévères qui bénéficient de la revascularisation comme le montre la sous-étude de COURAGE ou encore le registre CONFIRM. En revanche, un registre canadien(19) a montré qu’environ 20 % de patients avaient une revascularisation (angioplastie) non justifiée dont ils ne tiraient pas de bénéfice. Au contraire, les patients qui avaient une indication légitime de revascularisation (en fonction de la sévérité des symptômes, de l’ischémie, de la sévérité des lésions coronaires, etc.) ont clairement bénéficié de ce geste avec une réduction des événements cardiovasculaires par rapport au traitement médical lors du suivi.
La revascularisation doit s’adresser aux patients à haut risque. Il existe encore des patients les plus sévères qui devraient bénéficier d’une revascularisation et qui n’en bénéficient pas. Au contraire, il y a des patients à faible risque qui sont revascularisés et qui probablement ne bénéficient pas de ce geste.
Choix de la revascularisation et stratification du risque
Il reste enfin à définir le mode de revascularisation. Pendant longtemps et encore aujourd’hui, on cherche à opposer chirurgie et angioplastie avec des études au suivi trop court (même 5 ou 10 ans sont trop courts pour un coronarien de 60 ans). Ces techniques sont probablement beaucoup plus complémentaires qu’on ne veut le dire. Plusieurs métaanalyses et essais randomisés ont montré que la chirurgie et l’angioplastie faisait jeu égal sur la mortalité et la survenue d’infarctus mais il est vrai que l’angioplastie nécessite plus de revascularisations secondaires alors que la chirurgie offre un traitement plus « radical » d’emblée. L’étude SYNTAX a bien montré que la complexité des lésions anatomiques coronaires était un élément fondamental à prendre en considération pour l’angioplastie(20). En effet, les patients avec des lésions tritronculaires avec un score SYNTAX intermédiaire(23-32) et surtout élevé (≥ 33) doivent être orientés vers une revascularisation chirurgicale qui offrira moins d’événements cardiovasculaires dans le suivi (décès, IDM). De l’autre côté, la chirurgie devra évaluer l’ensemble des comorbidités du patient (notamment à l’aide de l’EuroScore II ou du STS score) afin d’évaluer le risque opératoire du patient. Au final, le choix médico-chirurgical de cette revascularisation doit faire l’objet d’une discussion transparente avec le patient et avec une équipe médico-chirurgicale notamment pour les patients pluritronculaires ou avec lésion du tronc commun (tableau 3). Voici les principales recommandations concernant la revascularisation, qui laissent une large place à la discussion pluridisciplinaire (figure 3) en fonction de l’expérience locale des équipes et des comorbidités du patient.
Figure 3. Algorithme de décision de revascularisation en fonction de l’anatomie coronaire du patient.
Patients diabétiques
Les patients diabétiques sont une population à très haut risque avec une morbi-mortalité cardiovasculaire supérieure à la population générale. La revascularisation chez ces patients reste encore un challenge et un domaine où l’on doit progresser. L’étude BARI 2D a montré l’efficacité du traitement médical en première intention par rapport à l’angioplastie(21). Cette étude a confirmé l’intérêt de la revascularisation chirurgicale par rapport au traitement médical chez les patients les plus sévères. L’étude FREEDOM(22) comparant la chirurgie de pontage par rapport à l’angioplastie chez les patients multitronculaires (83 % de tritronculaires) a montré sur un suivi clinique de 5 ans une supériorité de la chirurgie, notamment sur les infarctus et les décès cardiovasculaires même s’il y avait un peu plus d’AVC dans le groupe chirurgical. Du fait de la fréquence des lésions complexes chez les patients diabétiques, la chirurgie reste le traitement de référence et l’angioplastie ne sera proposée qu’après une analyse précise des lésions coronaires (score SYNTAX ≤ 22).
Patients avec une occlusion chronique
Les patients avec une occlusion chronique représentent environ 15 à 30 % des patients adressés pour une coronarographie selon les séries. La présence d’une occlusion chronique est associée à un moins bon pronostic. Une métaanalyse publiée en 2013(23) a montré une réduction de la mortalité chez les patients ayant bénéficié d’un succès de revascularisation par rapport à ceux qui gardaient une occlusion coronaire. La chirurgie de pontage doit bien évidemment être évoquée chez ces patients d’autant plus qu’il existe une lésion ou une occlusion sur l’IVA. Compte tenu des risques potentiels de l’angioplastie, celle-ci doit être réalisée après confirmation d’une ischémie myocardique importante (≥ 10 %) ou de symptômes réfractaires au traitement médical. Ces lésions restent également un challenge technique pour l’angioplasticien qui ne doit pas perdre de vue l’intérêt du patient. Ces angioplasties nécessitent un opérateur et une équipe entraînés (nécessité de matériel dédié, connaissance des différentes approches antérogrades et rétrogrades, etc.).
Avancées récentes et perspectives à venir pour nos patients coronariens
L’arrivée actuelle des stents biorésorbables va-t-elle permettre d’améliorer le pronostic à long terme de nos patients ? La disparition à terme du stent pour redonner à l’artère coronaire toute sa vasomotricité est un concept plutôt séduisant. L’étude ABSORB II présentée au TCT 2014 comparant le stent biorésorbable Absorb® au stent métallique Xience® a confirmé les espoirs de cette nouvelle génération de stents (événements cliniques similaires dans les deux groupes)(24). Nul doute que ces stents biorésorbables vont encore s’améliorer au fil des ans car leurs caractéristiques techniques restent une limite aujourd’hui.
Par ailleurs, l’environnement pharmacologique, notamment concernant l’antiagrégation plaquettaire, va aussi permettre d’améliorer encore le pronostic de nos revascularisations. L’arrivée de nouveaux inhibiteurs de P2Y12 (prasugrel et ticagrelor) a permis de réduire le taux de thrombose de stent lors d’un syndrome coronarien aigu. L’optimisation de ces traitements antiagrégants plaquettaires est très importante lors de la revascularisation. L’utilisation des tests d’agrégation plaquettaire permet d’identifier les patients à risque d’événements. Malheureusement, l’adaptation du traitement à partir du résultat des tests n’a pas permis de modifier le pronostic comme dans les études ARTIC ou TRIGGERPCI(25,26). Il reste donc des progrès à faire concernant le choix du test pour mesurer l’agrégation des patients, les cut-off utilisés et les stratégies d’adaptation médicamenteuse.
De plus, l’utilisation chronique du ticagrelor chez les patients diabétiques (étude THEMIS en cours) ou l’optimisation de l’administration de l’aspirine (en deux prises quotidiennes) qui est plus efficace biologiquement chez les patients diabétiques sont également de nouvelles perspectives thérapeutiques potentielles. Enfin, les premiers résultats avec les nouveaux hypolipémiants (anticorps monoclonal anti- PCSK9) sont très impressionnants sur le taux de LDL-cholestérol et nous attendons avec impatience les premiers résultats sur les événements cliniques.
Autant d’avancées techniques et thérapeutiques à venir qui permettront de sécuriser nos procédures de revascularisation dans les années à venir.
En pratique
Chez les patients coronariens stables, le traitement médical optimal en première intention est sûr et donne d’excellents résultats chez les patients à bas risque.
La coronarographie doit rester assez large, mais elle ne doit pas être suivie d’une revascularisation systématique.
La revascularisation myo cardique reste cependant nécessaire chez de nombreux patients malgré le traitement médical. Elle doit s’adresser aux patients à plus haut risque (ischémie importante) et non pas aux patients à bas risque qui n’en ont pas de bénéfice.
La revascularisation chez le coronarien stable n’est jamais une urgence (sauf cas exceptionnel) et doit être guidé par la sévérité des symptômes et de l’ischémie.
Le choix de la revascularisation doit prendre en compte les caractéristiques anatomiques ainsi que les comorbidités.
L’angioplastie ou la chirurgie doivent utiliser les techniques les plus récentes (FFR, stents actifs, pontages artériels, etc.). Des progrès vont probablement encore arriver dans les années à venir tant sur le plan médical que sur la revascularisation. Parmi les plus proches espoirs à venir, l’utilisation optimale des antiagrégants, l’arrivée des anti-PCSK9, l’utilisation de stents bio résorbables permettront peut-être encore une amélioration de la qualité de vie et du pronostic de nos coronariens stables.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :